Діючі речовини: Інфліксімаб
Remicade 100 мг порошок для концентрату для розчину для інфузій
Чому використовується Remicade? Для чого це?
Remicade містить діючу речовину під назвою інфліксимаб. Інфліксимаб - це білок людського та тваринного походження (від миші).
Remicade належить до групи ліків, які називаються "блокаторами ФНП". Застосовується у дорослих для лікування таких запальних захворювань:
- Ревматоїдний артрит
- Псоріатичний артрит
- Анкілозуючий спондиліт (хвороба Бехтерева)
- Псоріаз.
Remicade також застосовується у дорослих та дітей віком від 6 років для:
- Хвороба Крона
- Виразковий коліт.
Remicade діє, блокуючи дію білка, який називається «фактором некрозу пухлини альфа» (TNFα). Цей білок бере участь у запальних процесах організму, і, блокуючи його, можна зменшити запалення в організмі.
Ревматоїдний артрит
Ревматоїдний артрит - це запальне захворювання суглобів. Якщо у вас ревматоїдний артрит, вам спочатку буде надано лікування іншими препаратами. Якщо ви не реагуєте належним чином на ці ліки, вам буде надано лікування препаратом Ремікейд у поєднанні з іншим препаратом, що називається метотрексатом:
- Зменшити ознаки та симптоми хвороби,
- Уповільнює прогресування пошкодження суглобів,
- Поліпшити фізичні функції.
Псоріатичний артрит
Псоріатичний артрит - це запальне захворювання суглобів, яке зазвичай супроводжується псоріазом. Якщо у вас псоріатичний артрит, вам спочатку будуть призначені інші ліки. Якщо ви не реагуєте належним чином на ці ліки, вам буде надано лікування препаратом Ремікейд:
- Зменшити ознаки та симптоми захворювання,
- Уповільнюють прогресування пошкодження суглобів,
- Поліпшити фізичні функції.
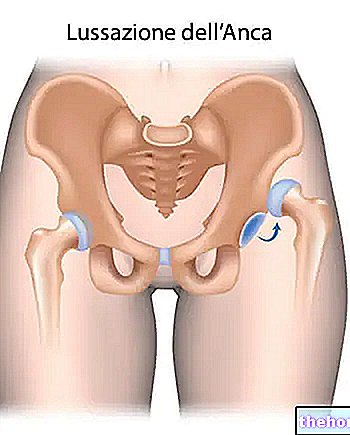
Анкілозуючий спондиліт (хвороба Бехтерева)
Анкілозуючий спондиліт - це запальне захворювання хребта. Якщо у вас хвороба Бехтерева, вам спочатку будуть призначені інші ліки. Якщо Ви не реагуєте належним чином на ці ліки, Ви будете отримувати Ремікейд:
- Зменшити ознаки та симптоми захворювання,
- Поліпшити фізичні функції.
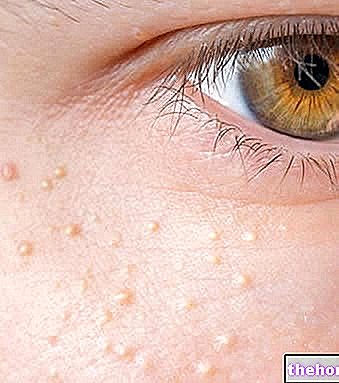
Псоріаз
Псоріаз - запальне захворювання шкіри. Якщо у вас псоріаз бляшок помірного та важкого ступеня, вам спочатку будуть призначені інші ліки або інші методи лікування, наприклад фототерапія. Якщо ви не реагуєте належним чином на ці ліки або лікування, вам буде призначено лікування препаратом Ремікейд, щоб зменшити ознаки та симптоми вашого захворювання.
Виразковий коліт
Виразковий коліт - це запальне захворювання кишечника. Якщо у вас виразковий коліт, вам спочатку будуть призначені інші ліки. Якщо ви не реагуєте належним чином на ці ліки, вам буде призначено Ремікейд для лікування захворювання.
Хвороба Крона
Хвороба Крона - це запальне захворювання кишечника. Якщо у вас хвороба Крона, вам спочатку будуть призначені інші ліки. Якщо ви не реагуєте належним чином на ці ліки, вам буде призначено лікування препаратом Ремікейд для: • лікування активної хвороби Крона • зменшення кількості аномальних отворів (свищів) між кишечником і шкірою, для яких інші ліки або операція виявилися недостатніми.
Протипоказання, коли Remicade не слід застосовувати
Вам не слід вводити Remicade, якщо:
- у вас алергія на інфліксимаб (діюча речовина у препараті Ремікейд) або на будь -який інший інгредієнт цього препарату (перерахований у розділі 6)
- у вас алергія (гіперчутливість) до білків миші
- хворі на туберкульоз (ТБ) або "іншу серйозну інфекцію, таку як пневмонія або сепсис
- мають «помірну або важку серцеву недостатність.
Не приймайте Remicade, якщо будь -яка з вищезазначених умов стосується вас. Якщо ви не впевнені, поговоріть зі своїм лікарем перед тим, як вам дадуть Ремікейд
Заходи безпеки при застосуванні Що потрібно знати, перш ніж приймати Remicade
Поговоріть зі своїм лікарем перед тим, як вам буде призначено Ремікейд, якщо у вас є:
Раніше отримував Remicade
- Скажіть своєму лікарю, якщо ви раніше отримували Ремікейд, і якщо Ви знову розпочинаєте лікування Ремікейдом.
Якщо Ви припинили прийом Ремікейд більше ніж на 16 тижнів, під час повторного запуску Ремікейд підвищується ризик розвитку алергічних реакцій.
Інфекції
Скажіть своєму лікарю, якщо у вас «інфекція, навіть дуже незначна, перед тим, як вам дадуть Ремікейд
- Скажіть своєму лікарю перед тим, як вам буде надано Ремікейд, якщо ви жили або подорожували "місцем, де поширені інфекції, що називаються гістоплазмозом, кокцидіоїдозом або бластомікозом. Ці інфекції викликані певними типами грибків, які можуть вражати легені або інші частини тіло. тіло
- Ви можете бути більш схильні до інфекцій при лікуванні Remicade. Якщо вам 65 років або старше, ви маєте більший ризик
- Ці інфекції можуть бути серйозними і включати туберкульоз, інфекції, викликані вірусами, грибками або бактеріями, або інші умовно-патогенні інфекції та сепсис, які в рідкісних випадках можуть бути небезпечними для життя.
Негайно повідомте свого лікаря, якщо під час лікування препаратом Ремікейд у вас виникнуть симптоми інфекції. Симптоми включають лихоманку, кашель, грипоподібні симптоми, погане самопочуття, почервоніння або дуже гарячу шкіру, рани або проблеми з зубами. Ваш лікар може порекомендувати тимчасову зупинку Remicade.
Туберкульоз (ТБ)
- Дуже важливо повідомити свого лікаря, якщо ви коли -небудь хворіли на туберкульоз, або якщо ви тісно контактували з людьми, які хворіли або хворіли на туберкульоз
- Ваш лікар зробить аналізи на наявність туберкульозу. Було зареєстровано кілька випадків туберкульозу у пацієнтів, які отримували Ремікейд, в рідкісних випадках навіть у пацієнтів, які проходили лікування протитуберкульозними препаратами. Лікар запише ці аналізи на картку оповіщення пацієнта
- Якщо ваш лікар вважає, що ви ризикуєте захворіти на туберкульоз, перед введенням препарату Ремікейд ви можете пройти курс лікування проти туберкульозу.
Негайно повідомте лікаря, якщо під час прийому Ремікейд ви помітили будь -які ознаки туберкульозу. Ознаки включають постійний кашель, втрату ваги, відчуття втоми, лихоманку, нічну пітливість.
Вірус гепатиту В (HBV)
- Скажіть своєму лікарю, якщо ви є носієм, чи хворіли або хворіли на гепатит В до того, як вам призначили Ремікейд
- Скажіть своєму лікарю, якщо ви вважаєте, що ризикуєте заразитися гепатитом В.
- Чи повинен лікар оцінити, чи є у вас гепатит В? Лікування блокаторами TNF, такими як Remicade, може викликати реактивацію вірусу гепатиту В у пацієнтів з цим вірусом, що в деяких випадках може призвести до смерті.
Проблеми з серцем
- Повідомте лікаря, якщо у вас є проблеми з серцем, наприклад, легка серцева недостатність
- Ваш лікар буде уважно стежити за вашою функцією серця.
Негайно повідомте лікаря, якщо під час лікування Ремікейдом ви помітили нові або погіршення ознак серцевої недостатності. Ознаки включають задишку або набряк ніг.
Рак і лімфома
- Скажіть своєму лікарю, якщо у вас була або коли -небудь була лімфома (тип раку крові) або інші види раку, перш ніж вам буде надано Ремікейд
- Пацієнти з важким ревматоїдним артритом, які тривалий час страждали від цього захворювання, можуть мати вищий за середній ризик розвитку лімфоми.
- Діти та дорослі, які приймають Ремікейд, можуть мати підвищений ризик розвитку лімфоми або іншого виду раку.
- Деякі пацієнти, які отримували лікування блокаторами ФНП, включаючи Ремікейд, захворіли на рідкісний тип раку, який називається гепатоспленочна Т-клітинна лімфома. Більшість із цих пацієнтів були підлітками або молодими дорослими чоловіками, і більшість з них мали хронічний або виразковий коліт. Цей вид раку зазвичай смертельний. Майже всі пацієнти на додаток до блокаторів ФНП також отримували ліки під назвою азатіоприн або 6-меркаптопурин.
- У деяких пацієнтів, які отримували інфліксимаб, розвинулися певні типи раку шкіри. Якщо під час або після терапії ви відчуваєте будь -які зміни у зовнішньому вигляді шкіри або нарости на шкірі, повідомте про це свого лікаря.
Хвороби легенів або сильне куріння
- Скажіть своєму лікарю, якщо у вас є захворювання легенів, яке називається хронічною обструктивною хворобою легень (ХОЗЛ), або ви завзято курите, перш ніж приймати Ремікейд
- Пацієнти з ХОЗЛ та сильні курці можуть мати підвищений ризик розвитку раку під час лікування препаратом Ремікейд.
Захворювання нервової системи
- Скажіть своєму лікарю, якщо у вас були або коли -небудь були проблеми з нервовою системою, перш ніж ви отримаєте Ремікейд. Це включає розсіяний склероз, синдром Гійєна-Барре, напади або діагноз «неврит зорового нерва».
Негайно повідомте лікаря, якщо під час прийому Ремікейд ви помітили симптоми нервового захворювання. Ознаки включають зміни зору, слабкість в руках і ногах, оніміння або поколювання в будь -якій частині тіла.
Аномальні шкірні отвори
- Скажіть своєму лікарю, якщо у вас є якісь ненормальні отвори на шкірі (свищі), перш ніж ви отримаєте Ремікейд.
Щеплення
- Скажіть своєму лікарю, якщо ви нещодавно були щеплені або плануєте щеплення
- Ви не повинні отримувати жодних вакцин під час лікування препаратом Ремікейд
- Деякі щеплення можуть викликати інфекції. Якщо ви отримували Remicade під час вагітності, у вашої дитини може бути підвищений ризик зараження цією інфекцією протягом приблизно шести місяців після останньої дози, отриманої під час вагітності. Важливо повідомити свого педіатра та інших медичних працівників про застосування Remicade, щоб він вирішив коли Ваша дитина повинна отримати будь -які вакцини.
Інфекційні терапевтичні засоби
- Поговоріть зі своїм лікарем, якщо ви нещодавно приймали або плануєте лікування інфекційним терапевтичним засобом (наприклад, ін'єкція БЦЖ, що використовується для лікування раку).
Стоматологічні операції або процедури
- Скажіть своєму лікарю, якщо ви збираєтесь проходити якісь стоматологічні процедури або лікування
- Повідомте хірурга або стоматолога, який виконує процедуру, що ви проходите курс лікування Remicade, показавши картку оповіщення пацієнта.
Діти та підлітки
Наведена вище інформація стосується також дітей та підлітків. Крім того:
- у деяких дітей та підлітків, які приймали ліки, що блокують ФНП, такі як Remicade, розвинулися ракові захворювання, включаючи незвичайні типи, які іноді були летальними.
- У порівнянні з дорослими, у більшої кількості дітей, які приймали Ремікейд, розвинулися інфекції
- Діти повинні отримати рекомендовані щеплення перед початком лікування Ремікейдом.
Якщо ви не впевнені, що будь -яка з вищезазначених умов стосується вас, зверніться до лікаря перед тим, як вам буде призначено Ремікейд.
Взаємодії Які препарати або продукти харчування можуть змінити ефект Remicade
Пацієнти із запальними захворюваннями вже приймають ліки для лікування хвороби. Ці ліки можуть викликати побічні ефекти. Ваш лікар порадить вам, які інші ліки слід продовжувати приймати під час лікування препаратом Ремікейд.
Скажіть своєму лікарю, якщо ви приймаєте або нещодавно приймали будь -які інші ліки, включаючи будь -які інші ліки для лікування хвороби Крона, виразкового коліту, ревматоїдного артриту, хвороби Бехтерева, псоріатичного артриту чи псоріазу, або ліків, які ви отримуєте без рецепта, таких як вітаміни та трави препарати.
Зокрема, повідомте свого лікаря, якщо ви використовуєте будь -яке з цих ліків:
- Ліки, що впливають на імунну систему
- Кінерет (анакінра). Ремікад і Кінерет не можна вводити разом
- Оренсія (абатацепт). Ремікаде та Оренсія не можна давати разом.
Якщо ви не впевнені, що будь -яка з вищезазначених умов стосується вас, зверніться до лікаря перед тим, як вам буде призначено Ремікейд.
Попередження Важливо знати, що:
Вагітність, грудне вигодовування та фертильність
- Якщо ви вагітні або годуєте грудьми, думаєте, що можете бути вагітними або плануєте народження дитини, зверніться до лікаря за порадою, перш ніж приймати ці ліки. Ремікад не рекомендується під час вагітності
- Вам слід уникати вагітності під час лікування препаратом Ремікейд та принаймні 6 місяців після припинення лікування.
- Не годуйте грудьми під час лікування препаратом Ремікейд або протягом 6 місяців після останнього лікування препаратом Ремікейд
- Якщо ви отримували Ремікейд під час вагітності, у вашої дитини може бути підвищений ризик зараження. Важливо повідомити свого педіатра та інших медичних працівників про ваше застосування Ремікейд до того, як Ваша дитина отримає будь -які вакцини (докладніше див. Розділ про вакцинацію) ).
Водіння автомобіля та роботу з машинами
Навряд чи Remicade вплине на вашу здатність керувати автомобілем або працювати з механізмами. Якщо ви відчуваєте втому або погане самопочуття після лікування препаратом Ремікейд, не слід керувати транспортними засобами та працювати з будь -якими інструментами чи машинами.
Доза, спосіб та час введення Як використовувати Remicade: дозування
Як дається Remicade
- Remicade вам дасть лікар або медсестра
- Ваш лікар або медсестра приготують розчин Remicade для ін’єкцій
- Розчин Remicade вводиться повільно (протягом 2 годин) у вену, зазвичай в руку. Ця процедура називається «внутрішньовенною інфузією» або крапельницею. Після третього курсу лікування ваш лікар може прийняти рішення про призначення препарату Ремікейд протягом 1 години
- Під час введення препарату Ремікейд та протягом 1–2 годин за вами буде здійснюватися нагляд.
Скільки дається Remicade
- Ваш лікар визначить дозу (у мг) та інтервал між прийомами Ремікейду. Це буде залежати від вашого захворювання, ваги та реакції на лікування.
- У наведеній нижче таблиці наведено частоту введення цього препарату.
Ревматоїдний артрит
Звичайна доза становить 3 мг на кожен кг маси тіла
Псоріатичний артрит, анкілозуючий спондиліт (хвороба Бехтерева), псоріаз, виразковий коліт та хвороба Крона
Звичайна доза становить 5 мг на кожен кг маси тіла.
Застосування у дітей та підлітків
Ремікейд можна застосовувати тільки у дітей при хворобі Крона або виразковому коліті. Ці діти повинні бути віком від 6 років.
Передозування Що робити, якщо ви прийняли занадто багато Remicade
Якщо Ви отримаєте більше Remicade, ніж Вам потрібно
Оскільки цей лікарський засіб вам надає лікар або медсестра, малоймовірно, що ви отримаєте занадто багато. Немає відомих побічних ефектів передозування Remicade.
Якщо ви забули або пропустили інфузію "Remicade"
Якщо ви забули або пропустили зустріч для введення Remicade, запишіться на іншу зустріч якомога швидше.
Якщо у вас виникнуть додаткові запитання щодо застосування цього препарату, зверніться до лікаря
Побічні ефекти Які побічні ефекти Remicade
Як і всі ліки, цей препарат може викликати побічні ефекти, хоча вони виникають не у всіх. Більшість з цих ефектів є легкими або помірними. Однак деякі пацієнти можуть відчувати серйозні побічні ефекти і вимагати медичного лікування. Побічні ефекти також можуть виникнути після закінчення лікування Ремікейдом.
Негайно повідомте лікаря, якщо ви помітили будь -який з наступних побічних ефектів:
- Ознаки алергічної реакції, такі як набряк обличчя, губ, рота або горла, що може спричинити утруднення ковтання або дихання, висип, кропив’янка, набряк кистей, стоп або щиколоток. Алергічна реакція може виникнути протягом 2 годин після ін’єкції або пізніше. Інші ознаки алергічної реакції, які можуть виникнути до 12 днів після ін’єкції, включають м’язові болі, лихоманку, біль у суглобах або щелепах, біль у горлі або біль у горлі.
- Ознаки проблеми з серцем, такі як задишка, набряк ніг або зміна серцебиття
- Ознаки інфекції (включаючи туберкульоз), такі як лихоманка, почуття втоми, кашель (постійний), задишка, грипоподібні симптоми, втрата ваги, нічна пітливість, діарея, рани, проблеми з зубами або печіння під час сечовипускання
- Ознаки проблеми з легенями, такі як кашель, утруднене дихання або стиснення в грудях
- Ознаки неврологічних проблем (включаючи проблеми з очима), такі як судоми, поколювання або оніміння будь -якої частини тіла, слабкість у руках або ногах, зміни зору, такі як подвійне бачення або інші проблеми з очима
- Ознаки проблеми з печінкою, такі як пожовтіння шкіри або очей, темно -коричнева сеча або біль у верхній правій частині живота, лихоманка
- Ознаки розладу імунної системи, званого вовчаком, такі як біль у суглобах або висип на щоках або руках, чутливі до сонця ділянки
- Ознаки зменшення кількості клітин крові, такі як стійка лихоманка, кровотеча або синці частіше або бліді.
Якщо ви помітили будь -який із описаних вище симптомів, негайно повідомте лікаря.
Дуже поширені побічні ефекти (виникають більш ніж у 1 з 10 пацієнтів)
- Біль у шлунку, нездужання
- Вірусні інфекції, такі як герпес або грип
- Інфекції верхніх дихальних шляхів, такі як гайморит
- Головний біль
- Небажаний ефект через інфузію
- Біль.
Поширені побічні ефекти (вражають від 1 до 10 користувачів на 100)
- Зміни функції печінки, збільшення печінкових ферментів (спостерігається в аналізах крові)
- Інфекції легенів або грудної клітини, такі як бронхіт або пневмонія
- Труднощі з диханням або біль при диханні, біль у грудях
- Кровотеча в шлунку або кишечнику, діарея, розлад травлення, печія, запор
- Кропив’янка-подібний висип, сверблячий висип або сухість шкіри
- Проблеми з рівновагою або відчуття запаморочення
- Лихоманка, підвищена пітливість
- Проблеми з кровообігом, такі як низький або високий кров'яний тиск
- Синці, почервоніння або кровотеча з носа, гаряча, червона шкіра (почервоніння)
- Відчуття втоми або слабкості
- Бактеріальні інфекції, такі як генералізована інфекція, абсцес або інфекція глибоких шарів шкіри (целюліт)
- Проблеми з кров’ю, такі як анемія або низький рівень лейкоцитів
- Збільшені лімфатичні вузли
- Депресія, порушення сну
- Проблеми з очима, включаючи почервоніння очей та інфекції
- Прискорене серцебиття (тахікардія) або серцебиття
- Біль у суглобах, м’язах або спині
- Інфекції сечовивідних шляхів
- Псоріаз, шкірні проблеми, такі як екзема та випадання волосся
- Реакції в місці ін’єкції, такі як біль, набряк, почервоніння або свербіж
- Озноб, скупчення рідини під шкірою, що викликає набряк
- Відчуття оніміння або поколювання.
Нечасті побічні ефекти (вражають від 1 до 10 користувачів на 1000)
- Погане кровопостачання, набряк вени
- Шкірні проблеми, такі як утворення пухирів, бородавок, аномальне зміна кольору або пігментація шкіри або набряклі губи
- Важкі алергічні реакції (наприклад, анафілаксія), порушення імунної системи, що називається вовчаком, алергічні реакції на чужорідні білки
- Рани, які повільно гояться
- Набряк печінки (гепатит) або жовчного міхура (жовчний міхур), пошкодження печінки
- Відволікання, дратівливість, розгубленість, нервозність
- Проблеми з очима, включаючи помутніння або зниження зору, набряклість очей або ялинки
- Нова або погіршена серцева недостатність, уповільнений пульс
- Непритомність
- Судоми, нервові розлади
- Перфорація кишечника або закупорка кишечника, біль у животі або судоми
- Набряк підшлункової залози (панкреатит)
- Грибкові інфекції, такі як дріжджові інфекції
- Проблеми з легенями (наприклад, набряк)
- Надлишок рідини навколо легенів (плевральний випіт)
- Інфекції нирок
- Низька кількість тромбоцитів, надмірна кількість лейкоцитів
- Інфекції у піхві.
Рідкісні побічні ефекти (вражають від 1 до 10 користувачів на 10000)
- Тип раку крові (лімфома)
- Погане надходження кисню до органів через кров, проблеми з кровообігом, такі як звуження судини
- Запалення мембрани, що вистилає мозок (менінгіт)
- Інфекції через ослаблення імунної системи
- Інфекція гепатиту В, якщо у вас раніше був гепатит В? Набряк або зростання аномальних тканин
- Набряк дрібних кровоносних судин (васкуліт)? Імунологічні порушення, які можуть вражати легені, шкіру та лімфатичні вузли (наприклад, саркоїдоз)
- Відсутність інтересу чи емоцій
- Серйозні шкірні проблеми, такі як токсичний епідермальний некроліз, синдром Стівена-Джонсона або мультиформна еритема, шкірні проблеми, такі як фурункули
- Серйозні розлади нервової системи, такі як поперечний мієліт, хвороба, подібна до розсіяного склерозу, неврит зорового нерва та синдром Гійєна-Барре
- Рідина в мембрані, що вистилає серце (перикардіальний випіт)
- Важкі проблеми з легенями (наприклад, інтерстиціальна пневмонія)
- Меланома (тип раку шкіри).
Інші побічні ефекти (частота невідома)
- Рак у дітей і дорослих
- Рідкісний рак крові, який вражає переважно молодих людей (гепатоспленочна Т-клітинна лімфома)
- Печінкова недостатність
- Меркель -клітинний рак (тип раку шкіри)
- Погіршення стану, званого дерматоміозитом (виглядає як «висип, що супроводжує м’язову слабкість).
Додаткові побічні ефекти у дітей та підлітків
Діти, які приймали Ремікейд від хвороби Крона, показали деякі відмінності у побічних ефектах порівняно з дорослими, які приймали Ремікейд від хвороби Крона.
Найбільш поширеними побічними ефектами у дітей були: низька кількість еритроцитів (анемія), кров у калі, низька кількість лейкоцитів (лейкопенія), припливи або почервоніння (припливи), вірусні інфекції, низька кількість нейтрофілів (нейтропенія), які - це білі кров'яні клітини, які борються з інфекцією, переломом кісток, бактеріальною інфекцією та алергічними реакціями дихальних шляхів.
Повідомлення про побічні ефекти
Якщо у вас виникли будь -які побічні ефекти, зверніться до свого лікаря, фармацевта чи медсестри.Це включає будь -які можливі побічні ефекти, не зазначені у цій брошурі. Ви також можете повідомити про побічні ефекти безпосередньо за допомогою національної системи повідомлень, наведеної у Додатку V. Побічні ефекти, які ви можете допомогти надайте додаткову інформацію про безпеку цього препарату.
Термін придатності та утримання
Зазвичай Remicade зберігатимуться медичними працівниками. Якщо вам це потрібно, відомості про збереження виглядають наступним чином:
- Зберігайте цей препарат подалі від очей та недоступного для дітей місця.
- Не використовуйте цей препарат після закінчення терміну придатності, зазначеного на етикетці та картонній упаковці після "EXP". Термін придатності відноситься до останнього дня цього місяця.
- Зберігати в холодильнику (2 ° C - 8 ° C).
- Цей препарат також можна зберігати в оригінальній коробці поза холодильником при температурі максимум 25 ° C протягом одного періоду до шести місяців. У такій ситуації його не слід знову зберігати в холодильнику. Напишіть на коробці новий термін придатності, включаючи день / місяць / рік. Викиньте цей лікарський засіб, якщо він не використовується до нового терміну придатності або до закінчення терміну придатності, надрукованого на картонній упаковці, залежно від того, що настане раніше.
- Коли Remicade готується до інфузії, рекомендується використати його якомога швидше (протягом 3 годин) .Однак, якщо розчин готується в умовах, повністю вільних від мікробів, його можна зберігати у холодильнику протягом 24 годин між 2 ° C і 8 ° C.
- Не використовуйте цей препарат, якщо він знебарвлений або містить частинки.
Що містить Remicade
- Діюча речовина - інфліксимаб. Кожен флакон містить 100 мг інфліксимабу. Після приготування кожен мл містить 10 мг інфліксимабу.
- Інші інгредієнти: сахароза, полісорбат 80, одноосновний фосфат натрію та двоосновний фосфат натрію.
Як виглядає Remicade та вміст упаковки
Remicade поставляється у скляному флаконі, що містить порошок для концентрату для розчину для інфузій. Порошок складається з ліофілізованих білих гранул.
Remicade випускається в упаковках по 1, 2, 3, 4 або 5 флаконів. Не всі розміри упаковок можна продати
Джерело з інформацією про упаковку: AIFA (Італійське агентство з лікарських засобів). Вміст, опублікований у січні 2016 р. Наявна інформація може бути не актуальною.
Щоб мати доступ до найновішої версії, бажано зайти на веб-сайт AIFA (Італійське агентство з лікарських засобів). Відмова від відповідальності та корисна інформація.
01.0 НАЗВА ЛЕКАРСТВЕННОГО ПРОДУКТУ
Порошок REMICADE 100 мг для концентрату для розчину для інфузій
02.0 ЯКІСНИЙ І КІЛЬКІСНИЙ СКЛАД
Кожен флакон містить 100 мг інфліксимабу. Інфліксимаб-це химерне моноклональне антитіло IgG1 людини-миші, що виробляється в клітинах гібридом мишей за технологією рекомбінантної ДНК. Після розчинення кожен мл містить 10 мг інфліксимабу.
Повний список допоміжних речовин див. У розділі 6.1.
03.0 ФАРМАЦЕВТИЧНА ФОРМА
Порошок для концентрату для розчину для інфузій.
Порошок складається з ліофілізованих білих гранул.
04.0 КЛІНІЧНА ІНФОРМАЦІЯ
04.1 Терапевтичні показання
Ревматоїдний артрит
Ремікад у поєднанні з метотрексатом показаний для зменшення ознак та симптомів та поліпшення фізичних функцій при:
• дорослі пацієнти з активним захворюванням, коли відповідь на модифіковані хворобою протиревматичні препарати (ДМАРД), включаючи метотрексат, була недостатньою.
• дорослі пацієнти з важким, активним і прогресуючим захворюванням, які раніше не лікувалися метотрексатом або іншими DMARD.
Рентгенологічне обстеження цієї популяції пацієнтів показало зменшення швидкості прогресування пошкодження суглобів (див. Розділ 5.1).
Хвороба Крона у дорослих
Remicade призначений для:
• лікування помірної та важкої активної хвороби Крона у дорослих пацієнтів, які не давали відповіді, незважаючи на повне та адекватне лікування кортикостероїдами та / або імунодепресантами; або у пацієнтів, які не переносять або мають медичні протипоказання до вищезгаданої терапії.
• лікування активної фістулізуючої хвороби Крона у дорослих пацієнтів, які не змогли відповісти, незважаючи на повний і адекватний курс терапії звичайним лікуванням (включаючи антибіотики, дренаж та імуносупресивну терапію).
Хвороба Крона у дітей
Remicade показаний для лікування важкої активної хвороби Крона, у дітей та підлітків у віці 6-17 років, які не відповіли на звичайну терапію кортикостероїдами, імуномодуляторами та первинною дієтою, або у пацієнтів, які не переносять або мають протипоказання для вищезгаданої терапії. Remicade вивчався лише в поєднанні зі звичайною імуносупресивною терапією.
Виразковий коліт
Remicade призначений для лікування помірного та важкого активного виразкового коліту у дорослих пацієнтів, які не реагували належним чином на звичайну терапію, включаючи кортикостероїди та 6-меркаптопурин (6-МП) або азатіоприн (AZA), або мають непереносимість або для яких існує медичне протипоказання до цієї терапії.
Виразковий коліт у дітей
Remicade призначається для лікування важкого, активного виразкового коліту у дітей та підлітків віком від 6 до 17 років, які не реагували належним чином на традиційну терапію, включаючи кортикостероїди та 6-МП або АЗА, або мають непереносимість або для яких є медична допомога протипоказання до цієї терапії.
Хвороба Марі-Штрюмпеля
Remicade показаний для лікування важкого, активного анкилозирующего спондилоартриту у дорослих пацієнтів, які не реагували належним чином на звичайну терапію.
Псоріатичний артрит
Remicade показаний для лікування активного та прогресуючого псоріатичного артриту у дорослих пацієнтів, коли відповідь на попереднє лікування DMARD була недостатньою.
Remicade слід надати:
• у поєднанні з метотрексатом
• або окремо у пацієнтів, які мають непереносимість метотрексату або яким він протипоказаний
Було показано, що Remicade покращує фізичні функції у пацієнтів з псоріатичним артритом та зменшує швидкість прогресування периферичного пошкодження суглоба, що вимірюється за допомогою рентгенівського випромінювання у пацієнтів із симетричними поліартикулярними підтипами захворювання (див. Розділ 5.1).
Псоріаз
Remicade показаний для лікування помірного та важкого бляшкового псоріазу у дорослих пацієнтів, які зазнали невдачі або мають протипоказання або мали непереносимість інших системних засобів, включаючи циклоспорин, метотрексат або PUVA (див. Розділ 5.1).
04.2 Дозування та спосіб введення
Лікування Remicade має розпочинати та контролювати лікар -спеціаліст, який має досвід у діагностиці та лікуванні ревматоїдного артриту, запального захворювання кишечника, хвороби Бехтерева, псоріатичного артриту чи псоріазу. Remicade необхідно вводити внутрішньовенно. Інфузії Remicade повинні вводити кваліфіковані медичні працівники, навчені розпізнавати будь-які проблеми, пов’язані з інфузією.
Під час лікування Ремікейдом слід оптимізувати застосування інших супутніх методів лікування, таких як кортикостероїди та імунодепресанти.
Дозування
Дорослі (≥ 18 років)
Ревматоїдний артрит
Внутрішньовенна інфузія 3 мг / кг з наступними інфузіями по 3 мг / кг на 2 та 6 тижнях після першої інфузії, потім кожні 8 тижнів.
Remicade слід вводити одночасно з метотрексатом.
Наявні дані свідчать про те, що клінічна відповідь зазвичай досягається протягом 12 тижнів від початку лікування. Якщо у пацієнта є неадекватна відповідь або вона втрачає відповідь після цього періоду, можна розглянути можливість поступового збільшення дози 1,5 мг. / Кг, максимум 7,5 мг / кг кожні 8 тижнів. Крім того, можна розглянути можливість введення 3 мг / кг кожні 4 тижні. Якщо досягається адекватна відповідь, лікування слід продовжувати. продовжувати терапію у пацієнтів, у яких немає доказів терапевтичної користі протягом перших 12 тижнів лікування або після коригування дози.
Помірна або важка активна хвороба Крона
5 мг / кг у вигляді внутрішньовенної інфузії з подальшою інфузією 5 мг / кг через 2 тижні після першої інфузії. Якщо пацієнт не реагує на терапію після 2 доз, подальше лікування інфліксимабом проводити не слід. Наявні дані не підтверджують подальше лікування інфліксимабом у пацієнтів, які не є пацієнтами респонденти протягом 6 тижнів після першої інфузії.
У пацієнтів, які відповіли, альтернативними рішеннями для продовження лікування є:
• Технічне обслуговування: додаткова інфузія в дозі 5 мг / кг на 6 тижні після першої дози, після чого повторні інфузії кожні 8 тижнів або
• Повторне введення: інфузія 5 мг / кг, якщо ознаки та симптоми захворювання зберігаються (див. Розділ «Повторне введення» та розділ 4.4).
Хоча порівняльних даних бракує, обмежені дані щодо пацієнтів, які спочатку відповіли на терапію 5 мг / кг, але втратили відповідь, вказують на те, що деякі пацієнти можуть відновити відповідь, збільшивши дозу (див. Розділ 5.1). Необхідно ретельно переглянути продовження терапії у пацієнтів, у яких після коригування дози немає доказів терапевтичної користі.
Активна фістулізуюча хвороба Крона
5 мг / кг у вигляді внутрішньовенної інфузії з подальшим введенням 5 мг / кг на 2 та 6 тижні після першої інфузії. Якщо пацієнт не реагує після 3 -х доз, подальше лікування інфліксимабом проводити не слід.
У пацієнтів, які відповіли, альтернативними рішеннями для продовження лікування є:
• Технічне обслуговування: додаткові інфузії по 5 мг / кг кожні 8 тижнів або
• Повторне введення: інфузія 5 мг / кг, якщо ознаки та симптоми захворювання зберігаються, потім вливання 5 мг / кг кожні 8 тижнів (див. Розділ «Повторне введення» та розділ 4.4).
Хоча порівняльних даних бракує, обмежені дані щодо пацієнтів, які спочатку відповіли на терапію 5 мг / кг, але втратили відповідь, свідчать про те, що деякі пацієнти можуть відновити відповідь, збільшивши дозу (див. Розділ 5.1). Необхідно ретельно переглянути продовження терапії у пацієнтів, у яких після коригування дози немає доказів терапевтичної користі.
При хворобі Крона досвід повторного застосування, якщо ознаки та симптоми захворювання зберігаються, є обмеженим, і немає порівняльних даних про ризик / користь альтернативних рішень для продовження лікування.
Виразковий коліт
Внутрішньовенна інфузія у дозі 5 мг / кг з подальшим введенням 5 мг / кг на 2 та 6 тижні після першої інфузії, потім повторюється кожні 8 тижнів.
Наявні дані свідчать про те, що клінічна відповідь зазвичай досягається протягом 14 тижнів після початку лікування, тобто після трьох введення.
Хвороба Марі-Штрюмпеля
Внутрішньовенна інфузія у дозі 5 мг / кг з наступними інфузіями у дозі 5 мг / кг через 2 та 6 тижні після першої інфузії, потім повторюється через 6-8 тижнів. Якщо пацієнт не реагує протягом 6 тижнів (тобто після 2 доз), він не повинен отримувати подальшого лікування інфліксимабом.
Псоріатичний артрит
Внутрішньовенна інфузія у дозі 5 мг / кг з подальшим введенням 5 мг / кг на 2 та 6 тижні після першої інфузії, потім повторюється кожні 8 тижнів.
Псоріаз
Внутрішньовенна інфузія у дозі 5 мг / кг з подальшим введенням 5 мг / кг на 2 та 6 тижні після першої інфузії, потім повторюється кожні 8 тижнів. Якщо пацієнт не реагує протягом 14 тижнів (тобто після 4 доз), подальше лікування інфліксимабом не повинно проводитися.
Повторне введення при хворобі Крона та ревматоїдному артриті
Якщо ознаки та симптоми захворювання повторюються, Remicade можна повторно ввести протягом 16 тижнів після останньої інфузії. У клінічних дослідженнях затримка реакцій гіперчутливості була «нечастою» і виникала через проміжки часу без застосування Remicade. Менше 1 року (див. Розділи 4.4 та 4.8). Безпека та ефективність повторного введення не були встановлені після більш ніж 16 тижнів без застосування препарату Ремікейд. Це стосується як пацієнтів з хворобою Крона, так і пацієнтів з ревматоїдним артритом.
Повторне введення при виразковому коліті
Безпека та ефективність повторного введення через інтервали, що не перевищують 8 тижнів, не встановлені (див. Розділи 4.4 та 4.8).
Повторне введення при анкілозуючому спондиліті
Безпека та ефективність повторного введення, крім тих, які вводяться з інтервалом від 6 до 8 тижнів, не встановлені (див. Розділи 4.4 та 4.8).
Повторне введення при псоріатичному артриті
Безпека та ефективність повторного введення через інтервали, що не перевищують 8 тижнів, не встановлені (див. Розділи 4.4 та 4.8).
Повторне введення при псоріазі
"Обмежений досвід лікування псоріазу в результаті повторного лікування одноразовою дозою Remicade через інтервал у 20 тижнів свідчить про" знижену ефективність та "більшу частоту легких до помірних інфузійних реакцій" порівняно з початковою схемою індукції. (Див. розділ 5.1).
"Обмежений досвід повторного лікування після погіршення захворювання за допомогою схеми повторної індукції свідчить про" високу частоту інфузійних реакцій, включаючи важкі, у порівнянні з тими, які проходять через 8 тижнів підтримуючого лікування (див. Параграф 4.8).
Повторне введення за різними показаннями
У разі припинення підтримуючої терапії та виникнення необхідності відновлення лікування застосування режиму повторної індукції не рекомендується (див. Розділ 4.8). У цій ситуації лікування препаратом Ремікейд слід розпочати одноразово, після чого підтримуюча доза відповідно до вищеописаних рекомендацій.
Пацієнти літнього віку (≥ 65 років)
Спеціальних досліджень з Remicade у пацієнтів літнього віку не проводилося. У клінічних дослідженнях не виявлено істотних вікових відмінностей у кліренсі або об’ємі розподілу.
Коригування дози не потрібне (див. Розділ 5.2). Для отримання додаткової інформації про безпеку Remicade для пацієнтів літнього віку див. Розділи 4.4 та 4.8.
Порушення функції нирок та / або печінки
Remicade не вивчався у цих популяціях пацієнтів. Не можна давати рекомендації щодо дози (див. Розділ 5.2).
Педіатричне населення
Хвороба Крона (6-17 років)
Доза 5 мг / кг, що вводиться шляхом внутрішньовенної інфузії, з подальшою інфузією у дозах 5 мг / кг через 2 та 6 тижнів після першої інфузії та кожні 8 тижнів після цього. Наявні дані не підтверджують подальше лікування інфліксимабом у дітей та підлітків, які не реагують протягом перших 10 тижнів лікування (див. Розділ 5.1).
Деяким пацієнтам може знадобитися коротший інтервал дозування для підтримки клінічної користі, тоді як для інших може бути достатнім більш тривалий інтервал між дозами. Пацієнти, у яких проміжок часу між дозами зменшився до менш ніж 8 тижнів, можуть мати підвищений ризик виникнення побічних реакцій. Продовження терапії зі скороченим інтервалом слід ретельно розглянути у тих пацієнтів, у яких немає доказів терапевтичної користі. проміжок часу між прийомами.
Безпека та ефективність препарату Ремікейд у дітей з хворобою Крона до 6 років не вивчалися. Наявні фармакокінетичні дані описані в розділі 5.2, але жодних рекомендацій щодо дозування не можна давати дітям віком до 6 років.
Виразковий коліт (6-17 років)
Доза 5 мг / кг, що вводиться шляхом внутрішньовенної інфузії, з подальшою інфузією у дозах 5 мг / кг через 2 та 6 тижнів після першої інфузії та кожні 8 тижнів після цього. Наявні дані не підтверджують подальшого лікування інфліксимабом у педіатричних пацієнтів, які не реагують протягом перших 8 тижнів лікування (див. Розділ 5.1).
Безпека та ефективність Remicade у дітей з виразковим колітом у віці до 6 років не вивчалися. Наявні фармакокінетичні дані описані в розділі 5.2, але жодних рекомендацій щодо дозування не можна давати дітям віком до 6 років.
Псоріаз
Безпека та ефективність препарату Ремікейд у дітей та підлітків віком до 18 років за показанням псоріаз не встановлені. Наразі наявні дані описані у розділі 5.2, але рекомендації щодо дозування не надаються.
Ювенільний ідіопатичний артрит, псоріатичний артрит та анкілозуючий спондиліт
Безпека та ефективність препарату Ремікейд у дітей та підлітків віком до 18 років за показаннями ювенільний ідіопатичний артрит, псоріатичний артрит та анкілозуючий спондиліт не встановлені. Наявні на даний момент дані описані у розділі 5.2, однак жодних рекомендацій щодо дозування зробити не можна.
Ювенільний ревматоїдний артрит
Безпека та ефективність препарату Ремікейд у дітей та підлітків віком до 18 років щодо ювенільного ревматоїдного артриту не встановлені. Наразі наявні дані описані у розділах 4.8 та 5.2, однак їх неможливо зробити. Рекомендації щодо дозування.
Порушення функції нирок та / або печінки
Remicade не вивчався у цих популяціях пацієнтів. Рекомендації щодо дози не надаються (див. Розділ 5.2).
Спосіб введення
Remicade слід вводити внутрішньовенно протягом 2 годин. Усі пацієнти, які отримують Ремікейд, повинні спостерігатися протягом щонайменше 1-2 годин після інфузії з метою виявлення гострих реакцій, пов’язаних з інфузією. Необхідно мати в наявності обладнання для екстреної допомоги, таке як адреналін, антигістамінні засоби, кортикостероїди та штучний респіратор. пов'язані реакції, особливо якщо реакції, пов'язані з інфузією, мали місце раніше (див. розділ 4.4).
Інфузії, скорочені за показаннями для дорослих
У ретельно відібраних дорослих пацієнтів, які перенесли щонайменше 3 початкові 2-годинні інфузії Remicade (фаза індукції) і які отримують підтримуючу терапію, введення наступних інфузій протягом не менше 1 години Якщо реакція інфузії, пов’язана із скороченням інфузії Якщо майбутні інфузії відбудуться, можна зменшити швидкість інфузії. Скорочені інфузії при дозах> 6 мг / кг не вивчалися (див. Розділ 4.8).
Інструкції щодо приготування та введення див. У розділі 6.6.
04.3 Протипоказання
Пацієнти з історією гіперчутливості до інфліксимабу (див. Розділ 4.8), до інших мишачих білків або до будь -якої з допоміжних речовин, перерахованих у розділі 6.1.
Пацієнти з туберкульозом або іншими серйозними інфекціями, такими як сепсис, абсцеси та умовно -патогенні інфекції (див. Розділ 4.4).
Пацієнти з помірною або важкою серцевою недостатністю (NYHA - Нью -Йоркська серцева асоціація - клас III / IV) (див. Розділи 4.4 та 4.8).
04.4 Спеціальні попередження та відповідні запобіжні заходи щодо використання
З метою покращення простежуваності біологічних лікарських засобів, товарний знак та номер партії введеного препарату повинні бути чітко записані (або позначені) у протоколі пацієнтів.
Реакції на інфузію та гіперчутливість
Інфліксимаб асоціювався з гострими реакціями, пов’язаними з інфузією, включаючи анафілактичний шок та реакції затримки гіперчутливості (див. Розділ 4.8).
Гострі реакції інфузії, включаючи анафілактичні, можуть виникнути протягом (протягом декількох секунд) або протягом кількох годин після інфузії. Якщо виникають гострі реакції на інфузію, інфузію слід негайно припинити. Необхідно мати в наявності обладнання для екстреної допомоги, таке як адреналін, антигістамінні препарати, кортикостероїди та штучний апарат штучної вентиляції легень.
Можуть розвинутися антитіла до інфліксимабу, які були пов’язані зі збільшенням частоти інфузійних реакцій. Низька швидкість інфузійних реакцій - важкі алергічні реакції. Також спостерігався зв’язок між виробленням антитіл до інфліксимабу та зниженням відповіді. Одночасний прийом імуномодуляторів був пов'язаний з меншою частотою антитіл до інфліксимабу та зменшенням частоти інфузійних реакцій. Ефект супутньої імуномодулюючої терапії був більш інтенсивним у пацієнтів з епізодичним лікуванням, ніж у пацієнтів, які отримували підтримуючу терапію. Пацієнти, які припинили імуносупресивну терапію до або під час лікування Ремікейдом, мають підвищений ризик розвитку цих антитіл. Антитіла до інфліксимабу не завжди можна виявити у зразках сироватки крові. Якщо виникають важкі реакції, слід призначити симптоматичне лікування та не вводити подальші інфузії препарату Ремікейд (див. Розділ 4.8.).
У клінічних дослідженнях повідомлялося про уповільнені реакції гіперчутливості. Наявні дані свідчать про підвищений ризик затримки гіперчутливості до збільшення тривалості інтервалів без застосування Ремікейду. Пацієнтам слід порадити негайно звернутися до лікаря у разі затримки побічної дії (див. Розділ 4.8). період, їх слід уважно стежити за ознаками та симптомами уповільненої гіперчутливості.
Інфекції
Перед, під час та після лікування препаратом Ремікейд пацієнти повинні перебувати під ретельним наглядом на наявність інфекцій, включаючи туберкульоз. Оскільки елімінація інфліксимабу може тривати до шести місяців, протягом цього періоду слід продовжувати моніторинг. Подальше лікування препаратом Ремікейд не слід проводити, якщо у пацієнта розвиваються важкі інфекції або сепсис.
Необхідна обережність при застосуванні Ремікейд пацієнтам з хронічною інфекцією або рецидивуючими інфекціями в анамнезі, включаючи супутню терапію імунодепресантами.Пацієнтів слід належним чином поінформувати про необхідність уникати впливу потенційних факторів ризику інфекцій.
Фактор некрозу пухлин альфа (TNFα) опосередковує запалення та модулює клітинну імунну відповідь. Експериментальні дані показують, що TNFα має важливе значення для вирішення внутрішньоклітинних інфекцій. Клінічний досвід показує, що імунна захист господаря порушується у деяких пацієнтів, які отримують інфліксимаб.
Слід зазначити, що пригнічення TNFα може маскувати симптоми такої інфекції, як гарячка. Раннє розпізнавання атипових клінічних проявів важких інфекцій та типових клінічних проявів рідкісних та незвичайних інфекцій має вирішальне значення для мінімізації затримок у діагностиці та лікуванні.
Пацієнти, які приймають препарати, що блокують ФНВ, більш схильні до серйозних інфекцій.
Туберкульоз, бактеріальні інфекції, включаючи сепсис та пневмонію, інвазивні грибкові, вірусні та інші умовно -патогенні інфекції спостерігалися у пацієнтів, які отримували інфліксимаб. Деякі з цих інфекцій мали летальний результат; найбільш часто повідомляються опортуністичні інфекції зі смертністю> 5% включають пенумоцистоз, кандидоз, лістеріоз та аспергільоз.
Пацієнти, у яких під час лікування препаратом Ремікейд з’являється нова інфекція, повинні бути ретельно обстежені та пройти ретельну діагностичну оцінку. Прийом препарату Ремікейд слід припинити, якщо у пацієнта з’явилася нова серйозна інфекція або сепсис, і розпочати відповідну протимікробну або протигрибкову терапію до повного усунення інфекції.
Туберкульоз
Повідомлялося про випадки активного туберкульозу у пацієнтів, які отримували Ремікейд. Слід зазначити, що в більшості цих випадків це був позалегеневий туберкульоз, як локалізований, так і дифузний.
Перед початком лікування препаратом Ремікейд слід обстежити всіх пацієнтів на наявність активного та неактивного («прихованого») туберкульозу.Ця оцінка повинна включати детальну історію хвороби, включаючи особисту історію туберкульозу або можливий попередній контакт з джерелом туберкульозної інфекції та попередню та / або супутню імуносупресивну терапію. Усім пацієнтам слід провести відповідні діагностичні тести, такі як туберкулінова шкірна проба та рентгенографія грудної клітки (можуть застосовуватися місцеві рекомендації). Рекомендується повідомляти про ці тести у картці оповіщення пацієнта. Рецепторам нагадується про ризик хибнонегативних результатів шкірного тесту на туберкулін, особливо у важкохворих або пацієнтів з ослабленим імунітетом.
Якщо діагностовано активний туберкульоз, терапію Remicade не слід розпочинати. (див. розділ 4.3)
При підозрі на прихований туберкульоз слід звернутися до лікаря з досвідом лікування туберкульозу. У всіх ситуаціях, описаних нижче, слід ретельно зважити співвідношення користь / ризик терапії препаратом Ремікейд.
Якщо діагностовано неактивний («латентний») туберкульоз, перед початком терапії препаратом Ремікейд відповідно до місцевих рекомендацій слід розпочати протитуберкульозну терапію прихованого туберкульозу.
У пацієнтів, які мають багато чи значні фактори ризику розвитку туберкульозу та мають негативний тест на прихований туберкульоз, перед початком лікування Ремікейдом слід розглянути можливість протитуберкульозної терапії.
Перед застосуванням препарату Ремікейд також слід розглянути можливість застосування протитуберкульозної терапії у пацієнтів з анамнезом латентного або активного туберкульозу в анамнезі, для яких адекватний курс лікування не може бути підтверджений.
Повідомлялося про деякі випадки активного туберкульозу у пацієнтів, які отримували Ремікейд під час та після лікування прихованого туберкульозу.
Всім пацієнтам слід порадити звернутися до лікаря, якщо під час або після лікування препаратом Ремікейд з’являються ознаки / симптоми, що свідчать про туберкульоз (наприклад, постійний кашель, виснаження / втрата ваги, субфебрильна температура).
Інвазивні грибкові інфекції
Інвазивну грибкову інфекцію, таку як аспергільоз, кандидоз, пневмоцистоз, гістоплазмоз, кокцидіоїдомікоз або бластомікоз, слід запідозрити у пацієнтів, які отримують Ремікейд, якщо у них розвинеться важке системне захворювання, і на ранній стадії слід звернутися до лікаря, компетентного у діагностиці та лікуванні інвазивних грибкових інфекцій при відвідуванні цих пацієнтів. Інвазивні грибкові інфекції можуть проявлятися як розповсюджене, а не локалізоване захворювання, а у деяких пацієнтів з активною інфекцією аналізи на антиген та антитіла можуть бути негативними. У процесі діагностики слід враховувати відповідну емпіричну протигрибкову терапію, враховуючи як ризик важкої грибкової інфекції, так і ризик протигрибкової терапії.
Для пацієнтів, які проживали в регіонах, де є інвазивні грибкові інфекції, такі як гістоплазмоз, кокцидіоїдомікоз або бластомікоз, є ендемічними, перед початком терапії препаратом слід ретельно зважити переваги та ризики лікування препаратом Ремікейд.
Свищева хвороба Крона
Пацієнтам з фістулізуючою хворобою Крона з гострими гнійними свищами не слід розпочинати терапію препаратом Ремікейд, доки не буде виключено джерело можливої інфекції, зокрема абсцеси (див. Розділ 4.3).
Реактивація гепатиту В (ВГВ)
Реактивація гепатиту В спостерігалася у пацієнтів, які отримували антагоніст ФНП, включаючи інфліксимаб, і які були хронічними носіями цього вірусу. У деяких випадках наступали летальні наслідки.
Пацієнтів слід обстежити на наявність інфекції ВГВ перед початком лікування препаратом Ремікейд. Пацієнтам, у яких позитивний тест на ВГВ, рекомендується проконсультуватися з лікарем, який має досвід лікування гепатиту В.
Носії ВГВ, яким потрібне лікування Ремікейдом, слід ретельно контролювати на наявність ознак та симптомів активної інфекції ВГВ протягом усього періоду терапії та протягом кількох місяців після закінчення терапії. Недостатньо даних про пацієнтів з ВГВ, які отримували противірусну терапію у комбінації з антагоністом ФНО. терапія для запобігання реактивації HBV У пацієнтів, у яких розвивається реактивація HBV, лікування Remicade слід припинити та розпочати ефективну противірусну терапію з відповідним підтримуючим лікуванням.
Гепатобіліарні події
Під час маркетингового періоду Remicade спостерігалися дуже рідкісні випадки жовтяниці та неінфекційного гепатиту, деякі з яких мали ознаки аутоімунного гепатиту. Були поодинокі випадки печінкової недостатності, що призвела до трансплантації печінки або смерті. У пацієнтів з ознаками та симптомами порушення функції печінки слід оцінити рівень ураження печінки. Якщо жовтяниця та / або підвищення рівня АЛТ ≥ 5 разів перевищує верхню межу норми, лікування Ремікейдом слід припинити та провести ретельне обстеження аномальних станів.
Асоціація інгібітора TNF-альфа та анакінри
Серйозні інфекції та нейтропенія мали місце у комбінованих клінічних випробуваннях анакінри та іншого інгібітора TNFα без додаткових клінічних переваг у порівнянні із застосуванням лише етанерцепту. комбінація анакінри та інших інгібіторів ФНП α. Тому комбінація Ремікаде та анакінри не рекомендується.
Асоціація інгібітора TNF-альфа та абатацепту
У клінічних дослідженнях комбіноване застосування антагоністів ФНП та абатасепту асоціювалося з підвищеним ризиком інфекцій, включаючи серйозні інфекції, порівняно з антагоністами ФНП, що застосовувалися окремо, без збільшення клінічної користі. Ремікаде та абатацепт не рекомендуються.
Асоціація з іншими біологічними методами лікування
Інформації про одночасне застосування інфліксимабу з іншими біологічними препаратами, що застосовуються для лікування тих самих станів, що і інфліксимаб, недостатньо. Одночасне застосування інфліксимабу з цими біопрепаратами не рекомендується через можливість підвищеного ризику інфекції та інших потенційних лікарських взаємодій.
Заміна між біологічними DMARD
Слід бути обережним, а пацієнтів слід продовжувати контролювати при переході з одного препарату на інший, оскільки перекриття біологічної активності може ще більше збільшити ризик побічних явищ, включаючи інфекцію.
Живі вакцини / інфекційні терапевтичні засоби
У пацієнтів, які отримують анти-TNF-терапію, є обмежені дані про відповідь на вакцинацію живими вакцинами або про вторинну передачу інфекції при введенні живих вакцин. . Не рекомендується одночасне введення живих вакцин з препаратом Ремікейд.
У немовлят, які зазнали внутрішньоутробного впливу інфліксимабу, повідомлялося про смертельний результат, спричинений дисемінованою інфекцією палички Кальмета-Герена (БЦЖ) після введення вакцини БЦЖ після народження. Перед введенням живих вакцин немовлятам, які піддаються впливу внутрішньоутробно для інфліксимабу рекомендується період очікування не менше шести місяців після народження (див. розділ 4.6).
Інше використання інфекційних терапевтичних засобів, таких як живі аттенуйовані бактерії (наприклад, внутрішньоміхурові інстиляції БЦЖ для лікування раку), може призвести до клінічних інфекцій, включаючи дисеміновані інфекції. Рекомендується не давати терапевтичні інфекційні агенти одночасно з Ремікейдом.
Аутоімунні реакції
Відносний дефіцит TNFα, викликаний анти-TNF-терапією, може призвести до початку аутоімунного процесу. Якщо у пацієнта після лікування препаратом Ремікейд є симптоми, що передбачають вовчакоподібний синдром, і позитивний для анти-ДНК-антитіл до подвійної спіралі, немає слід проводити подальше лікування препаратом Ремікейд (див. розділ 4.8).
Вплив на нервову систему
Застосування блокаторів ФНВ, включаючи інфліксимаб, асоціювалося з початком або загостренням клінічних симптомів та / або рентгенографічних ознак демієлінізуючих розладів центральної нервової системи, включаючи розсіяний склероз, та периферичних демієлінізуючих розладів, включаючи синдром Гійєна-Барре. при наявних або нещодавніх демієлінізуючих розладах слід ретельно розглянути переваги та ризики лікування анти-ФНП перед початком терапії препаратом Ремікейд.
У разі розвитку цих станів слід розглянути можливість припинення терапії препаратом Ремікейд.
Злоякісні новоутворення та лімфопроліферативні захворювання
На контрольованих фазах клінічних випробувань з інгібіторами ФНП спостерігалося більше випадків злоякісних пухлин, включаючи лімфому, серед пацієнтів, які отримували інгібітор ФНП, ніж у контрольних пацієнтів. Під час клінічних досліджень з Remicade, за всіма затвердженими показаннями, частота лімфом у пацієнтів, які отримували Remicade, була вищою, ніж очікувалося, у загальній популяції, але частота лімфоми була рідкісною. пацієнти, які отримували антагоніст TNF. Існує підвищений фоновий ризик розвитку лімфоми та лейкемії у пацієнтів з ревматоїдним артритом з дуже активним і тривалим запальним захворюванням, що ускладнює оцінку ризику.
У дослідницькому клінічному дослідженні, в якому оцінювалося застосування препарату Ремікейд у пацієнтів з помірною та важкою хронічною обструктивною хворобою легень (Хронічне обструктивне захворювання легень(ХОЗЛ), у пацієнтів, які отримували Ремікейд, було зареєстровано більше випадків злоякісних пухлин, ніж у контрольних пацієнтів. Усі пацієнти були завзятими курцями. Слід з обережністю оцінювати лікування пацієнтів з підвищеним ризиком злоякісних пухлин як завзятих курців.
Виходячи з сучасних знань, не можна виключити ризик розвитку лімфом або злоякісних пухлин у пацієнтів, які отримують інгібітор ФНП (див. Розділ 4.8). Слід бути обережним при розгляді терапії інгібіторами ФНП у пацієнтів із злоякісними новоутвореннями в анамнезі або при розгляді тривалого лікування у пацієнтів, у яких розвивається злоякісне новоутворення.
Слід також бути обережними у пацієнтів з псоріазом, які раніше отримували інтенсивне лікування імунодепресантами або протягом тривалого періоду з ПУВА.
У постмаркетинговому досвіді повідомлялося про злоякісні пухлини, деякі з яких смертельні, серед дітей, підлітків та молодих людей (до 22 років), які отримували препарати, що блокують ФНП (початок терапії ≤ 18 років), включаючи Remicade. Приблизно. половина випадків - це лімфоми, інші - різні злоякісні новоутворення і включали рідкісні злоякісні утворення, зазвичай пов'язані з імуносупресією. Не можна виключити ризик розвитку злоякісних новоутворень у пацієнтів, які отримують інгібітори ФНП.
Постмаркетингові рідкісні випадки гепатоспленочної Т-клітинної лімфоми (HSTCL) були зареєстровані у пацієнтів, які отримували блокатори ФНО, включаючи інфліксимаб. Ця рідкісна форма Т-клітинної лімфоми має надзвичайно агресивний перебіг та результат. Як правило, з летальним результатом. Майже всі пацієнти отримували лікування АЗА або 6-МП одночасно з блокатором ФНП або безпосередньо перед ним. Переважна більшість випадків з Ремікейдом траплялася у пацієнтів з хворобою Крона або виразковим колітом, а більшість випадків були зареєстровані у підлітків або молодих дорослих чоловіків. потенційний ризик комбінації AZA або 6-MP та Remicade необхідно ретельно розглянути. Не можна виключити ризик розвитку гепатоспленочної Т-клітинної лімфоми у пацієнтів, які отримують Ремікейд (див. Розділ 4.8).
Повідомлялося про меланому та клітинний рак Меркель у пацієнтів, які отримували терапію блокатором TNF, включаючи Remicade (див. Розділ 4.8). Рекомендується періодичний огляд шкіри, особливо пацієнтам з факторами ризику раку шкіри.
Ретроспективне когортне дослідження, засноване на даних з національних реєстрів охорони здоров’я Швеції, виявило підвищену захворюваність на рак шийки матки у жінок з ревматоїдним артритом, які отримували лікування інфліксимабом, порівняно з біологічно нелікованими пацієнтами чи загальною популяцією, включаючи осіб старше 60 років Періодичний скринінг слід проводити у жінок отримували лікування препаратом Ремікейд, включаючи осіб старше 60 років.
Усі пацієнти з виразковим колітом, які мають підвищений ризик розвитку дисплазії або карциноми товстої кишки (наприклад, пацієнти з тривалим виразковим колітом або первинним склерозуючим холангітом) або мають анамнез дисплазії або раку товстої кишки. до цієї дисплазії через регулярні проміжки часу, перед початком терапії та протягом хвороби. Ця оцінка повинна включати колоноскопію та біопсію відповідно до місцевих рекомендацій. З огляду на поточні дані, невідомо, чи впливає лікування інфліксимабом на ризик розвитку дисплазії або раку товстої кишки (див. Розділ 4.8).
Оскільки можливість підвищеного ризику розвитку раку у пацієнтів, які отримували Ремікейд із вперше виявленою дисплазією, не встановлена, необхідно оцінити співвідношення користь / ризик для окремих пацієнтів та розглянути можливість припинення терапії.
Серцева недостатність
Ремікад слід з обережністю застосовувати пацієнтам з легкою серцевою недостатністю (клас I / II NYHA).За пацієнтами слід проводити ретельний моніторинг, а лікування пацієнтами, які мають нові або погіршуються симптоми серцевої недостатності, слід припинити (див. Розділи 4.3 та 4.8).
Гематологічні реакції
Повідомлялося про випадки панцитопенії, лейкопенії, нейтропенії та тромбоцитопенії у пацієнтів, які отримували препарати проти ФНП, включаючи Ремікейд. Всім пацієнтам слід порадити негайно звернутися за медичною допомогою, якщо у них з’являться сумісні ознаки або симптоми порушення крові (наприклад, стійка лихоманка, синці, кровотеча та блідість). Пацієнтам з підтвердженими значними гематологічними відхиленнями слід розглянути питання про припинення терапії препаратом Ремікейд.
Інші
Досвід щодо безпеки лікування Remicade у пацієнтів, які перенесли операцію, включаючи ендопротезування, обмежений. Під час планування операції слід враховувати тривалий період напіввиведення інфліксимабу. Пацієнт, якому потрібна операція під час лікування препаратом Ремікейд, повинен ретельно контролюватися на предмет збільшення ризику інфекцій та розглянути відповідні заходи.
Відмова від лікування при хворобі Крона може свідчити про наявність жорстких фіброзних стриктур, які можуть потребувати хірургічного лікування. Немає клінічних даних, які б свідчили про те, що інфліксимаб погіршує або викликає фіброзні стриктури.
Особливі популяції
Пацієнти літнього віку (≥ 65 років)
Частота серйозних інфекцій у пацієнтів віком від 65 років і старше, які отримували Ремікейд, була вищою, ніж у пацієнтів віком до 65 років. Деякі з них були смертельними. Особливу увагу слід звернути на ризик зараження при лікуванні літніх людей (див. Розділ 4.8) .
Педіатричне населення
Інфекції
У клінічних дослідженнях у дітей частіше повідомлялося про інфекції, ніж у дорослих (див. Розділ 4.8).
Щеплення
Перед початком терапії препаратом Ремікейд педіатричним пацієнтам рекомендується, якщо це можливо, зробити всі щеплення відповідно до останніх рекомендацій.
Злоякісні новоутворення та лімфопроліферативні розлади
У постмаркетинговому досвіді повідомлялося про злоякісні пухлини, деякі з яких смертельні, серед дітей, підлітків та молодих людей (до 22 років), які отримували препарати, що блокують ФНП (початок терапії ≤ 18 років), включаючи Remicade. Приблизно. половина випадків - це лімфоми, інші - різні злоякісні новоутворення і включали рідкісні злоякісні утворення, зазвичай пов'язані з імуносупресією. Не можна виключити ризик розвитку злоякісних пухлин у дітей та підлітків, які отримують інгібітори ФНП.
У постмаркетинговому періоді повідомлялося про поодинокі випадки гепатоспленочної Т-клітинної лімфоми у пацієнтів, які отримували блокатори ФНО, включаючи інфліксимаб. Ця рідкісна форма Т-клітинної лімфоми має надзвичайно агресивний перебіг і, як правило, летальний результат. Майже всі пацієнти проходили лікування з АЗА або 6-МП одночасно з блокатором ФНП або безпосередньо перед ним. Переважна більшість випадків з Ремікейдом траплялася у пацієнтів з хворобою Крона або виразковим колітом, і більшість випадків повідомлялося у підлітків або молодих чоловіків. Потрібно ретельно продумати комбінацію AZA або 6-MP та Remicade. Не можна виключити ризик розвитку гепатоспленочної Т-клітинної лімфоми у пацієнтів, які отримують Ремікейд (див. Розділ 4.8).
04.5 Взаємодія з іншими лікарськими засобами та інші форми взаємодії
Досліджень взаємодії не проводилося.
Існують ознаки того, що одночасне застосування метотрексату та інших імуномодуляторів у пацієнтів з ревматоїдним артритом, псоріатичним артритом та хворобою Крона зменшує утворення антитіл проти інфліксимабу та збільшує концентрацію інфліксимабу у плазмі крові. Однак результати невизначені через обмеженість методів, що використовуються для аналізу інфліксимабу та антитіл до інфліксимабу в сироватці крові.
Схоже, що кортикостероїди не змінюють фармакокінетику інфліксимабу клінічно значущим чином.
Поєднання препарату Ремікейд з іншими біологічними препаратами, що застосовуються для лікування тих самих станів, що і Ремікейд, включаючи анакінру та абатацепт, не рекомендується (див. Розділ 4.4).
Рекомендується не вводити живі вакцини одночасно з Remicade. Також рекомендується не вводити немовлятам живі вакцини після контакту внутрішньоутробно до інфліксимабу протягом щонайменше 6 місяців після народження (див. розділ 4.4).
Інфекційні терапевтичні засоби не слід вводити одночасно з Remicade (див. Розділ 4.4).
04.6 Вагітність та лактація
Жінки дітородного віку
Жінки репродуктивного віку повинні використовувати адекватну контрацепцію під час лікування препаратом Ремікейд і продовжувати її застосування щонайменше 6 місяців після останньої дози.
Вагітність
Помірна кількість проспективно зібраних даних про вагітних пацієнтів (приблизно 450), які отримували інфліксимаб з відомими наслідками, включаючи обмежену кількість (приблизно 230) вагітностей, які проходили лікування у першому триместрі, не виявила несподіваних наслідків для результату. Через інгібування ФНП? інфліксимаб, призначений під час вагітності, може змінити нормальну імунну відповідь новонародженого. Ні токсичності для матері, ні ембріотоксичності, ні тератогенності не було виявлено у дослідженні токсичності розвитку мишей з використанням подібного антитіла, яке вибірково пригнічує функціональність ФНП (див. Розділ 5.3).
Наявний клінічний досвід надто обмежений, щоб виключити ризики, тому введення інфліксимабу не рекомендується під час вагітності.
Інфліксимаб проходить через плаценту і був виявлений у сироватці крові немовлят протягом 6 місяців після народження. Після експозиції внутрішньоутробно щодо інфліксимабу немовлята можуть мати більш високий ризик зараження, включаючи "важку розповсюджену інфекцію, яка може мати летальний результат. Введення живих вакцин (наприклад, вакцини БЦЖ) немовлятам, які піддаються впливу". внутрішньоутробно не рекомендується інфліксимаб щонайменше через 6 місяців після народження (див. розділи 4.4 та 4.5). Також повідомлялося про випадки агранулоцитозу (див. Розділ 4.8).
Час годування
Невідомо, чи інфліксимаб виділяється з грудним молоком або системно всмоктується після прийому. Оскільки імуноглобуліни людини виділяються у грудне молоко, жінки не повинні годувати грудьми щонайменше 6 місяців після лікування Ремікейдом.
Родючість
Недостатньо доклінічних даних, щоб зробити висновки про вплив інфліксимабу на фертильність та загальну репродуктивну функцію (див. Розділ 5.3).
04.7 Вплив на здатність керувати автомобілем та працювати з механізмами
Remicade має незначний вплив на здатність керувати автомобілем або працювати з механізмами. Після введення Ремікейду може виникнути запаморочення (див. Розділ 4.8).
04.8 Побічні ефекти
Короткий опис профілю безпеки
Інфекція верхніх дихальних шляхів була найпоширенішою побічною реакцією, про яку повідомлялося у клінічних випробуваннях, і зустрічалася у 25,3% пацієнтів, які отримували інфліксимаб, у порівнянні з 16,5% контрольних пацієнтів. "Застосування інгібіторів ФНВ, про які повідомлялося для Remicade, включає реактивацію ВГВ, застійну серцеву недостатність ( ХСН), важкі інфекції (включаючи сепсис, умовно-патогенні інфекції та туберкульоз), сироваткова хвороба (затримка реакцій гіперчутливості), гематологічні реакції, системний червоний вовчак / вовчакоподібний синдром, демієлінізуюча хвороба, гепатобіліарні події, лімфома, HSTCL, лейкемія, клітина карциноми Меркеля , меланома, злоякісне новоутворення у дітей, саркоїдоз / реакція типу саркоїду, кишковий або перианальний абсцес (при хворобі Крона) та важкі реакції на інфузію (див. розділ 4.4).
Таблиця побічних реакцій
У таблиці 1 перераховані небажані реакції, про які повідомлялося у клінічних випробуваннях, а також побічні реакції, деякі з летальним результатом, про які повідомлялося у постмаркетинговому періоді. У системі системних органів побічні реакції перераховані за частотою, використовуючи такі категорії: дуже часто (≥ 1/10); часто (≥ 1/100 до
Таблиця 1
Побічні ефекти під час клінічних випробувань та після маркетингу
* включаючи туберкульоз великої рогатої худоби (дисеміновану інфекцію БЦЖ), див. розділ 4.4
Реакції, пов’язані з інфузією
У клінічних випробуваннях реакцію, пов’язану з інфузією, визначали як будь-яку побічну подію, що відбулася під час інфузії або протягом 1 години після інфузії. реакція, пов’язана з інфузією.В цілому більша кількість пацієнтів, які отримували монотерапію інфліксимабом, зазнали реакції, пов’язані з інфузією, ніж пацієнти, які одночасно отримували інфліксимаб з імуномодуляторами. Приблизно 3% пацієнтів припинили лікування через реакції, пов’язані з інфузією, і всі пацієнти одужали з медикаментозною терапією або без неї.
З пацієнтів, які отримували інфліксимаб, які мали інфузійну реакцію протягом індукційного періоду до 6 тижня, 27% зазнали інфузійну реакцію протягом періоду підтримки між 7 тижнем та 54 тижнем. 9% зазнали інфузійну реакцію протягом періоду підтримки.
У клінічному дослідженні у пацієнтів з ревматоїдним артритом (ASPIRE) інфузії вводили протягом 2 годин протягом перших 3 інфузій. Тривалість наступних інфузій можна скоротити не менше ніж до 40 хвилин у пацієнтів, які не відчували жодних реакцій. настій. У цьому дослідженні шістдесят шість відсотків пацієнтів (686 з 1040) отримували принаймні одну скорочену інфузію тривалістю 90 хвилин або менше, а 44% пацієнтів (454 з 1040) отримували принаймні одну скорочену інфузію тривалістю 60 хвилин або менше. У пацієнтів, які отримували інфліксимаб, які отримували принаймні одну скорочену інфузію, реакції, пов’язані з інфузією, виникали у 15% пацієнтів, а тяжкі інфузійні реакції-у 0,4% пацієнтів.
У клінічному дослідженні у пацієнтів з хворобою Крона (SONIC) реакції, пов'язані з інфузією, спостерігалися у 16,6% (27/163) пацієнтів, які отримували монотерапію інфліксимабом, у 5% (9/179) пацієнтів, які отримували монотерапію інфліксимабом. у комбінації з AZA та у 5,6% (9/161) пацієнтів, які отримували монотерапію AZA. Важка інфузійна реакція (
У постмаркетинговий період випадки анафілактоїдних реакцій, включаючи набряк гортані / глотки, сильний бронхоспазм та судоми, були пов’язані з введенням препарату Ремікейд.
Крім того, були рідкісні повідомлення про тимчасову втрату зору та ішемію міокарда / інфаркт міокарда, що виникали під час або протягом двох годин після інфузії препарату Ремікейд (див. Розділ 4.4).
Реакції на інфузію після повторного введення Remicade
Для оцінки ефективності та безпеки тривалої підтримуючої терапії було розроблено клінічне дослідження у пацієнтів з помірним та важким псоріазом у порівнянні з повторним лікуванням за схемою індукції Remicade (максимум чотири інфузії на 0, 2, 6 та 14 тижнях) після захворювання погіршення.Пацієнти не отримували супутньої імуносупресивної терапії. У групі повторного лікування у 4% (8/219) пацієнтів спостерігалися важкі інфузійні реакції щодо набряку обличчя та гіпотензії. У всіх випадках лікування Ремікейдом було припинено та / або прийнято інше лікування з повним усуненням ознак та симптомів.
Затримка гіперчутливості
У клінічних дослідженнях реакції гіперчутливості із затримкою були рідкісними і виникали після тимчасових інтервалів, що не перевищували 1 року. У дослідженнях псоріазу на початку лікування виникали затримки реакцій гіперчутливості. Ознаки та симптоми включали міалгію та / або артралгію з лихоманкою та / або висипом, при цьому у деяких пацієнтів спостерігався свербіж, набряк обличчя, рук або губ, дисфагія, кропив’янка, біль у горлі та головний біль.
Недостатньо даних про частоту реакцій гіперчутливості із затримкою після тимчасових інтервалів, що не перевищують 1 року, але обмежені дані клінічних досліджень свідчать про підвищений ризик затримки гіперчутливості до збільшення тривалості інтервалів часу без застосування Ремікейду. (див. розділ 4.4).
У 1-річному клінічному дослідженні з повторними інфузіями у пацієнтів з хворобою Крона (дослідження ACCENT I) частота реакцій, що виникли внаслідок розвитку реакцій, подібних до сироваткової хвороби, склала 2,4%.
Імуногенність
Пацієнти, у яких виробилися антитіла до інфліксимабу, частіше відчували реакції, пов’язані з інфузією (приблизно у 2–3 рази вище). Одночасне застосування імуносупресивних засобів зменшило частоту реакцій, пов’язаних із інфузією.
У клінічних дослідженнях, в яких одноразово або багаторазово вводили інфліксимаб у діапазоні від 1 до 20 мг / кг, антитіла до інфліксимабу були виявлені у 14% пацієнтів, які отримували будь -яку імуносупресивну терапію, та у 24% пацієнтів, які не отримували імуносупресивної терапії. 8% пацієнтів з ревматоїдним артритом, які неодноразово отримували рекомендовану дозу і метотрексат, виробили антитіла до інфліксимабу. і 26% пацієнтів, які не отримували метотрексат на початковому етапі) .У пацієнтів з хворобою Крона, які отримували підтримуюче лікування, в середньому 3,3% пацієнтів, які отримували імунодепресанти, і 13,3% пацієнтів, які не отримували імунодепресантів, виробили антитіла проти інфліксимабу. Частота антитіл становила 2-3 разів вище для пацієнтів, які отримують епізодичне лікування. Через методологічні обмеження негативний тест не виключав наявності антитіл до інфліксимабу. Деякі пацієнти, у яких виявили високі титри антитіл до інфліксимабу, знижували ефективність. У пацієнтів з псоріазом, які отримували режим підтримки інфліксимабу, за відсутності супутнього лікування імуномодуляторами приблизно у 28% вироблялися антитіла до інфліксимабу (див. Розділ 4.4: «Реакції на інфузію та гіперчутливість»).
Інфекції
У пацієнтів, які отримували Ремікейд, спостерігалися туберкульоз, бактеріальні інфекції, включаючи сепсис та пневмонію, інвазивні грибкові, вірусні та інші умовно -патогенні інфекції. Деякі з них були смертельними. Найчастіше повідомляються про опортуністичні інфекції зі смертністю> 5%: пневмоцистоз, кандидоз, лістеріоз та аспергільоз (див. Розділ 4.4).
У клінічних дослідженнях 36% пацієнтів, які отримували інфліксимаб, лікувалися від інфекцій, у порівнянні з 25% пацієнтів, які отримували плацебо.
У клінічних випробуваннях ревматоїдного артриту частота серйозних інфекцій, включаючи пневмонію, була вищою у пацієнтів, які отримували інфліксимаб та метотрексат, ніж у пацієнтів, які отримували тільки метотрексат, особливо у дозах 6 мг / кг або вище (див. Розділ 4.4).
Серед спонтанних повідомлень, повідомлених у постмаркетинговий період, інфекції є найпоширенішою серйозною побічною подією. Деякі випадки мали летальний результат. Майже 50% зареєстрованих смертей були пов'язані з інфекцією. Повідомлялося про випадки туберкульозу., іноді з летальним результатом, включаючи випадки міліарного туберкульозу та туберкульозу позалегеневої локалізації (див. розділ 4.4).
Злоякісні новоутворення та лімфопроліферативні захворювання
У клінічних випробуваннях, проведених з інфліксимабом, в яких було проліковано 5780 пацієнтів, що становить 5494 пацієнтно-років, було виявлено 5 випадків лімфом та 26 випадків злоякісних пухлин нелімфом, порівняно з жодним випадком лімфоми та 1 випадком злоякісності нелімфоми. спостерігалося у 1600 пацієнтів, які отримували плацебо, що становить 941 пацієнт-рік.
У довгострокових випробуваннях безпеки до 5 років з застосуванням інфліксимабу, що становить 6 234 пацієнт-роки (3210 пацієнтів), було зареєстровано 5 випадків лімфоми та 38 випадків злоякісних пухлин нелімфом.
У постмаркетинговий період також повідомлялося про випадки злоякісних пухлин, включаючи лімфому (див. Розділ 4.4).
У дослідницькому клінічному дослідженні, в якому брали участь пацієнти з помірною та важкою формою ХОЗЛ, які були або курцями, або колишніми курцями, 157 дорослих пацієнтів лікувалися препаратом Ремікейд у таких же дозах, що і при ревматоїдному артриті та хворобі Крона. У дев’яти з цих пацієнтів розвинулися злоякісні пухлини, у тому числі 1 лімфома. Середня тривалість спостереження становила 0,8 року (частота 5,7% [95% ДІ 2,65%-10,6%]. Один із випадків злоякісного новоутворення був зареєстрований серед 77 пацієнтів у контролі (середня тривалість спостереження 0,8 року; частота) 1,3% [95% ДІ 0,03% - 7,0%]). Більшість із цих злоякісних пухлин вражали легені, голову або шию.
Ретроспективне когортне дослідження, проведене на основі популяції, виявило підвищену захворюваність на рак шийки матки у жінок з ревматоїдним артритом, які отримували лікування інфліксимабом, порівняно з пацієнтами, які не отримували біологічну терапію, або загальною популяцією, включаючи пацієнтів старше 60 років (див. Розділ 4.4).
Крім того, у постмаркетинговому періоді повідомлялося про поодинокі випадки гепатоспленочної Т-клітинної лімфоми у пацієнтів, які отримували Ремікейд, переважна більшість випадків були у пацієнтів з хворобою Крона та виразковим колітом, більшість пацієнтів були підлітками або молодими чоловіками (див. Розділ 4.4. ).
Серцева недостатність
У дослідженні ІІ фази, метою якого було оцінити Remicade при застійній серцевій недостатності (ХСН), була виявлена вища частота смертності через погіршення серцевої недостатності у пацієнтів, які отримували Ремікейд, особливо у пацієнтів, які отримували найвищу дозу 10 мг / кг (тобто подвоєння максимальної дозволеної дози). У цьому дослідженні 150 пацієнтів з ХСН класу III та IV за NYHA (фракція викиду лівого шлуночка ≤ 35%) отримували 3 інфузії препарату Ремікейд 5 мг / кг, 10 мг / кг або плацебо протягом 6 тижнів. На 38 тижні 9 із 101 пацієнта, які отримували Ремікейд (від 2 до 5 мг / кг і від 7 до 10 мг / кг), померли, тоді як серед 49 пацієнтів, які отримували плацебо, була одна смерть.
Під час постмаркетингового періоду у пацієнтів, які отримували Ремікейд, повідомлялося про випадки погіршення серцевої недостатності з ідентифікованими тригерами та без них. Протягом постмаркетингового періоду також повідомлялося про нову серцеву недостатність, включаючи серцеву недостатність. немає відомих наявних серцево-судинних захворювань Деякі з цих пацієнтів були віком до 50 років.
Гепатобіліарні події
У клінічних дослідженнях спостерігалося легке або помірне підвищення рівня АЛТ та АСТ у пацієнтів, які отримували Ремікейд без прогресування до тяжкого ураження печінки. Спостерігалося підвищення АЛТ ≥ 5 разів вище нормальних меж (ULN) (див. Таблицю 2). Підвищення рівня амінотрансферази (частіше при АЛТ, ніж АСТ) спостерігалося у більшої частки пацієнтів, які отримували Ремікейд, ніж у контрольних групах, як при одночасному прийомі Ремікейду, так і при комбінації з іншими імуносупресивними препаратами. Більшість аномалій амінотрансферази були тимчасовими; однак тривале збільшення спостерігалося у невеликої кількості пацієнтів. Загалом, пацієнти, у яких спостерігалося підвищення рівня АЛТ та АСТ, були безсимптомними, а відхилення зменшувалися або усувалися або шляхом продовження, або припинення лікування препаратом Ремікейд, або шляхом зміни супутньої терапії. Дуже рідкісні випадки жовтяниці та гепатиту, деякі з ознаками аутоімунного гепатиту, були зареєстровані у пацієнтів, які отримували Ремікейд у період постмаркетингового спостереження (див. Розділ 4.4).
Таблиця 2
Кількість пацієнтів з підвищеною активністю АЛТ у клінічних випробуваннях
1 Пацієнти у групі плацебо отримували метотрексат, тоді як пацієнти у групі інфліксимабу отримували як інфліксимаб, так і метотрексат.
2 Пацієнти у групі плацебо у 2 -х дослідженнях фази III хвороби Крона, ACCENT I та ACCENT II, отримували початкову дозу 5 мг / кг інфліксимабу на початку дослідження та плацебо на етапі підтримки. а згодом перейшли на інфліксимаб, вони були включені до групи інфліксимабу в аналізі АЛТ. У дослідженні фази IIIb при хворобі Крона, SONIC, пацієнти у групі плацебо отримували AZA 2,5 мг / кг / день як активний контроль, на додаток до інфузій плацебо інфліксимабу.
3 Кількість пацієнтів, обстежених на АЛТ.
4 Середнє спостереження базується на лікуванні пацієнтів.
Антиядерні антитіла (ANA) / дволанцюгові антитіла до ДНК (dsDNA)
Приблизно половина пацієнтів, які отримували інфліксимаб у клінічних випробуваннях, у яких вихідний аналіз був негативним по АНА, під час дослідження стали АНА-позитивними порівняно з приблизно однією п'ятою пацієнтів, які отримували плацебо. Нещодавно антитіла до dsDNA були виявлені приблизно у 17% пацієнтів, які отримували інфліксимаб, порівняно з 0% пацієнтів, які отримували плацебо. За останньою оцінкою, 57% пацієнтів, які отримували інфліксимаб, залишалися позитивними щодо антитіл до dsDNA. Однак повідомлення про подібний вовчак та вовчаковий синдроми залишаються рідкісними (див. Розділ 4.4).
Педіатричне населення
Хворі на ювенільний ревматоїдний артрит
Remicade вивчали у клінічному дослідженні, в якому брали участь 120 пацієнтів (віковий діапазон: 4-17 років) з активним ювенільним ревматоїдним артритом незалежно від застосування метотрексату.Пацієнти отримували 3 або 6 мг / кг інфліксимабу у вигляді 3-дозової схеми індукції (тиждень 0, 2, 6 або тиждень 14,16, 20 відповідно) з подальшою підтримуючою терапією кожні 8 тижнів у поєднанні з метотрексатом.
Реакції на інфузію
Реакції на інфузію виникали у 35% пацієнтів з ювенільним ревматоїдним артритом, які отримували 3 мг / кг, у порівнянні з 17,5% пацієнтів, які отримували 6 мг / кг. можлива анафілактична реакція (2 з яких були включені до важких інфузійних реакцій). У групі 6 мг / кг у 2 з 57 пацієнтів спостерігалася важка інфузійна реакція. "інфузія, одна з яких мала можливу анафілактичну реакцію (див. ).
Імуногенність
38% пацієнтів, які отримували 3 мг / кг, виробили антитіла до інфліксимабу порівняно з 12% пацієнтів, які отримували 6 мг / кг. Титри антитіл були значно вищими у групі, яка отримувала 3 мг / кг, ніж у групі, яка отримувала 6 мг / кг.
Інфекції
Інфекції сталися у 68% (41/60) дітей, які отримували 3 мг / кг протягом 52 тижнів, у 65% (37/57) дітей, які отримували 6 мг / кг інфліксимабу протягом 38 тижнів, і у 47% (28 /60) дітей, які протягом 14 тижнів отримували плацебо (див. Розділ 4.4).
Дитячі пацієнти з хворобою Крона
Наступні небажані ефекти частіше повідомлялися у пацієнтів з хворобою Крона у дітей, включених до дослідження REACH (див. Розділ 5.1), ніж у дорослих пацієнтів з хворобою Крона: анемія (10,7%), кров у калі (9,7%), лейкопенія (8,7%), почервоніння шкіри з почервонінням шкіри (8,7%), вірусними інфекціями (7,8%), нейтропенією (6,8%), переломами кісток (6,8%), бактеріальними інфекціями (5,8%) та алергічними реакціями з ураженням дихальних шляхів (5,8%). Інші особливі міркування викладені нижче.
Реакції, пов’язані з інфузією
17,5% рандомізованих пацієнтів у дослідженні REACH зазнали 1 або більше інфузійних реакцій. Не повідомлялося про серйозні випадки інфузійних реакцій, а у 2 суб’єктів дослідження REACH розвивалися несерйозні анафілактичні реакції.
Імуногенність
Антитіла до інфліксимабу були виявлені у 3 (2,9%) педіатричних пацієнтів.
Інфекції
У дослідженні REACH повідомлялося про інфекції у 56,3% рандомізованих суб’єктів, які отримували інфліксимаб. Інфекції повідомлялися частіше у суб'єктів, яким вводили інфузії кожні 8 тижнів, ніж у осіб, які отримували лікування кожні 12 тижнів (73,6% та 38,0% відповідно), тоді як серйозні інфекції були зареєстровані у 3 суб'єктів у групі підтримуючого лікування кожні 8 тижнів та у 4 суб'єктів у оброблену групу кожні 12 тижнів. Найчастіше повідомлялося про інфекції верхніх дихальних шляхів та фарингіт. Абсцес був найпоширенішим із серйозних інфекцій. Повідомлялося про 3 випадки пневмонії (1 важка) та 2 випадки оперізувального герпесу (обидві несерйозні).
Дитячі пацієнти з виразковим колітом
В цілому, побічні реакції, про які повідомлялося у дослідженні у педіатричних пацієнтів з виразковим колітом (C0168T72), в цілому відповідали тим, що повідомлялися у дослідженнях у дорослих пацієнтів з виразковим колітом (ACT 1 та ACT 2). У дослідженні C0168T72 найбільш поширеними побічними реакціями були інфекції верхніх дихальних шляхів, фарингіт, біль у животі, лихоманка та головний біль. Найпоширенішою побічною подією було погіршення виразкового коліту, частота якого була вищою у пацієнтів, які отримували лікування кожні 12 тижнів, ніж у пацієнтів, які отримували лікування кожні 8 тижнів.
Реакції, пов’язані з інфузією
В цілому 8 (13,3%) із 60 пацієнтів, які отримували лікування, повідомили про одну або кілька інфузійних реакцій, причому 4 з 22 пацієнтів (18,2%) у кожній 8 -тижневій групі підтримки та 3 з 23 пацієнтів (13, 0%) у групі підтримуючої терапії кожні 12 тижнів Не повідомлялося про серйозні реакції на інфузію. Усі інфузійні реакції були легкими або помірними.
Імуногенність
Антитіла до інфліксимабу були виявлені у 4 (7,7%) пацієнтів до 54 тижня.
Інфекції
Інфекції були зареєстровані у 31 (51,7%) із 60 пацієнтів, які лікувалися у дослідженні C0168T72, а 22 (36,7%) потребували перорального або парентерального антимікробного лікування. Частка пацієнтів з інфекціями у дослідженні C0168T72 була подібна до такої у дослідженні дитячої хвороби Крона (REACH), але вища, ніж частка у дослідженнях виразкового коліту у дорослих (ACT 1 та ACT 2). Загальна частота інфекцій у дослідженні C0168T72 становила 13/22 (59%) у групі підтримуючої терапії кожні 8 тижнів та 14/23 (60,9%) у групі підтримуючої терапії кожні 12 тижнів. Верхніх дихальних шляхів (7/60 [12 %]) та фарингіт (5/60 [8%]) були найбільш поширеними інфекціями дихальної системи. Серйозні інфекції були зареєстровані у 12% (7/60) від усіх пролікованих пацієнтів.
У цьому дослідженні було більше пацієнтів у віковій групі від 12 до 17 років, ніж у віці від 6 до 11 років (45/60 [75,0%]) проти 15/60 [25,0%]). Незважаючи на те, що кількість пацієнтів у кожній підгрупі була занадто мала, щоб робити якісь чіткі висновки щодо "впливу віку на події, пов'язані з безпекою", була більша частка пацієнтів із серйозними побічними явищами та припиненням лікування, спричиненим подіями. молодша вікова група, ніж у старшій віковій групі. Хоча частка пацієнтів з інфекціями також була вищою у молодшій віковій групі, для важких інфекцій пропорції у двох групах були подібними. Загальна частка побічних явищ та реакцій на інфузію були подібне між віковими групами від 6 до 11 та від 12 до 17 років.
Постмаркетинговий досвід
Спонтанні постмаркетингові повідомлення про серйозні побічні реакції у педіатричних пацієнтів включали злоякісні пухлини, включаючи гепатоспленочну Т-клітинну лімфому, минущі порушення ферментів печінки, вовчакоподібні синдроми та позитивні аутоантитіла (див. Розділи 4.4 та 4.8).
Додаткова інформація про особливі групи населення
Пацієнти літнього віку (≥ 65 років)
У клінічних випробуваннях ревматоїдного артриту частота серйозних інфекцій була вищою у пацієнтів, які отримували інфліксимаб плюс метотрексат у віці 65 років і старше (11,3%), ніж у пацієнтів віком до 65 років (4, 6%). У пацієнтів, які отримували тільки метотрексат, частота серйозних інфекцій становила 5,2% у пацієнтів віком від 65 років і порівняно з 2,7% у пацієнтів віком до 65 років (див. Розділ 4.4).
Повідомлення про підозрювані побічні реакції
Повідомлення про підозрювані побічні реакції, які виникають після реєстрації лікарського засобу, є важливими, оскільки вони дозволяють постійно контролювати співвідношення користь / ризик лікарського засобу. , веб -сайт: www.agenziafarmaco.gov.it/it/responsabili.
04.9 Передозування
Випадків передозування не зафіксовано. Разові дози до максимум 20 мг / кг вводилися без токсичних ефектів.
05.0 ФАРМАКОЛОГІЧНІ ВЛАСТИВОСТІ
05.1 Фармакодинамічні властивості
Фармакотерапевтична група: інгібітори фактора некрозу пухлини альфа (TNF-альфа).
Код ATC: L04AB02.
Механізм дії
Інфліксимаб-це химерне, моноклональне антитіло людини-миші, яке з високою спорідненістю зв'язується як з розчинною, так і з трансмембранною формою TNFα, але не з лімфотоксином α (TNFβ).
Фармакодинамічні ефекти
Інфліксимаб пригнічує в пробірці Активність TNFα у широкому діапазоні біологічних доз. Інфліксимаб запобігав захворюванням у трансгенних мишей, які розвивали поліартрит як наслідок суттєвої експресії TNFα людини, і при введенні після початку захворювання він дозволяв регресувати суглобові ерозії. В природних умовах, інфліксимаб швидко утворює стабільні комплекси з TNFα людини, процес, який призводить до втрати біологічної активності TNFα.
Високі концентрації TNFα були виявлені в суглобах пацієнтів з ревматоїдним артритом і пов'язані з високою активністю захворювання. Лікування інфліксимабом призвело до зменшення інфільтрації запальних клітин у запалених ділянках суглобів та зменшення експресії при ревматоїдному артриті.молекули, що опосередковують адгезію клітин, хемотаксис та деградацію тканин. Після лікування інфліксимабом у пацієнтів спостерігався знижений рівень інтерлейкіну 6 (ІЛ-6) у сироватці крові та С-реактивного білка (СРБ) та підвищений рівень гемоглобіну у пацієнтів з РА зі зниженим рівнем гемоглобіну порівняно із значеннями до лікування. Крім того, лімфоцити периферичної крові не виявили значного зменшення кількості та проліферативної відповіді на тест в пробірці мітогенної стимуляції порівняно з клітинами нелікованих пацієнтів. У пацієнтів з псоріазом лікування інфліксимабом призвело до зменшення епідермального запалення та нормалізації диференціації кератиноцитів у псоріатичні бляшки.При псоріатичному артриті короткочасне лікування препаратом Ремікейд зменшило кількість Т-клітин та кровоносних судин. У синовіальній та псоріатичній шкірі.
Гістологічна оцінка біопсії товстої кишки, проведена до та через 4 тижні після введення інфліксимабу, показала значне зниження виявленого TNFα. Лікування інфліксимабом у пацієнтів з хворобою Крона також було пов'язане з істотним
зниження сироваткової концентрації CRP, зазвичай підвищеного маркера запалення. Загальна кількість периферичних лейкоцитів була мінімально позначена у пацієнтів, які отримували інфліксимаб, хоча зміни в лімфоцитах, моноцитах та нейтрофілах відображали зміни від нормальних значень. Мононуклеарні клітини периферичної крові (РВМК) пацієнтів, які отримували інфліксимаб, продемонстрували незмінену здатність проліферативної відповіді на подразники порівняно з пацієнтами, які не отримували лікування; Крім того, після лікування інфліксимабом не було помічено істотних змін у виробленні цитокінів стимульованими клітинами РВМС. Аналіз мононуклеарних клітин lamina propria, отриманий після біопсії слизової оболонки кишечника, показав, що лікування інфліксимабом призвело до зменшення кількості клітин, здатних експресувати TNFα та інтерферон γ. Подальші гістологічні дослідження надали докази того, що лікування інфліксимабом зменшує інфільтрацію запальних клітин у уражені ділянки кишечника та наявність маркерЕндоскопічні дослідження слизової оболонки кишечника показали загоєння слизової у пацієнтів, які отримували інфліксимаб.
Клінічна ефективність та безпека
Артрит ревматоїдний у дорослих
Ефективність інфліксимабу оцінювали у двох багатоцентрових, рандомізованих, подвійних сліпих клінічних випробуваннях: ATTRACT та ASPIRE. В обох дослідженнях одночасне застосування стабільних доз фолієвої кислоти, пероральних кортикостероїдів (≤ 10 мг / добу) та / або не стероїдні протизапальні засоби (НПЗЗ).
Основними кінцевими точками були зменшення ознак та симптомів, визначених критеріями Американського коледжу ревматології (ACR20 для ATTRACT, індикатор ACR-N для ASPIRE), запобігання структурним пошкодженням суглобів та поліпшення фізичних функцій. А симптоми були визначені як поліпшення щонайменше 20% (ACR20) за кількістю хворобливих і набряклих суглобів та за 3 із наступних 5 критеріїв: загальна оцінка лікаря, загальна оцінка пацієнта, оцінка функції / інвалідності, візуальна аналогова шкала болю, швидкість осідання еритроцитів або С- реактивний білок. ACR-N використовує ті ж критерії, що і ACR20, розрахований з урахуванням найнижчого відсотка поліпшення кількості набряклих суглобів, хворобливих суглобів та медіани решти 5 компонентів відповіді ACR. Структурні пошкодження суглобів (ерозія та зменшення суглобової лінії) в обох руках і ногах вимірювали, оцінюючи зміну загального балу Шарпа, модифікованого ван дер Хайде (0-440). Анкета оцінки стану здоров'я (HAQ; шкала від 0 до 3) була використана для оцінки середньої зміни з плином часу фізичної функції від вихідної.
Дослідження ATTRACT оцінювало відповіді на 30, 54 та 102 тижні у плацебо-контрольованому дослідженні у 428 пацієнтів з активним ревматоїдним артритом, незважаючи на лікування метотрексатом. Приблизно 50% пацієнтів перебували у III функціональному класі. Пацієнти отримували плацебо, 3 мг / кг або 10 мг / кг інфліксимабу на 0, 2 і 6 тижнях, а потім кожні 4 або 8 тижнів. Усі пацієнти приймали стабільну дозу метотрексату (медіана 15 мг / тиждень) протягом 6 місяців до зарахування і залишалися на стабільних дозах протягом усього дослідження.
Результати на 54-му тижні (ACR20, загальний бал Шарпа, модифікований ван дер Хайде та HAQ), наведені в таблиці 3. Вища частота клінічної відповіді (ACR50 та ACR70) спостерігалася у всіх групах, які отримували інфліксимаб на 30 та 54 тижнях. порівняно з одним метотрексатом.
Зменшення швидкості прогресування структурних пошкоджень суглобів (ерозія та зменшення суглобової щілини) спостерігалося у всіх групах, які отримували інфліксимаб, на 54 тижні (табл. 3).
Ефекти, які спостерігалися на 54 -му тижні, зберігалися протягом 102 -го тижня лікування. Через кількість перерв лікування не вдалося визначити ступінь різниці в ефекті між групами монотерапії інфліксимабом та метотрексатом.
Таблиця 3
Вплив на ACR20, структурні пошкодження суглобів та фізичну функцію на 54 -му тижні, АТРАКТ
контрольований = Усі пацієнти мали активний РА, незважаючи на лікування стабільними дозами метотрексату протягом 6 місяців до зарахування, і вони повинні були залишатися у стабільних дозах протягом дослідження. дозволено застосування нестероїдних протизапальних засобів (НПЗЗ); давали добавку фолієвої кислоти.
b Усі дози інфліксимабу вводили одночасно з метотрексатом та фолатом, а в деяких випадках з кортикостероїдами та / або нестероїдними протизапальними засобами (НПЗЗ)
c стор
d більш високі значення вказують на більші пошкодження суглобів.
та HAQ = Анкета оцінки стану здоров'я; більш високі значення вказують на "меншу інвалідність.
Дослідження ASPIRE оцінювало відповіді на 54 тижні у 1004 пацієнтів, які раніше не отримували метотрексат, з активним ревматоїдним артритом (середня кількість набряклих і ніжних суглобів: 19 та 31 відповідно) з недавнього початку (тривалість захворювання ≤ 3 роки, медіана 0,6 року). Усі пацієнти отримували метотрексат (оптимізований до 20 мг / тиждень на 8 -му тижні) у поєднанні з плацебо або інфліксимабом 3 мг / кг або 6 мг / кг на 0, 2 та 6 тижнях та кожні 8 тижнів після цього. Результати на 54 тижні наведені в таблиці 4.
Після 54 тижнів лікування обидві дози інфліксимабу + метотрексату дали статистично значуще більше покращення ознак та симптомів, ніж тільки метотрексат, що вимірюється часткою пацієнтів, які досягли відповідей ACR 20, 50 та 70.
У ASPIRE більше 90% пацієнтів мали принаймні дві оцінювані рентгенограми. Зменшення швидкості прогресування структурних ушкоджень спостерігалося на 30 та 54 тижнях у групах інфліксимабу + метотрексату порівняно з одним метотрексатом.
Таблиця 4
Вплив на ACRn, структурні пошкодження суглобів та фізичну функцію на 54 -му тижні, ASPIRE
на стор
b більші значення вказують на більші пошкодження суглобів.
c опитувальник оцінки стану здоров'я; більш високі значення вказують на "меншу інвалідність.
d р = 0,030 д
Дані, що підтверджують титрування дози при ревматоїдному артриті, надходять з досліджень
АТРАКТ, АСПІР і СТАРТ. START-це рандомізоване, багатоцентрове, подвійне сліпе, 3-ричне, паралельне дослідження, дослідження безпеки. В одній із досліджуваних груп (група 2, n = 329) пацієнтам з неадекватною відповіддю дозволили титрувати дозу з кроком 1,5 мг / кг від 3 до 9 мг / кг. Більшість (67%) цих пацієнтів не потребували титрування дози. З пацієнтів, які цього потребували, 80% досягли клінічної відповіді, а більшість (64%) з них вимагали лише збільшення на 1,5 мг / кг.
Хвороба Крона у дорослих
Індукційне лікування при активній хворобі Крона середньої та важкої форми Ефективність одноразової дози інфліксимабу оцінювали у 108 пацієнтів з активною хворобою Крона розміром від помірного до важкого (індекс активності хвороби Крона (CDAI) ≥ 220 ≤ 400) у дослідженні, рандомізованому, подвійному сліпому, плацебо-контрольованій дозі З 108 пацієнтів 27 отримували рекомендовану дозу інфліксимабу (5 мг / кг). Усі пацієнти мали неадекватну відповідь на попередні традиційні методи лікування. отримувати таку терапію.
Первинною кінцевою точкою був розрахунок кількості пацієнтів, які зазнали клінічної відповіді, визначеної як зменшення CDAI на ≥ 70 балів від вихідного рівня, на 4 -му тижні і без збільшення використання ліків або хірургічних втручань щодо захворювання. Пацієнти, які відповіли на 4 -й тиждень, проходили спостереження до 12 -го тижня. Вторинні кінцеві точки включали кількість пацієнтів, які перебували у клінічній ремісії на 4 -му тижні (CDAI
На 4 тижні після введення одноразової дози у 22/27 (81%) пацієнтів, які отримували інфліксимаб у дозі 5 мг/кг, була клінічна відповідь порівняно з 4/25 (16%) пацієнтів, які отримували плацебо (p
Підтримуюче лікування при активній хворобі Крона середньої та важкої форми у дорослих
Ефективність повторних інфузій з інфліксимабом оцінювали у 1-річному клінічному дослідженні (ACCENT I). Загалом 573 пацієнти з помірною та важкою активною хворобою Крона (CDAI ≥ 220 ≤ 400) отримували одноразову інфузію 5 мг / кг на тиждень 0. 178 із 580 зарахованих пацієнтів (30,7%) мали важке захворювання (показник CDAI> 300 та супутня терапія кортикостероїдами та / або імунодепресантами), що відповідає популяції, визначеній у показаннях (див. Розділ 4.1). На 2 -му тижні всіх пацієнтів оцінювали для клінічної відповіді та рандомізовано в одну з 3 груп лікування; групу підтримки плацебо, групу підтримки 5 мг / кг та підтримку 10 мг / кг. Потім усі 3 групи отримували повторні інфузії на 2, 6 тижні та кожні 8 тижнів після цього. .
З 573 рандомізованих пацієнтів 335 (58%) досягли клінічної відповіді на 2 -му тижні. Ці пацієнти були класифіковані як відповіді на 2 -й тиждень і включені до первинного аналізу (див. Таблицю 5). Тиждень 2, 32% (26/81) у плацебо -підтримуючої групи та 42% (68/163) у підтримуючій групі інфліксимабу досягли клінічної відповіді на 6 -му тижні. Після цього не було ніякої різниці між групами в кількості пацієнтів, які згодом відповіли на терапію.
Супутніми первинними кінцевими точками були відсотки пацієнтів у клінічній ремісії (CDAI
Таблиця 5
Вплив на швидкість реакції та ремісію, дані ACCENT I (пацієнти досягають відповіді на 2 тижні)
a Зниження CDAI ≥ 25% та ≥ 70 балів.
b CDAI
На початку 14-го тижня пацієнти, які відповіли на лікування, але згодом втратили клінічну користь, були переведені на дозу інфліксимабу на 5 мг / кг, більшу за дозу, до якої вони були рандомізовані. L "Вісімдесят дев'ять відсотків (50 / 56) пацієнтів, які втратили клінічну відповідь на підтримуючу терапію інфліксимабу 5 мг / кг після 14 тижня, відповіли на лікування 10 мг / кг інфліксимабу.
На 30 та 54 тижнях у групах підтримки інфліксимабу спостерігалося поліпшення оцінки якості життя, зменшення кількості госпіталізацій, пов’язаних із захворюваннями, та застосування кортикостероїдів порівняно з групою підтримки плацебо.
Інфліксимаб з АЗА або без нього оцінювали у рандомізованому подвійному сліпому дослідженні з активним порівнянням (SONIC) 508 дорослих пацієнтів з помірною та тяжкою хворобою Крона (CDAI ≥ 220 ≤ 450), які раніше ніколи не лікувалися біологічними препаратами та імунодепресанти та із середньою тривалістю захворювання 2,3 року. На початку 27,4% пацієнтів отримували системні кортикостероїди, 14,2% пацієнтів-будесонід та 54,3% пацієнтів-сполуки 5-АСК. Пацієнти були рандомізовані для отримання монотерапії AZA, монотерапії інфліксимабом або комбінованої терапії AZA. Інфліксимаб вводили у дозі 5 мг / кг на 0, 2, 6 тижні та кожні 8 тижнів після цього. AZA вводили у добовій дозі 2,5 мг / кг.
Первинною кінцевою точкою дослідження була клінічна ремісія без кортикостероїдів на 26-му тижні, що визначається як пацієнти з клінічною ремісією (CDAI преднізолон або еквівалент) або будесонід у дозі> 6 мг / добу. на 26 -му тижні були значно вищими у групах комбінованої терапії інфліксимабом та AZA (43,9%, стор
Таблиця 6
Відсоток пацієнтів, які досягли клінічної ремісії без кортикостероїдів на 26 тижні, SONIC
* Значення P представляють кожну групу лікування інфліксимабом порівняно з монотерапією AZA
Подібні закономірності досягнення клінічної ремісії без кортикостероїдів спостерігалися на 50-му тижні. Крім того, покращення якості життя спостерігалося при застосуванні інфліксимабу, як повідомляється в опитувальнику IBDQ.
Індукційне лікування при активній фістулізуючій хворобі Крона
Ефективність оцінювали у рандомізованому подвійному сліпому плацебо-контрольованому дослідженні у 94 пацієнтів з хворобою Крона, які мали свищі протягом щонайменше 3 місяців. Тридцять один з цих пацієнтів отримував 5 мг / кг інфліксимабу. Близько 93% пацієнтів, які раніше проходили антибіотикотерапію або імуносупресивну терапію.
Допускалося одночасне застосування незміненої дози звичайної терапії, і 83% пацієнтів продовжували отримувати принаймні одну з цих терапій.Пацієнти отримували три дози плацебо або інфліксимабу на 0, 2 та 6 тижнях. Первинною кінцевою точкою була кількість пацієнтів, які зазнали клінічної відповіді, що визначається як зменшення ≥ 50% від вихідного рівня кількості продувних свищів після легкого стиснення щонайменше у двох послідовних контролях (через 4 тижні) без збільшення вживання наркотиків або операція з приводу хвороби Крона.
68% (21/31) пацієнтів, які отримували інфліксимаб у дозі 5 мг/кг, зазнали клінічної відповіді порівняно з 26% (8/31) пацієнтів, які отримували плацебо (р = 0,002). Середній час відповіді у групі інфліксимабу становив 2 тижні. Середня тривалість відповіді становила 12 тижнів. Крім того, закриття всіх нориць спостерігалося у 55% пацієнтів, які отримували інфліксимаб, у порівнянні з 13% пацієнтів, які отримували плацебо (р = 0,001).
Підтримуюче лікування при активній фістулізуючій хворобі Крона
Ефективність повторних інфузій інфліксимабу у пацієнтів з фістулізуючою хворобою Крона оцінювали у 1-річному дослідженні (АКЦЕНТ II). Усього 306 пацієнтів отримували 3 дози по 5 мг / кг інфліксимабу на 0, 2 та 6 тижнях. , 87% пацієнтів мали періанальні свищі, 14% мали абдомінальні свищі, 9% мали ректовагінальні свищі. Середній показник CDAI становив 180. На 14 тижні 282 пацієнта оцінили на клінічну відповідь та рандомізували на лікування плацебо або інфліксимабом у дозі 5 мг. / кг кожні 8 тижнів до 46 тижня.
Пацієнтів, які відповіли на 14 тиждень (195/282), аналізували на предмет первинної кінцевої точки, тобто часу між рандомізацією та втратою відповіді (див. Таблицю 7). Зниження кортикостероїдів було дозволено після 6 тижня.
Таблиця 7
Вплив на швидкість реакції, дані дослідження ACCENT II (пацієнти досягають відповіді на 14 тижні)
a ≥ 50% зменшення кількості зливних свищів від вихідного рівня протягом періоду ≥ 4 тижнів
b Відсутність дренуючих свищів
На початку 22 тижня пацієнти, які спочатку відповіли на лікування, а згодом втратили відповідь, переходили на активне повторне лікування кожні 8 тижнів у дозі інфліксимабу на 5 мг / кг вище, ніж доза, у якій вони були рандомізовані. у групі підтримки інфліксимабу 5 мг / кг, яка перейшла на активне лікування, оскільки втратила відповідь на зменшення свища після 22 тижня, 57% (12/21) відповіли на повторне лікування інфліксимабом 10 мг / кг кожні 8 тижнів.
Між плацебо та інфліксимабом не було значної різниці у частці пацієнтів із тривалим закриттям всіх свищів до 54 тижня, у симптомах прокталгії, абсцесу та інфекцій сечовивідних шляхів або у кількості нових свищів, що з’явилися під час лікування.
Підтримуюча терапія інфліксимабом кожні 8 тижнів значно зменшила кількість госпіталізацій та операцій, пов’язаних із захворюваннями, порівняно з плацебо. Крім того, спостерігалося зменшення використання кортикостероїдів та поліпшення якості життя.
Виразковий коліт у дорослих
Безпеку та ефективність Remicade оцінювали у двох рандомізованих подвійних сліпих плацебо-контрольованих клінічних випробуваннях (ACT 1 та ACT 2) у дорослих пацієнтів з помірним та важким активним виразковим колітом (оцінка Мейо від 6 до 12; ендоскопічний суббалл ≥ 2) з неадекватною відповіддю на звичайну терапію [пероральні кортикостероїди, аміносаліцилати та / або імуномодулятори (6 МП, AZA)]. Допускалося одночасне застосування пероральних аміносаліцилатів, кортикостероїдів та / або імуномодулюючих препаратів. або Ремікейд 5 мг / кг або Ремікейд 10 мг / кг на 0, 2, 6, 14 і 22 тижнях і в АКТ 1 на тижнях 30, 38 та 46. Зниження кортикостероїдів було дозволено через 8 тижнів.
Таблиця 8
Вплив на клінічну реакцію, клінічну ремісію та загоєння слизових на 8 та 30 тижнях.
Об’єднані дані з АКТ 1 і 2
на стор
Ефективність Remicade на 54 тижні оцінювали у дослідженні ACT 1.
На 54 тижні у 44,9% пацієнтів у групі комбінованого лікування інфліксимабом була клінічна відповідь порівняно з 19,8% у групі плацебо (p
Більша частина пацієнтів у комбінованій групі інфліксимабу змогла припинити лікування кортикостероїдами та залишатися у клінічній ремісії порівняно з групою плацебо на обидва тижні (22,3% проти 7,2%, p
Об’єднані дані досліджень ACT 1 та ACT 2 та їх розширення, проаналізовані від вихідного рівня до 54-го тижня, продемонстрували зменшення госпіталізацій та хірургічних втручань, пов’язаних з виразковим колітом, після лікування інфліксимабом. Кількість госпіталізацій, пов’язаних з виразковим колітом, була значно нижчою у групах лікування 5 та 10 мг / кг інфліксимабу порівняно з групою плацебо (середня кількість госпіталізацій на 100 пацієнтів на рік: 21 та 19 проти 40 у групі плацебо; p = 0,019 і р = 0,007 відповідно).
Кількість операцій, пов’язаних з виразковим колітом, також була нижчою у групах лікування 5 та 10 мг / кг інфліксимабу порівняно з групою плацебо (середня кількість операцій на 100 пацієнтів на рік: 22 та 19 проти 34; p = 0,145 та p = 0,022 відповідно).
Було зібрано та об’єднано кількість суб’єктів, які в будь -який час протягом 54 тижнів після першої інфузії досліджуваного агента пройшли колектомію, та об’єднали її з даними досліджень ACT 1 та ACT 2 та їх розширення. /кг групи (28/242 або 11,6% [NS]) та у групі інфліксимабу 10 мг/кг (18/242 або 7,4% [p = 0,011]) порівняно з групою плацебо (36/244; 14,8%).
Зменшення захворюваності на колектомію також вивчалося в іншому рандомізованому подвійному сліпому дослідженні (C0168Y06) у госпіталізованих пацієнтів (n = 45) з помірним та важким активним виразковим колітом, які не реагували на внутрішньовенні кортикостероїди. високий ризик для колектомії. За 3 місяці після інфузії було значно менше колектомій у пацієнтів, які отримували разову дозу інфліксимабу 5 мг / кг, порівняно з пацієнтами, які отримували плацебо (29,2 % проти 66,7 % відповідно, р = 0,017).
У дослідженнях ACT 1 та ACT 2 інфліксимаб покращив якість життя, що підтверджено статистично значущим поліпшенням як у вимірі параметра конкретної хвороби, IBDQ, так і у покращенні 36 загальних питань, що складають SF-36.
Анкілозуючий спондилоартрит у дорослих
Ефективність та безпеку інфліксимабу вивчали у двох подвійних сліпих, плацебо-контрольованих багатоцентрових дослідженнях у пацієнтів з активним анкилозуючим спондилітом (показник ванночки активності хвороби Бехтерева [BASDAI] ≥ 4 та біль у хребті ≥ 4 за шкалою від 1 до 10).
У першому дослідженні (P01522), яке включало 3-місячну подвійну сліпу фазу, 70 пацієнтів лікувалися або інфліксимабом 5 мг / кг, або плацебо на 0, 2, 6 тижні (35 пацієнтів у групі). З 12-го тижня пацієнти, які досі отримували плацебо, почали отримувати інфліксимаб у дозі 5 мг / кг кожні 6 тижнів до 54-го тижня. Після першого року 53 пацієнти були поміщені у відкритий протокол до 102-го тижня.
У другому клінічному дослідженні (ASSERT) 279 пацієнтів були рандомізовані для лікування плацебо (група 1, n = 78) або інфліксимабом 5 мг / кг (група 2, n = 201) через 0, 2, 6 та кожні 6 тижнів через 24 тиждень. Після цього всі досліджувані продовжували приймати інфліксимаб кожні 6 тижнів до 96 тижня. Група 1 отримувала дозу інфліксимабу 5 мг / кг. У групі 2, починаючи з 36 -го тижня, пацієнтів, які мали BASDAI ≥ 3 протягом 2 послідовних відвідувань, лікували дозою інфліксимабу 7,5 мг / кг кожні 6 тижнів до 96 тижня.
У дослідженні ASSERT покращення ознак та симптомів спостерігалося з 2 -го тижня. На 24 -му тижні кількість пацієнтів, які мали відповідь на ASAS 20, становила 15/78 (19%) у групі плацебо та дорівнювала 123/201 (61 %) у групі інфліксимабу 5 мг / кг (стор
У дослідженні P01522 поліпшення ознак та симптомів спостерігалося з 2 -го тижня. На 12 -му тижні пацієнтів, які мали відповідь на BASDAI 50, було 3/35 (9 %) у групі плацебо та 20/35 (57 %) у інфліксимабі 5 мг / кг група (стор
В обох дослідженнях фізичні функції та якість життя, виміряні за BASFI та показником фізичних компонентів за шкалою SF-36, значно покращилися.
Псоріатичний артрит у дорослих
Ефективність та безпеку оцінювали у двох подвійних сліпих, плацебо-контрольованих, багатоцентрових дослідженнях у пацієнтів з активним псоріатичним артритом.
У першому клінічному дослідженні (IMPACT) ефективність та безпеку застосування інфліксимабу вивчали у 104 пацієнтів з поліартикулярним активним псоріатичним артритом. 0, 2, 6 і 14 (по 52 пацієнта в кожній групі). Починаючи з 16 -го тижня, пацієнти у групі плацебо були переведені на інфліксимаб, а потім усі пацієнти отримували інфліксимаб у дозі 5 мг / кг кожен. 8 тижнів на тиждень 46. Після першого року дослідження 78 пацієнтів продовжили відкрите продовження до 98 тижня.
У другому клінічному дослідженні (IMPACT 2) ефективність та безпеку застосування інфліксимабу вивчали у 200 пацієнтів з активним псоріатичним артритом (набряклі суглоби ≥ 5 та болючі суглоби ≥ 5). 46 % пацієнтів продовжували приймати фіксовані дози метотрексату ( ≤ 25 мг / тиждень) Під час 24-тижневої подвійної сліпої фази пацієнти отримували або 5 мг / кг інфліксимабу, або плацебо на 0, 2, 6, 14 та 22 тижнях (по 100 пацієнтів у кожній групі). 47 пацієнтів отримували плацебо з поліпшенням стану
Основні результати ефективності для IMPACT та IMPACT 2 наведено нижче
Таблиця 9
Вплив на ACR та PASI у IMPACT та IMPACT 2
* ITT-аналіз, до якого були включені суб'єкти з відсутніми даними Ні-респонденти
на 98-му тижні дані IMPACT включали пацієнтів із групи плацебо та пацієнтів, які отримували інфліксимаб, які вступили на відкрите продовження
b Виходячи з пацієнтів з PASI ≥ 2,5 на початковому етапі для IMPACT та пацієнтів із залученням псоріатичної площі поверхні тіла (BSA) на початковому рівні ≥ 3% у IMPACT 2
** Відповідь PASI 75 для IMPACT не включена через низький N; стор
У IMPACT та IMPACT 2 клінічна відповідь спостерігалася вже на 2 -му тижні і зберігалася відповідно до 98 -го та 54 -го тижня відповідно. Ефективність була продемонстрована як при одночасному застосуванні метотрексату, так і без нього. У пацієнтів, які отримували інфліксимаб, спостерігалося зниження параметрів периферичної активності, характерних для псоріатичного артриту (таких як кількість набряклих суглобів, кількість хворобливих / чутливих суглобів, дактиліт та наявність ентезопатій).
Рентгенологічні зміни оцінювали в IMPACT2. Рентгенограми рук і ніг були зібрані на початковому етапі, 24 тижні та 54 тиждень. Лікування інфліксимабом зменшило швидкість прогресування периферичних пошкоджень суглобів порівняно з лікуванням плацебо на першому кінцевому етапі 24 тижня, що вимірювалося як зміна від вихідного рівня у зміненому загальному показнику vdH -S (середній бал ± SD становив 0,82 ± 2,62 у групі плацебо проти - 0,70 ± 2,53 у групі інфліксимабу; p
Значне поліпшення фізичної функції за оцінкою HAQ було продемонстровано у пацієнтів, які отримували інфліксимаб. Також було продемонстровано значне поліпшення якості життя, виміряне сумарним показником фізичних та психічних компонентів SF-36 у IMPACT 2.
Псоріаз у дорослих
Ефективність інфліксимабу оцінювали у двох рандомізованих подвійних сліпих багатоцентрових дослідженнях SPIRIT та EXPRESS. Пацієнти в обох дослідженнях мали псоріаз із бляшками (BSA [площа поверхні тіла] ≥ 10% та оцінка PASI [площа псоріазу та індекс тяжкості] ≥ 12 ) Первинною кінцевою точкою в обох дослідженнях була частка пацієнтів, які досягли ≥ 75% поліпшення показника PASI від вихідного рівня на 10 тижні.
SPIRIT оцінив ефективність індукційної терапії інфліксимабом у 249 пацієнтів із бляшковим псоріазом, які раніше отримували PUVA або системну терапію. мали право на додаткову інфузію того ж лікування на 26 тижні.
У SPIRIT частка пацієнтів, які досягли PASI 75 на 10 тижні, становила 71,7% у групі інфліксимабу 3 мг / кг, 87,9% у групі інфліксимабу 5 мг / кг та у групі інфліксимабу 5 мг / кг. 5,9% у групі група плацебо (р 20 тижнів. Не спостерігалося явищ відскоку.
Компанія EXPRESS оцінила ефективність індукційної та підтримуючої терапії інфліксимабом у 378 пацієнтів із бляшковим псоріазом. і протягом 46 -го тижня у групі інфліксимабу. На 24 -му тижні група плацебо перейшла на індукційну терапію інфліксимабом (5 мг / кг), а потім підтримуючу терапію інфліксимабом (5 мг / кг). ) Попередню терапію PUVA, метотрексатом, циклоспорином або ацитретином отримали 71,4% пацієнтів, хоча вони не обов’язково були стійкими до терапії. Найбільш значні результати представлені в таблиці 10. У пацієнтів, які отримували інфліксимаб, значні відповіді на PASI 50 були видно у першому ст isita (тиждень 2) та відповіді на PASI 75 під час другого відвідування (тиждень 6). Ефективність у підгрупі пацієнтів, які раніше проходили системну терапію, була такою ж, як і в загальній популяції досліджуваного.
Таблиця 10
Резюме відповідей PASI, відповідей PGA та відсоток пацієнтів, у яких всі нігті зажили на 10, 24 та 50 тижнях. EXPRESS.
на стор
b n = 292
c Аналіз проводився на суб’єктах з псоріазом нігтів на початковому етапі (81,8% пацієнтів). Середні вихідні показники NAPSI становили 4,6 та 4,3 у групах інфліксимабу та плацебо.
Значні поліпшення щодо базового рівня були очевидні в DLQI (стор
Педіатричне населення
Хвороба Крона у педіатричних пацієнтів (6-17 років)
У дослідженні REACH 112 пацієнтів (у віці 6-17 років, середній вік 13 років) з помірною до важкої активної хворобою Крона (середнє значення CDAI у дітей 40) та з неадекватною відповіддю на звичайну терапію, отримували 5 мг / кг інфліксимабу на 0, 2 та 6 тижнях. Для всіх пацієнтів була потрібна стабільна доза 6 МП, AZA або МТХ (35% також були на кортикостероїдах на початку). Пацієнти, які, на думку дослідника, мали клінічну відповідь на 10 тижні, були рандомізовані у дві групи та отримували інфліксимаб у дозі 5 мг / кг кожні 8 тижнів або кожні 12 тижнів як підтримуючу терапію.Якщо відповідь була втрачена під час підтримки, допускався перехід на більш високу дозу (10 мг / кг) та / або з меншими інтервалами між інфузіями (кожні 8 тижнів). Тридцять два педіатричних пацієнта, які оцінювалися для цілей дослідження, зазнали цього переходу (9 пацієнтів у групі отримували лікування кожні 8 тижнів і 23 суб’єкти у групі-кожні 12 тижнів). Двадцять чотири з цих пацієнтів (75,0%) відновили клінічну відповідь після цього переходу.
Відсоток пацієнтів з клінічною відповіддю на 10 тижні становив 88,4% (99/112). Відсоток суб’єктів, які досягли клінічної ремісії на 10 тижні, становив 58,9% (66/112).
На 30 тижні відсоток пацієнтів у клінічній ремісії був вищим у кожній 8 -тижневій групі (59,6%, 31/52), ніж у пацієнтів у кожній 12 -тижневій групі підтримки (35,3%, 18/51; p = 0,013) . На 54 -му тижні дані були такими: 55,8% (29/52) у групі підтримуючого лікування кожні 8 тижнів та 23,5% (12/51) у групі підтримуючого лікування кожні 12 тижнів (p
Дані про нориці були отримані з балів PCDAI. З 22 пацієнтів, які мали вихідні нориці, 63,6% (14/22), 59,1% (13/22) і 68,2% (15/22) отримали повну відповідь щодо фістули. На 10, 30 тижні та 54, відповідно, враховуючи загалом групи підтримки як тих, хто отримує лікування кожні 8 тижнів, так і тих, хто отримує лікування кожні 12 тижнів.
Крім того, було помічено статистично та клінічно значне поліпшення якості життя та зростання, а також значне зменшення вживання кортикостероїдів від вихідного рівня.
Виразковий коліт у дітей (6-17 років)
Безпеку та ефективність інфліксимабу оцінювали у багатоцентровому рандомізованому відкритому паралельному груповому клінічному дослідженні (C0168T72) у 60 педіатричних пацієнтів віком 6-17 років (середній вік 14,5 років) з колітом. Оцінка Mayo від 6 до 12; ендоскопічний суббалл ≥ 2) з неадекватною відповіддю на звичайну терапію. На початку 53% пацієнтів отримували імуномодулюючу терапію (6-MP, AZA та / або MTX), а 62% пацієнтів-кортикостероїди. імуномодулятори та зменшення кортикостероїдів було дозволено після 0 тижня.
Усі пацієнти отримували режим індукції 5 мг / кг інфліксимабу на 0, 2 та 6 тижнях. Пацієнти, які не відповіли на інфліксимаб на 8-му тижні (n = 15), не отримували ліків і повернулися для подальшого спостереження за оцінкою безпеки. На 8 тижні 45 пацієнтів були рандомізовані та отримували підтримуюче лікування інфліксимабом у дозі 5 мг / кг кожні 8 тижнів або кожні 12 тижнів.
Частка пацієнтів з клінічною відповіддю на 8 тижні становила 73,3% (44/60). Клінічна відповідь на 8 -му тижні була аналогічною у пацієнтів з початковим застосуванням імуномодуляторів та без них. Клінічна ремісія на 8 -му тижні становила 33,3% (17/51), виміряну за показником індексу активності дитячого виразкового коліту (PUCAI).
На 54 тижні частка пацієнтів у клінічній ремісії, виміряна за показником PUCAI, становила 38% (8/21) у 8-тижневій групі підтримки та 18% (4/22) у кожній 12-тижневій групі підтримки. . Для пацієнтів, які отримували кортикостероїди на початковому етапі, частка пацієнтів, які перебували у стадії ремісії та не отримували кортикостероїди на 54 -му тижні, становила 38,5% (5/13) у кожній 8 -тижневій групі підтримки та 0% (0 /13) у групі підтримуючого лікування кожні 12 тижнів.
У цьому дослідженні було більше пацієнтів у віковій групі від 12 до 17 років, ніж у віці від 6 до 11 років (45/60 проти 15/60). Хоча кількість пацієнтів у кожній підгрупі була замалою для того, щоб робити чіткі висновки щодо «впливу віку», у молодшій віковій групі було більша кількість пацієнтів, які збільшили дозу або припинили лікування через недостатню ефективність.
Інші педіатричні показання
Європейське агентство з лікарських засобів відмовилося від зобов’язання подавати результати досліджень з Remicade у всіх підгрупах педіатричної популяції при ревматоїдному артриті, ювенільному ідіопатичному артриті, псоріатичному артриті, хворобі Бехтерева, псоріазі та хворобі Крона (див. Розділ 4.2 для інформації про застосування у педіатрії ).
05.2 "Фармакокінетичні властивості
Одноразові внутрішньовенні інфузії 1, 3, 5, 10 або 20 мг / кг інфліксимабу збільшували як максимальну сироваткову концентрацію (Cmax), так і площу під кривою концентрація-час (AUC) у пропорційному дозі розподілі у рівноважному стані. (середнє значення Vd 3,0-4,1 літра) не залежало від введеної дози, що свідчить про те, що інфліксимаб переважно розподіляється у судинному відділі. Не спостерігалося залежності фармакокінетичних характеристик від часу. інфліксимаб не був охарактеризований. у пацієнтів з ревматоїдним артритом спостерігалися значні відмінності у кліренсі або об’ємі розподілу, пов’язані з віком або масою тіла. Фармакокінетика інфліксимабу у пацієнтів літнього віку не вивчена. Не проводилося досліджень у пацієнтів з порушенням функції печінки або нирок.
При одноразових дозах 3, 5 або 10 мг / кг середні значення Cmax становили 77, 118 та 277 мкг / мл відповідно. Середній кінцевий період напіввиведення у цих дозах коливався від 8 до 9,5 днів. У більшості пацієнтів при рекомендованій разовій дозі 5 мг / кг при хворобі Крона та 3 мг / кг кожні 8 тижнів для підтримки. При ревматоїдному артриті інфліксимаб міг би виявляються в сироватці крові щонайменше 8 тижнів.
Повторне введення інфліксимабу (5 мг / кг на 0, 2 і 6 тижнях при фістулізуючій хворобі Крона, 3 або 10 мг / кг кожні 4 або 8 тижнів при ревматоїдному артриті) призвело до незначного накопичення інфліксимабу в сироватці крові після другої дози. спостерігалося клінічно значуще накопичення
Педіатричне населення
"Популяційний фармакокінетичний аналіз на основі даних, отриманих від пацієнтів з виразковим колітом (N = 60), хворобою Крона (N = 112), ювенільним ревматоїдним артритом (N = 117) та хворобою Кавасакі (N = 16) у віці від 2 місяців до Загалом 17 років показали, що вплив інфліксимабу нелінійно залежить від маси тіла. Після введення 5 мг / кг препарату Ремікейд кожні 8 тижнів очікувана середня експозиція інфліксимабу у рівноважному стані (площа під кривою концентрація-час у рівноважному стані, AUCss) у педіатричних пацієнтів віком від 6 до 17 років була приблизно на 20% нижчою Медіана AUCss у педіатричних пацієнтів віком від 2 до 6 років була прогнозованою приблизно на 40% нижче, ніж у дорослих, хоча кількість пацієнтів, які підтверджують цю оцінку, обмежена.
05.3 Дані доклінічної безпеки
Інфліксимаб не перехресно реагує з ФНП у інших видів тварин, окрім людини та шимпанзе. Тому звичайні доклінічні дані про безпеку застосування інфліксимабу обмежені. виявлено, токсичність для матері, ембріотоксичність, тератогенність. У дослідженні фертильності та загальної репродуктивної функції кількість вагітних мишей зменшилася після введення того самого аналогового антитіла. Невідомо, чи були ці результати наслідком впливу на чоловіків та / або жінок. У 6-місячному дослідженні токсичності при повторних дозах на щурах, використовуючи ті ж аналогічні антитіла до мишачого TNFα, на капсулі кришталика деяких оброблених самців щурів спостерігалися кристалічні відкладення. Жодного конкретного офтальмологічного обстеження пацієнтів не проводили для оцінки важливості цієї події у людей. Довгострокових досліджень для оцінки канцерогенного потенціалу інфліксимабу не проводилося. У дослідженнях, проведених на мишах з дефіцитом TNFα, було показано, що немає збільшення пухлин при спровокуванні відомими ініціаторами пухлини та / або промоторами.
06.0 ФАРМАЦЕВТИЧНА ІНФОРМАЦІЯ
06.1 Допоміжні речовини
Сахароза
Полісорбат 80
Одноосновний фосфат натрію
Двоосновний фосфат натрію
06.2 Несумісність
За відсутності досліджень сумісності цей лікарський засіб не слід змішувати з іншими лікарськими засобами.
06.3 Строк дії
До відновлення:
3 роки при 2 ° C - 8 ° C.
Remicade можна зберігати при температурі не вище 25 ° C протягом одного періоду до 6 місяців, але не пізніше початкового терміну придатності. Новий термін придатності повинен бути написаний на коробці. Після виймання з холодильника Remicade більше не слід зберігати в холодильнику.
Після відновлення:
Хімічна та фізична стабільність відновленого розчину у процесі використання була продемонстрована протягом 24 годин при температурі 25 ° C. З мікробіологічної точки зору продукт слід використати якомога швидше, а в будь-якому випадку-протягом 3 годин після відновлення та розведення . Якщо не використати негайно, час зберігання та умови зберігання перед використанням є відповідальністю користувача і ні в якому разі не повинні перевищувати 24 години при температурі від 2 ° C до 8 ° C.
06.4 Особливі умови зберігання
Зберігати в холодильнику (2 ° C - 8 ° C).
Щодо умов зберігання до 25 ° C перед розчиненням лікарського засобу, див. Розділ 6.3.
Щодо умов зберігання після розчинення лікарського засобу, див. Розділ 6.3.
06.5 Характер негайної упаковки та вміст упаковки
Скляний флакон типу I з гумовою пробкою та алюмінієвим обтиском, захищений пластиковою кришкою, що містить 100 мг інфліксимабу.
Remicade випускається в упаковках по 1, 2, 3, 4 або 5 флаконів. Не всі розміри упаковок можна продавати.
06.6 Інструкції з використання та поводження
1. Обчисліть дозу та кількість необхідних флаконів Remicade. Кожен флакон Remicade містить 100 мг інфліксимабу. Обчисліть загальний об’єм, необхідний для відновленого розчину Remicade.
2. В асептичних умовах розведіть кожен флакон Remicade з 10 мл води для ін’єкцій за допомогою шприца з голкою 21 калібру (0,8 мм) або менше. Зніміть алюмінієву вкладку з флакона і очистіть ковпачок ватним тампоном, змоченим у 70% спирті. Вставте голку шприца у флакон через середину гумової пробки та направте потік води для ін’єкцій до скляної стінки флакона. Обережно покрутіть розчин, щоб повністю розчинити ліофілізований порошок. Не струшуйте сильно або протягом тривалого часу . НЕ ТРИСАЙТЕ. Під час відновлення може утворитися піна. Дайте відстояному розчину постояти 5 хвилин. Перевірте, щоб розчин був безбарвним до жовтого кольору та опалесцентним, у розчині можуть бути невеликі напівпрозорі частинки, оскільки інфліксимаб є білком. Не використовуйте рішення, якщо ви помітили тьмяні частинки, зміну кольору або інші сторонні тіла.
3. Розведіть загальний об’єм дози відновленого розчину Remicade до 250 мл, використовуючи для інфузій розчин хлориду натрію 9 мг / мл (0,9%). Не розбавляйте відновлений розчин Remicade будь -яким іншим розчинником. Це можна зробити, вилучивши об'єм розчину натрію хлориду 9 мг / мл (0,9%) для інфузій із скляної пляшки або інфузійного пакета на 250 мл, що дорівнює об'єму відновленого Remicade. Повільно додайте загальний об’єм відновленого розчину Remicade до флакона або інфузійного пакета по 250 мл. Акуратно перемішайте.
4. Введіть інфузійний розчин протягом часу інфузії, що не менше рекомендованого часу інфузії (див. Розділ 4.2). Використовуйте лише інфузійний набір зі стерильним, непірогенним, рядним фільтром з низьким зв'язуванням білка (діаметр пір 1,2 мікрометра або менше). Оскільки консервант не міститься, рекомендується розпочати введення розчину для внутрішньовенної інфузії якомога швидше та протягом 3 годин після розведення та розведення. Якщо відновлення та розведення проводиться в асептичних умовах, інфузійний розчин Remicade можна використовувати протягом 24 годин при зберіганні при температурі від 2 ° C до 8 ° C. Невикористаний розчин не слід зберігати для подальшого використання.
5. Дослідження фізичної та біохімічної сумісності не проводилися для оцінки комбінації препарату Ремікейд з іншими препаратами. Не вводьте Remicade одночасно з іншими лікарськими засобами в тій же внутрішньовенній лінії.
6. Перед введенням візуально огляньте Remicade, щоб переконатися, що немає частинок або зміни кольору.Якщо спостерігаються непрозорі частинки, зміна кольору або сторонні частинки, не використовуйте
7. Невикористані ліки та відходи, отримані з цього препарату, необхідно утилізувати відповідно до місцевих правил.
07.0 ВЛАСНИК РОЗРОБНИЦТВА
Janssen Biologics B.V. Ейнштейнвег 101
2333 CB Leiden
Нідерланди
08.0 НОМЕР РОЗВИТКУ З РОБОТИ
ЄС/1/99/116/001
034528012
ЄС/1/99/116/002
ЄС/1/99/116/003
ЄС/1/99/116/004
ЄС/1/99/116/005
09.0 ДАТА ПЕРШОГО ДОЗВІЛЕННЯ АБО ОНОВЛЕННЯ ДОЗВІЛЛЯ
Дата першого дозволу: 13 серпня 1999 р. Дата останнього оновлення: 02 липня 2009 р.
10.0 ДАТА ПЕРЕГЛЯНУ ТЕКСТУ
24 вересня 2015 року