Діючі речовини: Вільдагліптин
Галвус таблетки по 50 мг
Показання Для чого використовується Galvus? Для чого це?
Діюча речовина препарату Галвус, вілдагліптин, належить до групи лікарських засобів, які називаються «пероральними протидіабетиками».
Galvus використовується для лікування дорослих пацієнтів з діабетом 2 типу. Застосовується, коли діабет неможливо контролювати лише за допомогою дієти та фізичних вправ. Він допомагає контролювати рівень цукру в крові. Ваш лікар призначить Galvus окремо або разом. Інші протидіабетичні препарати ви вже приймаєте, якщо вони не були достатньо ефективними для контролю діабету.
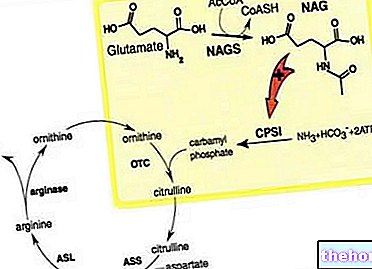
Діабет 2 типу розвивається, коли організм не виробляє достатню кількість інсуліну, або якщо інсулін, що виробляється організмом, працює не так, як слід. Він також може розвинутися, коли організм виробляє занадто багато глюкагону.
Інсулін - це речовина, що сприяє зниженню рівня цукру в крові, особливо після їжі.
Як працює Galvus
Галвус діє, змушуючи підшлункову залозу виробляти більше інсуліну і менше глюкагону. Це допомагає контролювати рівень цукру в крові. Було показано, що цей препарат знижує рівень цукру в крові. Це може запобігти ускладненням діабету. Навіть якщо ви зараз починаєте приймати ліки від діабету, важливо продовжувати дотримуватися рекомендованої дієти та / або фізичних вправ.
Протипоказання Коли Галвус не слід застосовувати
Не приймайте Galvus:
- якщо у вас алергія на вілдагліптин або будь -який інший інгредієнт цього препарату (перерахований у розділі 6). Якщо ви думаєте, що у вас алергія на вілдагліптин або будь -який інший інгредієнт Galvus, не приймайте цей препарат і зверніться до лікаря.
Заходи безпеки при застосуванні Що потрібно знати, перш ніж приймати Galvus
Перед тим, як приймати Галвус, поговоріть зі своїм лікарем, фармацевтом або медсестрою з діабету
- якщо у вас діабет 1 типу (ваше тіло не виробляє інсулін) або якщо у вас є стан, що називається діабетичним кетоацидозом.
- якщо ви приймаєте протидіабетичний препарат, відомий як сульфонілсечовина (якщо ви приймаєте його разом з Galvus, ваш лікар може захотіти зменшити дозу сульфанілсечовини, щоб уникнути зниження рівня глюкози в крові [гіпоглікемія]).
- якщо у вас помірне або тяжке захворювання нирок (вам потрібно буде прийняти меншу дозу Galvus).
- якщо ви перебуваєте на діалізі
- якщо у вас захворювання печінки
- якщо ви страждаєте на серцеву недостатність
- якщо у вас є або колись було захворювання підшлункової залози
Якщо ви раніше приймали вілдагліптин, але вам довелося припинити його через захворювання печінки, не слід приймати цей препарат.
Ураження шкіри є поширеним ускладненням діабету. Рекомендується дотримуватись рекомендацій щодо догляду за шкірою та стопами, наданих лікарем або медсестрою, а також приділяти особливу увагу розвитку пухирів або виразок під час прийому препарату Галвус. Якщо це сталося, слід негайно звернутися до лікаря.
Перед початком лікування препаратом Галвус буде проведено обстеження для оцінки функціонування печінки, яке буде повторюватися кожні три місяці протягом першого року лікування та періодично після цього. Це необхідно для якнайшвидшого виявлення ознак підвищення печінкових ферментів.
Діти та підлітки
Застосування Galvus дітям та підліткам до 18 років не рекомендується.
Взаємодії Які ліки або продукти харчування можуть змінити дію Galvus
Повідомте свого лікаря або фармацевта, якщо ви приймаєте, нещодавно приймали або могли б приймати будь -які інші ліки.
Ваш лікар, можливо, захоче змінити дозу Galvus, якщо ви приймаєте інші ліки, такі як:
- тіазиди або інші діуретики (їх також називають таблетками для сечовипускання) - кортикостероїди (зазвичай використовуються для лікування запалення)
- ліки для щитовидної залози
- деякі ліки, що впливають на нервову систему.
Попередження Важливо знати, що:
Вагітність та годування груддю
Якщо ви вагітні або годуєте грудьми, думаєте, що можете бути вагітними або плануєте народження дитини, зверніться за порадою до свого лікаря або фармацевта, перш ніж приймати цей препарат.
Не можна використовувати Galvus під час вагітності. Невідомо, чи проникає Galvus у грудне молоко. Не слід використовувати Galvus, якщо ви годуєте грудьми або плануєте годувати грудьми.
Водіння автомобіля та роботу з машинами
Якщо під час прийому Galvus відчувається запаморочення, не керуйте автомобілем та не працюйте з механізмами.
Galvus містить лактозу
Galvus містить лактозу (молочний цукор). Якщо ваш лікар сказав вам, що у вас непереносимість деяких цукрів, зверніться до лікаря, перш ніж приймати цей лікарський засіб.
Доза, спосіб та час введення Як вживати Galvus: Дозування
Завжди приймайте цей препарат точно так, як вам сказав ваш лікар. Якщо є сумніви, зверніться до лікаря або фармацевта.
Скільки брати і коли
Кількість Galvus, яку необхідно прийняти, залежить від індивідуальних умов. Ваш лікар точно скаже вам, скільки таблеток Galvus слід прийняти. Максимальна добова доза становить 100 мг.
Звичайна доза Galvus:
- 50 мг на добу, що приймається одноразово вранці, якщо ви приймаєте Galvus разом з іншим препаратом, який називається сульфонілсечовиною.
- 100 мг на день у вигляді 50 мг вранці та 50 мг ввечері, якщо ви приймаєте Галвус окремо, з іншими ліками під назвою метформін або глітазон, з комбінацією метформіну та сульфонілсечовини або з інсуліном.
- 50 мг на день вранці, якщо у вас помірне або тяжке захворювання нирок або ви перебуваєте на діалізі.
Як приймати Galvus
- Проковтніть таблетки з невеликою кількістю води.
Скільки приймати Galvus
- Приймайте Galvus щодня так довго, як рекомендує ваш лікар. Можливо, вам доведеться продовжувати це лікування протягом тривалого часу.
- Ваш лікар буде регулярно перевіряти ваш стан, щоб переконатися, що лікування дає бажаний ефект.
Якщо ви забули прийняти Галвус
Якщо ви забули прийняти дозу цього препарату, прийміть його, як тільки ви згадаєте. Потім прийміть наступну дозу у звичайний час. Якщо настав час наступної дози, пропустіть пропущену дозу. Не приймайте подвійну дозу, щоб компенсувати пропущену таблетку.
Якщо Ви припините прийом Galvus
Не припиняйте прийом препарату Галвус, якщо вам не скаже ваш лікар. Якщо ви не впевнені, як довго ви будете приймати цей препарат, зверніться до лікаря.
Передозування Що робити, якщо ви прийняли занадто багато Galvus
Якщо ви приймаєте занадто багато таблеток Galvus або якщо хтось інший приймав ваші ліки, негайно зверніться до лікаря. Може знадобитися медична допомога. Якщо вам потрібно відвідати лікаря або відправитися в лікарню, візьміть упаковку з собою.
Побічні ефекти Які побічні ефекти Galvus
Як і всі ліки, цей препарат може викликати побічні ефекти, хоча вони виникають не у всіх.
Деякі симптоми вимагають негайної медичної допомоги:
Ви повинні припинити прийом Galvus і негайно звернутися до лікаря, якщо виникне будь -який з наступних побічних ефектів:
- Ангіоневротичний набряк (рідко: може зачіпати до 1 з 1000 осіб): Симптоми включають набряк обличчя, язика або горла, утруднення ковтання, утруднене дихання, раптову висип або кропив’янку, що може свідчити про реакцію, яка називається «ангіоневротичний набряк».
- Захворювання печінки (гепатит) (рідко): Симптоми включають пожовтіння шкіри та очей, нудоту, втрату апетиту або темну сечу, що може свідчити про захворювання печінки (гепатит).
- Запалення підшлункової залози (панкреатит) (частота невідома). Симптоми включають сильний і постійний біль у животі (область живота), який може поширюватися на спину, а також нудоту та блювоту.
Інші побічні ефекти
Деякі пацієнти відчували такі побічні ефекти під час прийому Галвусу та метформіну:
- Поширені (можуть виникнути до 1 з 10 осіб): тремор, головний біль, запаморочення, нудота, низький рівень глюкози в крові.
- Нечасті (можуть виникнути до 1 з 100 осіб): втома.
Деякі пацієнти відчували такі побічні ефекти під час прийому Galvus та сульфонілсечовини:
- Часто: тремор, головний біль, запаморочення, слабкість, низький рівень глюкози в крові.
- Нечасто: запор.
- Дуже рідко (може виникнути до 1 з 10 000 осіб): біль у горлі, нежить.
Деякі пацієнти відчували такі побічні ефекти під час прийому Galvus та глітазону:
- Поширені: збільшення маси тіла, набряк кистей, щиколоток або стоп (набряк).
- Нечасто: головний біль, слабкість, низький рівень глюкози в крові.
Деякі пацієнти відчували такі побічні ефекти при одночасному застосуванні Galvus:
- Часто: запаморочення.
- Нечасто: головний біль, запор, набряк кистей, щиколоток або стоп (набряк), біль у суглобах, низький рівень глюкози в крові.
- Дуже рідко: біль у горлі, нежить, лихоманка.
Деякі пацієнти відчували такі побічні ефекти під час прийому Galvus, метформіну та сульфонілсечовини:
- Часто: запаморочення, тремор, слабкість, низький рівень глюкози в крові, підвищена пітливість.
Деякі пацієнти відчували такі побічні ефекти під час прийому Galvus та інсуліну (з метформіном або без нього):
- Часто: головний біль, озноб, нудота (нудота), низький рівень глюкози в крові, печія.
- Нечасто: діарея, метеоризм.
Під час маркетингу цього препарату також повідомлялося про такі побічні ефекти:
- Частота невідома (неможливо оцінити за наявними даними): свербляча висипка, запалення підшлункової залози, локальне лущення шкіри або пухирів, біль у м’язах.
Повідомлення про побічні ефекти
Якщо у вас виникли будь -які побічні ефекти, зверніться до свого лікаря, фармацевта або медсестри з діабету. Це включає будь -які можливі побічні ефекти, не зазначені у цій брошурі. Ви також можете повідомити про побічні ефекти безпосередньо за допомогою національної системи повідомлень, наведеної у Додатку V. Повідомляючи про побічні ефекти Ви можете допомогти надати більше інформації про безпеку цього ліки.
Термін придатності та утримання
- Зберігайте цей препарат подалі від очей та недоступного для дітей місця.
- Не використовуйте цей препарат після закінчення терміну придатності, зазначеного на блістері та картонній упаковці після "EXP" / "EXP". Термін придатності відноситься до останнього дня цього місяця.
- Зберігати в оригінальній упаковці для захисту від вологи.
- Не використовуйте упаковку Galvus, яка пошкоджена або має ознаки втручання.
Expiry "> Інші взаємодії
Що містить Galvus
- Діюча речовина - вілдагліптин. Кожна таблетка містить 50 мг вілдагліптину.
- Інші інгредієнти: безводна лактоза, мікрокристалічна целюлоза, натрію крохмальгліколят (тип А) та стеарат магнію.
Опис того, як виглядає Galvus, та вміст пачки
Таблетки Galvus 50 мг - круглі, плоскі, від білого до злегка жовтуватого кольору, з "NVR" з одного боку та "FB" з іншого.
Таблетки Галвус по 50 мг випускаються в упаковках, що містять 7, 14, 28, 30, 56, 60, 90, 112, 180 або 336 таблеток, та у багатоупаковках, що містять 3 коробки, кожна з яких містить 112 таблеток.
Не всі розміри упаковок можуть продаватися у вашій країні.
Джерело з інформацією про упаковку: AIFA (Італійське агентство з лікарських засобів). Вміст, опублікований у січні 2016 р. Наявна інформація може бути не актуальною.
Щоб мати доступ до найновішої версії, бажано зайти на веб-сайт AIFA (Італійське агентство з лікарських засобів). Відмова від відповідальності та корисна інформація.
01.0 НАЗВА ЛЕКАРСТВЕННОГО ПРОДУКТУ -
Таблетки GALVUS 50 мг
02.0 ЯКІСНИЙ І КІЛЬКІСНИЙ СКЛАД -
Кожна таблетка містить 50 мг вілдагліптину.
Допоміжна речовина з відомим ефектом: кожна таблетка містить 47,82 мг лактози (безводний).
Повний список допоміжних речовин див. У розділі 6.1.
03.0 ФАРМАЦЕВТИЧНА ФОРМА -
Планшет.
Кругла (діаметром 8 мм), біла до злегка жовтуватого кольору, плоска таблетка зі скошеними краями.
Букви "NVR" вибиті з одного боку, "FB" з іншого.
04.0 КЛІНІЧНА ІНФОРМАЦІЯ -
04.1 Терапевтичні показання -
Вільдагліптин показаний для лікування цукрового діабету 2 типу у дорослих:
У монотерапії
- у пацієнтів, які не мають належного контролю тільки за допомогою дієти та фізичних вправ, і для яких терапія метформіном є недоцільною через протипоказання або непереносимість.
При подвійній оральній терапії в поєднанні з:
- метформін у пацієнтів з недостатнім контролем глікемії, незважаючи на призначення максимально допустимої дози метформіну окремо,
- сульфонілсечовини у пацієнтів з недостатнім контролем глікемії, незважаючи на введення максимально допустимої дози сульфанілсечовини, і для яких терапія метформіном недоцільна через протипоказання або непереносимість,
- тіазолідиндіон у пацієнтів з недостатнім контролем глікемії і для яких доцільно застосування тіазолідиндіону.
При потрійній пероральній терапії в поєднанні з:
- сульфонілсечовини та метформіну, коли дієта та фізичні вправи, пов’язані з подвійною терапією цими препаратами, не забезпечують належного глікемічного контролю.
Вілдагліптин також призначений для застосування в комбінації з інсуліном (з метформіном або без нього), коли дієта та фізичні вправи у поєднанні зі стабільною дозою інсуліну не забезпечують належного глікемічного контролю.
04.2 Дозування та спосіб введення -
Дозування
Дорослі
При одночасному застосуванні, у комбінації з метформіном, у поєднанні з тіазолідиндіоном, у комбінації з метформіном та сульфонілсечовиною або у комбінації з інсуліном (з метформіном або без нього) рекомендована добова доза вілдагліптину становить 100 мг, що вводиться за одну дозу. 50 мг вранці і доза 50 мг ввечері.
При застосуванні у подвійній терапії в поєднанні з сульфонілсечовиною рекомендована доза вілдагліптину становить 50 мг один раз на день, що вводиться вранці. У цій популяції пацієнтів вілдагліптин у дозі 100 мг на день був не більш ефективним, ніж вілдагліптин у дозі 50 мг один раз на день.
При одночасному застосуванні з сульфонілсечовиною можна зменшити ризик гіпоглікемії, зменшивши дозу сульфонілсечовини.
Дози вище 100 мг не рекомендуються.
Якщо пропущено дозу Galvus, її слід прийняти, як тільки пацієнт це згадає.
Подвійну дозу не слід приймати в той же день.
Безпека та ефективність вілдагліптину як пероральної потрійної терапії у поєднанні з метформіном та тіазолідиндіоном не встановлені.
Додаткова інформація для конкретних груп пацієнтів
Літні люди (≥ 65 років)
У пацієнтів літнього віку корекція дози не потрібна (див. Також розділи 5.1 та 5.2).
Порушення функції нирок
Не потрібно коригувати дозу пацієнтам з легким порушенням функції нирок (оформлення креатинін ≥ 50 мл / хв). Пацієнтам з помірною або тяжкою нирковою недостатністю або термінальною стадією ниркової недостатності (ESRD) рекомендована доза Galvus становить 50 мг 1 раз на день (див. Також розділи 4.4, 5.1 та 5.2).
Порушення функції печінки
Galvus не слід застосовувати пацієнтам з печінковою недостатністю, включаючи пацієнтів, які мають аланінамінотрансферазу (ALT) або аспартатамінотрансферазу (AST)> 3 -кратну верхню межу норми (ULN) до початку лікування (див. Також розділи 4.4 та 5.2).
Педіатричне населення
Застосування Galvus не рекомендується дітям та підліткам (
Спосіб введення
Пероральне застосування
Galvus можна приймати з їжею або без неї (див. Також розділ 5.2).
04.3 Протипоказання -
Підвищена чутливість до активної речовини або до будь -якої з допоміжних речовин, перерахованих у розділі 6.1.
04.4 Спеціальні попередження та відповідні запобіжні заходи при використанні -
Загальні
Galvus не є заміною інсуліну у пацієнтів з інсулінозалежністю. Galvus не слід застосовувати пацієнтам з діабетом 1 типу або для лікування діабетичного кетоацидозу.
Порушення функції нирок
Досвід застосування пацієнтам на гемодіалізі з ШОЕ обмежений, тому цим пацієнтам слід з обережністю застосовувати Galvus (див. Також розділи 4.2, 5.1 та 5.2).
Порушення функції печінки
Galvus не слід застосовувати пацієнтам з печінковою недостатністю, у тому числі пацієнтам, які перед початком лікування мали АЛТ або АСТ> 3-кратну ВГН (див. Також розділи 4.2 та 5.2).
Моніторинг печінкових ферментів
Повідомлялося про рідкісні випадки порушення функції печінки (включаючи гепатит). У цих випадках пацієнти, як правило, протікали безсимптомно, без клінічних наслідків, а показники функції печінки нормалізувалися після припинення лікування. Перед початком лікування препаратом Галвус слід провести аналізи функції печінки, щоб дізнатися вихідну цінність пацієнта. Під час лікування препаратом Галвус слід перевіряти функцію печінки кожні три місяці протягом першого року лікування, а потім періодично. Пацієнти, у яких підвищується рівень трансаміназ, повинні бути перевірені повторною оцінкою функції печінки для підтвердження результатів, а потім повторно проходити часті аналізи функції печінки до тих пір, поки відхилення не прийде в норму. Якщо підвищення АСТ або АЛТ зберігається у 3 рази від верхньої межі норми або вище, рекомендується припинити терапію Галвусом.Пацієнтам, у яких розвинулася жовтяниця або інші ознаки, що свідчать про порушення функції печінки, слід припинити лікування Галвусом.
Після припинення лікування Galvus та нормалізації показників функції печінки лікування Galvus не слід відновлювати.
Серцева недостатність
Клінічне дослідження вілдагліптину у пацієнтів функціональних класів I-III Нью-Йоркської асоціації серця (NYHA) показало, що лікування вілдагліптином не було пов'язане зі зміною функції лівого шлуночка або погіршенням наявної застійної серцевої недостатності (ХСН) порівняно з плацебо. Досвід у пацієнтів III класу функціонального класу NYHA, які отримували лікування вілдагліптином, все ще обмежений, і результати непереконливі (див. розділ 5.1).
Немає досвіду застосування вілдагліптину у клінічних дослідженнях у пацієнтів з IV функціональним класом NYHA, тому його застосування не рекомендується цим пацієнтам.
Шкірні розлади
У неклінічних токсикологічних дослідженнях повідомлялося про ураження шкіри, включаючи пухирі та виразки, на кінцівках мавп (див. Розділ 5.3). Незважаючи на те, що "підвищеної частоти уражень шкіри" у клінічних дослідженнях не спостерігалося, досвід у пацієнтів з діабетичними шкірними ускладненнями був обмежений. Крім того, надходили постмаркетингові повідомлення про бульозні та ексфоліативні ураження шкіри. Відповідно до звичайного догляду за хворим на цукровий діабет рекомендується моніторинг будь -яких шкірних захворювань, таких як пухирі та виразки.
Гострий панкреатит
Застосування вілдагліптину пов'язане з ризиком розвитку гострого панкреатиту. Пацієнтів слід поінформувати про характерні симптоми гострого панкреатиту.
При підозрі на панкреатит слід припинити застосування вілдагліптину; якщо гострий панкреатит підтверджується, вілдагліптин не слід відновлювати. Слід бути обережним у пацієнтів з гострим панкреатитом в анамнезі.
Гіпоглікемія
Відомо, що сульфонілсечовини викликають гіпоглікемію. Пацієнти, які отримують вілдагліптин у поєднанні з сульфонілсечовиною, можуть бути ризиковані гіпоглікемією. Тому для зменшення ризику гіпоглікемії можна розглянути можливість зменшення дози сульфонілсечовини.
Допоміжні речовини
Таблетки містять лактозу. Пацієнти з рідкісними спадковими проблемами непереносимості галактози, дефіциту лактази Лаппа або мальабсорбції глюкози-галактози не повинні приймати цей препарат.
04.5 Взаємодія з іншими лікарськими засобами та інші форми взаємодії -
Вілдагліптин має низький потенціал взаємодії у поєднанні з іншими лікарськими засобами. Оскільки вілдагліптин не є субстратом ферменту цитохрому P (CYP) 450 і не інгібує або не індукує ферменти CYP 450, взаємодія з активними речовинами, які є субстратами, інгібіторами або індукторами цих ферментів, малоймовірна.
Поєднання з піоглітазоном, метформіном та глібенкламідом
Результати досліджень, проведених з цими пероральними антидіабетиками, не виявили клінічно значущих фармакокінетичних взаємодій.
Дигоксин (субстрат p-глікопротеїну), варфарин (субстрат CYP2C9)
Клінічні дослідження, проведені зі здоровими суб’єктами, не виявили клінічно значущих фармакокінетичних взаємодій. Однак цей доказ не був підтверджений у референтній популяції.
Комбінація з амлодипіном, раміприлом, валсартаном або симвастатином
Дослідження взаємодії лікарських засобів з амлодипіном, раміприлом, валсартаном та симвастатином проводили у здорових добровольців. У цих дослідженнях після одночасного застосування з вілдагліптином не спостерігалося клінічно значущих фармакокінетичних взаємодій.
Як і при застосуванні інших пероральних антидіабетиків, гіпоглікемічний ефект вілдагліптину може зменшуватися деякими активними речовинами, включаючи тіазиди, кортикостероїди, препарати щитовидної залози та симпатоміметики.
04.6 Вагітність та годування груддю -
Вагітність
Немає адекватних даних про застосування вілдагліптину вагітним жінкам. Дослідження на тваринах показали репродуктивну токсичність у високих дозах (див. Розділ 5.3). Потенційний ризик для людини невідомий. Через відсутність даних щодо застосування препарату Галвус не слід вагітність.
Час годування
Невідомо, чи виділяється вілдагліптин у жіноче молоко. Дослідження на тваринах показали, що вілдагліптин виводиться з молоком. Galvus не слід застосовувати під час лактації.
Родючість
Досліджень щодо впливу Galvus на фертильність людини не проводилося (див. Розділ 5.3).
04.7 Вплив на здатність керувати автомобілем та працювати з механізмами -
Досліджень щодо здатності керувати транспортними засобами та працювати з механізмами не проводилося.Пацієнтам, які відчувають запаморочення як побічну реакцію, слід уникати керування транспортними засобами та роботи з механізмами.
04.8 Побічні ефекти -
Короткий опис профілю безпеки
Дані про безпеку були отримані від загальної кількості 3784 пацієнтів, які отримували щоденні дози вілдагліптину 50 мг (один раз на день) або 100 мг (50 мг двічі на день або 100 мг один раз на день) у контрольованих дослідженнях тривалістю щонайменше 12 тижнів. З цих пацієнтів 2264 отримували лише вілдагліптин, а 1520 - вілдагліптин у поєднанні з іншими ліками. 2682 пацієнта отримували 100 мг вілдагліптину щодня (50 мг двічі на день або 100 мг один раз на день), а 1102 пацієнтам - 50 мг вілдагліптину 1 раз на добу.
Більшість побічних реакцій у цих клінічних випробуваннях мали легкий та минущий характер і не вимагали припинення терапії. Не було зв’язку між побічними реакціями та віком, етнічною приналежністю, тривалістю впливу або добовою дозою.
Повідомлялося про рідкісні випадки порушення функції печінки (включаючи гепатит). У цих випадках пацієнти, як правило, протікали безсимптомно, без клінічних наслідків, а показники функції печінки нормалізувалися після припинення лікування. З даних контрольних монотерапії або додаткових досліджень тривалістю до 24 тижнів, частота підвищення рівня АЛТ або АСТ у ≥ 3 рази перевищує верхню межу норми (класифікується як присутня принаймні у 2 послідовних контролях або під час останнього відвідування під час лікування) становив 0,2%, 0,3% та 0,2% для вілдагліптину 50 мг 1 раз на добу, вілдагліптину 50 мг 2 рази на день та всіх порівняльників відповідно. Ці підвищення рівня трансаміназ, як правило, були безсимптомними, непрогресуючими та не пов’язаними з холестазом або жовтяницею.
Повідомлялося про поодинокі випадки ангіоневротичного набряку при застосуванні вілдагліптину з частотою, подібною до контрольної групи.Більшість випадків повідомлялося про одночасне застосування вілдагліптину в комбінації з інгібітором ферменту ангіотензину (інгібітор АПФ). Більшість подій були середнього ступеня тяжкості і зникали під час лікування вілдагліптином.
Таблиця побічних реакцій
Побічні реакції, про які повідомлялося у пацієнтів, які отримували Galvus у подвійних сліпих дослідженнях як монотерапію та додаткову терапію, наведені нижче для кожного показника за класом системних органів та абсолютною частотою. Частоти визначаються як дуже поширені (≥1 / 10), загальні (≥1 / 100,
Поєднання з метформіном
Таблиця 1 Побічні реакції, про які повідомлялося у пацієнтів, які отримували Galvus 100 мг щодня у комбінації з метформіном у подвійних сліпих дослідженнях (N = 208)
Опис окремих побічних реакцій
У контрольованих клінічних випробуваннях, проведених із комбінацією вілдагліптину 100 мг на добу + метформіну, не повідомлялося про відміну через побічні реакції ні у групі вілдагліптину у дозі 100 мг на добу + метформіну, ні у групі плацебо + метформіну. У клінічних дослідженнях частота гіпоглікемії була часто зустрічається у пацієнтів, які отримували вілдагліптин у дозі 100 мг на день у поєднанні з метформіном (1%), і нечасто у пацієнтів, які отримували плацебо + метформін (0,4%). Не повідомлялося про серйозні гіпоглікемічні події на групі застосування вілдагліптину.
У клінічних дослідженнях вага не змінювався від вихідного рівня, коли до метформіну додавали 100 мг вілдагліптину щодня (+0,2 кг та -1,0 кг для вілдагліптину та плацебо відповідно).
Клінічні дослідження, що тривали більше 2 років, не показали жодних додаткових сигналів щодо безпеки або непередбачених ризиків при поєднанні вілдагліптину з метформіном.
Поєднання з сульфонілсечовиною
Таблиця 2 Побічні реакції, повідомлені у пацієнтів, які отримували 50 мг Galvus у поєднанні з сульфонілсечовиною у подвійних сліпих дослідженнях (N = 170)
Опис окремих побічних реакцій
У контрольованих клінічних випробуваннях із комбінацією вілдагліптину 50 мг + сульфонілсечовини загальна частота відміни через побічні реакції становила 0,6% у групі вілдагліптину 50 мг + сульфонілсечовини проти 0% у групі, яка отримувала плацебо + сульфонілсечовину.
У клінічних дослідженнях, коли до глімепіриду додавали вілдагліптин у дозі 50 мг один раз на день, частота гіпоглікемії становила 1,2% проти 0,6% при застосуванні плацебо + глімепіриду.
У клінічних дослідженнях маса не змінювалася від вихідної, коли до глімепіриду додавали 50 мг вілдагліптину щодня (-0,1 кг та -0,4 кг для вілдагліптину та плацебо відповідно).
Асоціація з тіазолідиндіоном
Таблиця 3 Побічні реакції, зареєстровані у пацієнтів, які отримували Galvus 100 мг на день у поєднанні з тіазолідиндіоном у подвійних сліпих дослідженнях (N = 158)
Опис окремих побічних реакцій
У контрольованих клінічних випробуваннях із комбінацією вілдагліптин 100 мг на добу + тіазолідиндіон, як у групах вілдагліптіну по 100 мг на добу + тіазолідиндіон, так і в групі плацебо + тіазолідиндіон не повідомлялося про відміну через побічні реакції. У клінічних дослідженнях частота гіпоглікемії була нечасто у пацієнтів, які отримували вілдагліптин + піоглітазон (0,6%), тоді як це було часто у пацієнтів, які отримували плацебо + піоглітазон (1,9%). Не повідомлялося про серйозні гіпоглікемічні події на групі застосування вілдагліптину. У додаткових дослідженнях з піоглітазоном абсолютний приріст ваги при застосуванні плацебо та Galvus у дозі 100 мг на день становив 1,4 та 2,7 кг відповідно.
Частота периферичних набряків при додаванні 100 мг вілдагліптину щодня до фонової терапії піоглітазоном у максимальній дозі (45 мг один раз на день) становила 7,0% порівняно з 2,5% лише для піоглітазону.
Монотерапія
Таблиця 4 Побічні реакції, зареєстровані у пацієнтів, які отримували Galvus по 100 мг на добу як монотерапію у подвійних сліпих дослідженнях (N = 1855)
Опис окремих побічних реакцій
Крім того, у контрольованих клінічних випробуваннях, які проводилися з застосуванням вілдагліптину окремо, загальна частота відміни через побічні реакції не була вищою для пацієнтів, які отримували вілдагліптин у дозі 100 мг на день (0,3%) порівняно з пацієнтами, які отримували плацебо (0,6%) або порівняльний засіб ( 0,5%).
У порівняльних контрольованих дослідженнях монотерапії гіпоглікемія була рідкістю і була зареєстрована у 0,4% (7 з 1855) пацієнтів, які отримували вілдагліптин у дозі 100 мг на добу, порівняно з 0,2% (2 з 1082) пацієнтів у групах активного порівняння або плацебо, при цьому немає повідомлялося про серйозні або серйозні події.
У клінічних дослідженнях вага не змінювався від вихідного рівня, коли вілдагліптин у дозі 100 мг на добу застосовувався як монотерапія (-0,3 кг та -1,3 кг для вілдагліптину та плацебо відповідно).
Комбінація з метформіном та сульфонілсечовиною
Таблиця 5 Побічні реакції, про які повідомлялося у пацієнтів, які отримували Galvus 50 мг двічі на день у поєднанні з метформіном та сульфонілсечовиною (N = 157)
Опис окремих побічних реакцій
Не було відміни препарату через побічні реакції, про які повідомлялося у групі лікування вілдагліптином + метформіном + глімепіридом, порівняно з 0,6% у групі плацебо + метформіну + глімепіриду.
Частота гіпоглікемії була загальною в обох групах лікування (5,1% для групи вілдагліптину + метформіну + глімепіриду проти 1,9% для групи плацебо + метформіну + глімепіриду).
У групі вілдагліптину повідомлялося про одну важку гіпоглікемічну подію.
Наприкінці дослідження вплив на середню масу тіла був нейтральним (+0,6 кг у групі вілдагліптину та -0,1 кг у групі плацебо).
Асоціація з інсуліном
Таблиця 6 Побічні реакції, зареєстровані у пацієнтів, які отримували Galvus по 100 мг на день у поєднанні з інсуліном (з метформіном або без нього) у подвійних сліпих дослідженнях (N = 371)
Опис окремих побічних реакцій
У контрольованих клінічних випробуваннях з комбінацією вілдагліптину 50 мг двічі на день плюс інсулін, з супутнім метформіном або без нього, загальна частота відміни через побічні реакції становила 0,3% у групі лікування вілдагліптином. У групі плацебо не було відміни.
Частота гіпоглікемії була подібною в обох групах лікування (14,0% у групі вілдагліптину проти 16,4% у групі плацебо). У двох пацієнтів у групі вілдагліптину та у 6 пацієнтів у групі плацебо спостерігалися серйозні гіпоглікемічні події.
Наприкінці дослідження вплив на середню масу тіла був нейтральним (+0,6 кг від вихідного рівня у групі вілдагліптину та без зміни маси у групі плацебо).
Досвід постмаркетингу
Таблиця 7 Постмаркетингові побічні реакції
Повідомлення про підозрювані побічні реакції
Повідомлення про підозрювані побічні реакції, що виникають після реєстрації лікарського засобу, є важливими, оскільки вони дозволяють постійно контролювати співвідношення користі / ризику лікарського засобу. Медичних працівників просять повідомляти про будь -які підозрювані побічні реакції через національну систему звітності.
04.9 Передозування -
Інформація про передозування вілдагліптину обмежена.
Симптоми
Інформація про ймовірні симптоми передозування була отримана з дослідження переносимості збільшення дози у здорових добровольців, які отримували Galvus протягом 10 днів. У дозі 400 мг було три випадки м’язового болю та окремі випадки легкої та минущої парестезії, лихоманки, набряку та тимчасового підвищення рівня ліпази. При дозі 600 мг у одного суб’єкта розвинувся набряк у стопах і руках і підвищився рівень креатинфосфокінази (CPK), аспартатамінотрансферази (AST), креативного білка (CRP) та міоглобіну. У трьох інших пацієнтів виник набряк стопи, у двох випадках - парестезія. Усі симптоми та лабораторні відхилення усуваються без лікування після припинення досліджуваного препарату.
Лікування
У разі передозування рекомендується підтримуюче лікування. Вільдагліптин неможливо видалити гемодіалізом. Однак основний метаболіт, що походить від гідролізу (LAY 151), можна усунути шляхом гемодіалізу.
05.0 ФАРМАКОЛОГІЧНІ ВЛАСТИВОСТІ -
05.1 "Фармакодинамічні властивості -
Фармакотерапевтична група: Препарати, що застосовуються при діабеті, інгібітори дипептидилпептидази 4 (DPP-4), код ATC: A10BH02
Вільдагліптин відноситься до класу препаратів, що модулюють острівці підшлункової залози, і є потужним і селективним інгібітором ДПП-4.
Механізм дії
Введення вілдагліптину призводить до швидкого та повного пригнічення активності ДПП-4, що призводить до збільшення ендогенного рівня голодування та постпрандіального вживання GLP-1 (глюкагоноподібний пептид-1) та GIP (глюкозозалежний інсулінотропний поліпептид).).
Фармакодинамічні ефекти
Збільшуючи ендогенні рівні інкретинів, вілдагліптин підвищує чутливість бета-клітин до глюкози, що призводить до поліпшення глюкозозалежної секреції інсуліну. Лікування вілдагліптином по 50-100 мг на день у пацієнтів з діабетом 2 типу значно покращило i маркер функція бета -клітин, включаючи HOMA -b (оцінка моделі гомеостазу -b), співвідношення проінсуліну до інсуліну та показники чутливості бета -клітин у тесті на толерантність до їжі при частому відборі проб. У пацієнтів без діабету (нормальний рівень глюкози в крові) вілдагліптин не стимулює секрецію інсуліну та не знижує рівень глюкози.
Підвищуючи рівень ендогенного GLP-1, вілдагліптин також підвищує чутливість альфа-клітин до глюкози, що призводить до адекватної секреції глюкагону для кількості глюкози.
Збільшення співвідношення інсулін / глюкагон при гіперглікемії, спричинене збільшенням рівня інкретину, призводить до зменшення вироблення глюкози в печінці натще та після їжі, що призводить до зниження рівня глюкози в крові.
Відомий ефект підвищення рівня GLP-1, що уповільнює спорожнення шлунка, не спостерігається під час лікування вілдагліптином.
Клінічна ефективність та безпека
Понад 15 000 пацієнтів з цукровим діабетом 2 типу брали участь у подвійних сліпих плацебо- або активних контрольованих клінічних випробуваннях з тривалістю лікування більше 2 років. У цих дослідженнях вілдагліптин вводили більш ніж 9000 пацієнтам у добових дозах 50 мг один раз на день, 50 мг двічі на день або 100 мг один раз на день. Більше 5000 пацієнтів чоловічої статі та більше 4000 жінок отримували вілдагліптин у дозі 50 мг 1 раз на добу або 100 мг на добу. Більше 1900 пацієнтів, які отримували вілдагліптин у дозі 50 мг один раз на день або 100 мг на день, були у віці ≥ 65 років. У цих дослідженнях вілдагліптин призначався як монотерапія пацієнтам з цукровим діабетом 2 типу, які не отримували лікарські засоби, або в комбінації з пацієнтами, які не отримували належного контролю з іншими протидіабетичними препаратами. продуктів.
В цілому, вілдагліптин покращив глікемічний контроль при одночасному застосуванні або при застосуванні в комбінації з метформіном, сульфонілсечовиною та тіазолідиндіоном, що відображається клінічно значущим зниженням «HbA1c від вихідного рівня»кінцева точка дослідження (див. таблицю 8).
У клінічних дослідженнях величина зниження HbA1c при застосуванні вілдагліптину була більшою у пацієнтів з вищими вихідними значеннями HbA1c.
У 52-тижневому подвійному сліпому контрольованому дослідженні вілдагліптин (50 мг двічі на день) знизив вихідний рівень HbA1c на -1% порівняно з -1,6%, досягнутим при застосуванні метформіну (з титруванням до 2 г / добу). Статистичної неповноцінності не отримано при лікуванні вілдагліптином повідомлялося про значно меншу частоту побічних реакцій з боку шлунково -кишкового тракту, ніж при лікуванні метформіном.
У 24-тижневому подвійному сліпому контрольованому дослідженні вілдагліптин (50 мг двічі на день) порівнювали з розиглітазоном (8 мг один раз на день). У пацієнтів із середнім вихідним рівнем HbA1c 8,7% середнє зниження становило -1,20% при застосуванні вілдагліптину та -1,48% при застосуванні розиглітазону. У пацієнтів, які отримували розиглітазон, спостерігалося середнє збільшення ваги (+1,6 кг), тоді як у тих, хто отримував вілдагліптин, не спостерігалося збільшення маси тіла (-0,3 кг). Частота периферичних набряків була нижчою у групі вілдагліптину, ніж у групі росиглітазону (2,1% проти 4,1% відповідно).
У 2-річному клінічному дослідженні вілдагліптин (50 мг двічі на день) порівнювали з гліклазидом (до 320 мг на добу). Через два роки середнє зниження HbA1c становило -0,5% для вілдагліптину та -0,6% для гліказиду порівняно із середнім вихідним рівнем HbA1c на 8,6%. Статистичної неповноцінності не досягнуто. Вілдагліптин асоціювався з меншою кількістю випадків гіпоглікемії (0,7%), ніж гліказид (1,7%).
У 24-тижневому клінічному дослідженні вілдагліптин (50 мг двічі на день) порівнювали з піоглітазоном (30 мг один раз на день) у пацієнтів, які не отримували належного контролю за метформіном (середня добова доза: 2020 мг). Порівняно з вихідним показником HbA1c на 8,4%, середнє зниження становило -0,9% при застосуванні вілдагліптину в поєднанні з метформіном та -1,0% при застосуванні піоглітазону в поєднанні з метформіном. спостерігалося порівняно з +0,3 кг, що спостерігалося у тих, хто отримував вілдагліптин у комбінації з метформіном.
У 2-річному клінічному дослідженні вілдагліптин (50 мг двічі на день) порівнювали з глімепіридом (до 6 мг / добу-2-річна середня доза: 4,6 мг) у пацієнтів, які отримували метформін (середня добова доза: 1894 мг). Через 1 рік середнє зниження HbA1c становило -0,4% при застосуванні вілдагліптину в комбінації з метформіном та -0,5% при застосуванні глімепіриду в поєднанні з метформіном порівняно із середнім вихідним рівнем HbA1c 7,3%. Зміна маси тіла становила -0,2 кг з вілдагліптином порівняно з +1,6 кг з глімепіридом. Частота гіпоглікемії була значно нижчою у групі вілдагліптину (1,7%), ніж у групі глімепіриду (16,2%). Наприкінці дослідження (2 роки) в обох групах лікування було виявлено, що HbA1c подібний до вихідних значень зміни маси тіла та відмінності в гіпоглікемії зберігалися.
У 52-тижневому дослідженні вілдагліптин (50 мг двічі на день) порівнювали з гліклазидом (середня добова доза: 229,5 мг) у пацієнтів, які не отримували належного контролю за метформіном (вихідна доза метформіну 1928 мг / добу). Через 1 рік середнє зниження HbA1c становило -0,81% при застосуванні вілдагліптину у поєднанні з метформіном (середній вихідний рівень HbA1c 8,4%) та -0,85% при застосуванні гліклазиду у поєднанні з метформіном (середній вихідний рівень HbA1c 8,5%)); досягнуто статистичної неповноцінності (95% ДІ: -0,11 -0,20). Зміна маси тіла становила +0,1 кг при застосуванні вілдагліптину порівняно із збільшенням ваги +1,4 кг при застосуванні гліклазиду.
Ефективність фіксованої комбінації вілдагліптину та метформіну (поступово титрується до дози 50 мг / 500 мг двічі на день або 50 мг / 1000 мг двічі на день) у ході терапії оцінювали у 24-тижневому дослідженні. denovo).
HbA1c знижувався на -1,82% при застосуванні вілдагліптину / метформіну 50 мг / 1000 мг двічі на день, на -1,61% при застосуванні вілдагліптину / метформіну 50 мг / 500 мг двічі на день, на -1, 36% при застосуванні метформіну 1000 мг двічі на день та -1,09 % з 50 мг вілдагліптину двічі на день, починаючи з середнього вихідного рівня HbA1c 8,6%. ≥10,0% було більш помітним.
Було проведено 24-тижневе, подвійне сліпе, рандомізоване, багатоцентрове, плацебо-контрольоване дослідження для оцінки ефекту лікування вілдагліптину у дозі 50 мг 1 раз на добу порівняно з плацебо у 515 пацієнтів з діабетом 2 типу та нирковою недостатністю. Середній (N = 294) або тяжкий (N = 221). 68,8% та 80,5% пацієнтів з помірною та тяжкою нирковою недостатністю відповідно отримували лікування інсуліном (середня добова доза 56 одиниць та 51,6 одиниць відповідно) на початку лікування. У пацієнтів з помірною нирковою недостатністю вілдагліптин значно зменшив HbA1c порівняно з плацебо (різниця -0,53%) від середнього вихідного рівня 7,9%. У пацієнтів з тяжкою нирковою недостатністю вілдагліптин значно знизив HbA1c порівняно з плацебо (різниця -0,56% ) починаючи з середнього базового рівня 7,7%.
24-тижневе, рандомізоване, подвійне сліпе, плацебо-контрольоване дослідження було проведено у 318 пацієнтів для оцінки ефективності та безпеки вілдагліптину (50 мг двічі на день) у поєднанні з метформіном (≥1500 мг на день) та глімепіридом (≥4 мг) щоденно). Вільдагліптин у поєднанні з метформіном та глімепіридом значно знизив HbA1c порівняно з плацебо
Середнє зниження HbA1c, скориговане плацебо, із середнього вихідного рівня 8,8% становило -0,76%.
24-тижневе рандомізоване подвійне сліпе плацебо-контрольоване дослідження було проведено у 449 пацієнтів для оцінки ефективності та безпеки вілдагліптину (50 мг двічі на день) у поєднанні зі стабільною дозою базального або попередньо змішаного інсуліну (середня добова доза 41 одиниць) з одночасним застосуванням метформіну (N = 276) або без супутнього застосування метформіну (N = 173). Вілдагліптин у комбінації з інсуліном значно знижує HbA1c порівняно з плацебо. У загальній популяції середнє зниження HbA1c, скориговане плацебо, із середнього вихідного рівня HbA1c на 8,8% становило -0,72%. У підгрупах, які отримували інсулін з супутнім метформіном або без нього, середнє плацебо -скориговане зниження HbA1c становило -0,63% та -0,84% відповідно. Частота гіпоглікемії у загальній популяції становила 8,4% та 7,2% у групах вілдагліптину та плацебо відповідно.
В іншому 24-тижневому дослідженні у пацієнтів з більш просунутим діабетом 2 типу, які не отримували належного контролю над інсуліном (коротка і тривала дія, середня доза інсуліну 80 МО / добу), середнє зниження HbA1c, коли вілдагліптин (50 мг двічі на день), було статистично і значно більше, ніж при застосуванні плацебо + інсуліну (0,5% проти 0,2%). Частота гіпоглікемії була нижчою у групі вілдагліптину, ніж у групі плацебо (22,9% проти 29,6%).
52-тижневе, багатоцентрове, рандомізоване, подвійне сліпе дослідження було проведено у пацієнтів з діабетом 2 типу та застійною серцевою недостатністю (функціональний клас I-III за NYHA) для оцінки ефекту вілдагліптину 50 мг двічі на день (N = 128) у порівнянні з плацебо (N = 126) на фракції викиду лівого шлуночка (LVEF). Вільдагліптин не асоціюється зі зміною функції лівого шлуночка або погіршенням наявної ХСН. Порушення серцево-судинної системи були загалом збалансованими. У пацієнтів із серцевою недостатністю III класу за NYHA при застосуванні вілдагліптину було більше серцевих подій, ніж у пацієнтів, які отримували плацебо.Однак у вихідному серцево -судинному ризику на користь плацебо були зміщення, а кількість подій була низькою, що виключало остаточні висновки. %) від значення середнє вихідне значення - 7,8% на 16 тижні. У підгрупі III класу NYHA зниження HbA1c було меншим (різниця 0,3%), але цей висновок обмежений через невелику кількість пацієнтів (N = 44). Частота гіпоглікемії в загальній популяції становила 4,7% та 5,6% у групах вілдагліптину та плацебо відповідно.
Серцево -судинний ризик
Був проведений мета-аналіз 25 клінічних випробувань фази III тривалістю понад 2 роки, незалежно від того, чи були передбачені перспективні серцево-судинні події. Цей аналіз показав, що лікування вілдагліптином не асоціювалося з підвищеним серцево -судинним ризиком порівняно з порівняннями. Комбінована кінцева точка підтверджених серцево -судинних та цереброваскулярних подій (CCV) [гострий коронарний синдром (ACS), транзиторна ішемічна атака (з ознаками серцевого нападу на знімках), інсульт або смерть від CCV] була подібною для вілдагліптину порівняно з комбінацією порівняння активний і плацебо [Коефіцієнт ризику Мантеля-Хаенцеля 0,84 (95% довірчий інтервал 0,63-1,12)]. В цілому 99 із 8 956 пацієнтів у групі вілдагліптину повідомили про подію проти 91 із 6061 пацієнта у групі порівняння.
Таблиця 8 Ключові результати ефективності вілдагліптину в плацебо-контрольованій монотерапії та додаткових дослідженнях (первинна ефективність у популяції ІТТ- намір лікувати)
Педіатричне населення
Європейське агентство з лікарських засобів скасувало зобов’язання надсилати результати досліджень з вілдагліптином у всіх підгрупах педіатричної популяції з цукровим діабетом 2 типу (див. Розділ 4.2 для інформації про застосування у педіатрії).
05.2 "Фармакокінетичні властивості -
Поглинання
Після перорального прийому натщесерце вілдагліптин швидко всмоктується, причому максимальна концентрація у плазмі крові настає через 1,7 години. Їжа дещо затримує (2,5 години) час досягнення пікової концентрації в плазмі, але не змінює загальної експозиції (AUC). Введення вілдагліптину разом з їжею призводить до зниження Cmax (19%). L Однак ступінь зміни не є є клінічно значущим, тому Galvus можна приймати незалежно від їжі. Абсолютна біодоступність становить 85%.
Розповсюдження
Зв’язування вілдагліптину з білками плазми крові низьке (9,3%), і вілдагліптин рівномірно розподіляється між плазмою та еритроцитами крові. Після внутрішньовенного введення середній об'єм розподілу вілдагліптину алло стаціонарний стан (Vss) - 71 літр, що свідчить про позасудинний розподіл.
Біотрансформація
У людей метаболізм є основним шляхом елімінації вілдагліптину і становить 69% дози. Основний метаболіт (LAY 151) є фармакологічно неактивним і є продуктом гідролізу групи ціано і становить 57% дози, а потім за допомогою глюкуроніду (BQS867) та продуктів гідролізу аміду (4% дози). Дані в пробірці на мікросомах нирок людини свідчить про те, що нирка може бути одним із основних факторів, що сприяють гідролізу вілдагліптину до його основного неактивного метаболіту, ЛАЙ 151. DPP-4 частково сприяє гідролізу вілдагліптину згідно з дослідженням в природних умовах проводили з використанням щурів, вільних від DPP-4. Вілдагліптин не метаболізується в кількісній мірі ферментами CYP 450. Отже, не очікується, що одночасний прийом інгібіторів CYP 450 та / або індукторів лікарського засобу впливає на метаболічний кліренс вілдагліптину. в пробірці продемонстрували, що вілдагліптин не інгібує / не індукує ферменти CYP 450. Тому вілдагліптин, ймовірно, не впливає на метаболічний кліренс лікарських засобів, що метаболізуються за допомогою CYP 1A2, CYP 2C8, CYP 2C9, CYP 2C19, CYP 2D6, CYP 2E1 або CYP 3A4 / 5, при одночасному введенні.
Ліквідація
Після перорального введення [14С] вілдагліптину приблизно 85% дози виводиться із сечею, а 15% дози виводиться з калом. Після перорального застосування ниркова екскреція незміненого вілдагліптину становить 23% дози. У здорових осіб після внутрішньовенного введення оформлення загальні плазмові та ниркові значення вілдагліптину становлять 41 та 13 л / год відповідно. Після внутрішньовенного введення середній період напіввиведення становить приблизно 2 год. Після перорального введення період напіввиведення становить приблизно 3 години.
Лінійність / Нелінійність
В межах діапазону терапевтичних доз Cmax вілдагліптину та площа під кривою концентрація-час у плазмі крові (AUC) збільшуються приблизно пропорційно дозі.
Конкретні групи пацієнтів
Секс
Клінічно значущих відмінностей у фармакокінетиці вілдагліптину не спостерігалося між здоровими чоловіками та жінками у "широкому діапазоні віку та індексу маси тіла (ІМТ). Інгібування DPP-4 вілдагліптином не впливає" від статі.
Літні громадяни
У здорових людей похилого віку (≥ 70 років) загальна експозиція вілдагліптину (100 мг один раз на день) збільшилася на 32% із збільшенням максимальної концентрації у плазмі крові на 18% порівняно зі здоровими молодими людьми (18 Однак ці зміни не враховуються Клінічно значуще. Вік не впливає на інгібування ДПП-4 вілдагліптином.
Порушення функції печінки
Вплив печінкової недостатності на фармакокінетику вілдагліптину вивчали у пацієнтів з легкою, помірною та тяжкою печінковою недостатністю, виходячи з бала Чайлда-П’ю (у діапазоні від 6 для легкого до 12 для важкого) у порівнянні зі здоровими пацієнтами. при легкій та помірній печінковій недостатності, вплив вілдагліптину після одноразової дози зменшується (на 20%та 8%відповідно), тоді як для пацієнтів з тяжкою печінковою недостатністю вплив вілдагліптину збільшується на 22%. Максимальна зміна (зменшення або збільшення ) експозиція вілдагліптину становить ≥30%, що не вважається клінічно значущим. Не існує кореляції між тяжкістю захворювання печінки та змінами експозиції вілдагліптину.
Порушення функції нирок
Було проведено відкрите багаторазове дослідження для оцінки фармакокінетики нижчої терапевтичної дози вілдагліптину (50 мг один раз на день) у пацієнтів з різним ступенем хронічної ниркової недостатності, що визначається кліренсом креатиніну (легкий: від 50 до
Вільдагліптин видалявся шляхом гемодіалізу в обмеженій мірі (3% протягом 3-4-годинного сеансу гемодіалізу, починаючи через 4 години після введення дози).
Етнічні групи
Обмежені дані свідчать про те, що раса не має значного впливу на фармакокінетику вілдагліптину.
05.3 Доклінічні дані про безпеку -
Затримки внутрішньосерцевої імпульсної провідності спостерігалися у собак з дозою без ефекту 15 мг / кг (в 7 разів більше експозиції на людину на основі Cmax).
У щурів та мишей спостерігалося скупчення пінистих альвеолярних макрофагів у легенях. Доза без ефекту становила 25 мг / кг (у 5 разів більша за експозицію людини на основі AUC) у щурів та 750 мг / кг (у 142 разів перевищувала експозицію на людину) у мишей. Шлунково -кишкові симптоми, особливо м’який стілець, мукоїдний стілець, діарея та у вищих дозах кров у калі спостерігалися у собак. Рівень без ефекту не встановлено.
У звичайних дослідженнях генотоксичності в пробірці І в природних умовах вілдагліптин не був мутагенним. У щурів дослідження фертильності та раннього ембріонального розвитку не показали, що вілдагліптин спричиняє порушення фертильності, репродуктивної здатності або раннього ембріонального розвитку. Ембріонально-фетальну токсичність оцінювали у щурів та кроликів. У щурів спостерігалося збільшення захворюваності плаваючими ребрами у зв’язку зі зменшенням параметрів маси тіла матері, при цьому доза без ефекту 75 мг / кг (у 10 разів перевищувала вплив людини). У кроликів зменшилася маса плода та зміни скелета, що свідчать про затримку розвитку, спостерігалися лише за наявності тяжкої токсичності для матері, при дозі без ефекту 50 мг / кг (в 9 разів перевищувала вплив на людину). лише у зв’язку з токсичністю для матері при ≥ 150 мг / кг, включаючи тимчасове зниження маси тіла та зниження рухової активності у поколінні F1.
Дворічне дослідження канцерогенності на щурах проводилося з пероральними дозами до 900 мг / кг (приблизно в 200 разів більше експозиції на людину при максимальній рекомендованій дозі). Збільшення захворюваності на пухлини, пов’язані з вілдагліптином, не спостерігалося. Ще 2-річне дослідження канцерогенності проводилося на мишах з пероральними дозами до 1000 мг / кг. Спостерігалося збільшення захворюваності на аденокарциноми молочної залози. Гемангіосаркоми без ефектів 500 мг / кг (59 разів перевищує вплив на людину) та 100 мг / кг (16 разів перевищує опромінення людини) відповідно. Підвищена захворюваність цими пухлинами у мишей не вважалася значною загрозою для людини через відсутність генотоксичності вілдагліптину та його основного метаболіту, розвиток пухлин у одного виду і все. .
Під час 13-тижневого токсикологічного дослідження у мавп cynomolgus повідомлялося про ураження шкіри при дозах ≥ 5 мг / кг / добу. Поразки послідовно локалізувалися на кінцівках (кисті, стопи, вуха та хвіст). У дозі 5 мг / кг / добу (приблизно еквівалентно AUC людини після впливу дози 100 мг) спостерігали лише везикули. Вони погіршилися, незважаючи на продовження лікування, і не були пов'язані з гістопатологічними відхиленнями. При дозах ≥ 20 мг / кг / добу (приблизно в 3 рази більше AUC у людини після впливу дози 100 мг) відзначалося лущення та лущення шкіри, струпів та хвороб хвороб з відповідними гістопатологічними змінами. Некротичні ураження хвоста спостерігалися при дозах ≥ 80 мг / кг / добу.
Протягом 4-тижневого періоду відновлення пошкодження шкіри не регресували у мавп, які отримували 160 мг / кг / день.
06.0 ФАРМАЦЕВТИЧНА ІНФОРМАЦІЯ -
06.1 допоміжні речовини -
Безводна лактоза
Мікрокристалічна целюлоза
Гліколят натрію крохмалю (тип А)
Стеарат магнію
06.2 Несумісність "-
Не актуально.
06.3 Строк дії "-
3 роки
06.4 Особливі умови зберігання -
Зберігати в оригінальній упаковці для захисту від вологи.
06.5 Характер безпосередньої упаковки та вміст упаковки -
Алюміній / алюмінієвий блістер (PA / Al / PVC // Al)
Випускається в упаковках, що містять 7, 14, 28, 30, 56, 60, 90, 112, 180 або 336 таблеток, і в багатоупаковках, що містять 336 (3 упаковки по 112) таблеток.
Не всі розміри упаковок можна продавати.
06.6 Інструкції з використання та поводження -
Ніяких спеціальних вказівок.
07.0 ВЛАСНИК "РОЗРОБНИЦТВА"
Novartis Europharm Limited
Бізнес -парк Фрімлі
Camberley GU16 7SR
Великобританія
08.0 НОМЕР РОЗВИТКУ З РОБОТИ
ЄС / 1/07/414 / 001-010
ЄС/1/07/414/018
038144010
038144022
038144034
038144046
038144059
038144061
038144073
038144085
038144097
038144109
038144186
09.0 ДАТА ПЕРШОГО ДОЗВІЛЕННЯ АБО ОНОВЛЕННЯ ДОЗВІЛА -
Дата першого дозволу: 26 вересня 2007 року
Дата останнього оновлення: 26 вересня 2012 року
10.0 ДАТА ПЕРЕГЛЯДУ ТЕКСТУ -
D.CCE, квітень 2015 р