Діючі речовини: Левоцетиризин (Левоцетиризин дигідрохлорид)
Ксизал 5 мг таблетки, вкриті оболонкою
Пакети Xyzal доступні для розмірів упаковки:- Ксизал 5 мг таблетки, вкриті оболонкою
- Ксизал 5 мг / мл пероральні краплі, розчин
- Ксізал 0,5 мг / мл пероральний розчин
Чому використовується Xyzal? Для чого це?
Діючою речовиною Xyzal є левоцетиризину дигідрохлорид.
Ксізал - протиалергічний препарат.
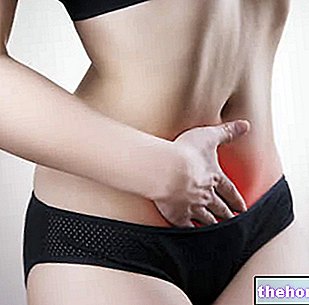
Для лікування ознак захворювання (симптомів), пов'язаних з:
- алергічний риніт (включаючи стійкий алергічний риніт);
- хронічна кропив’янка (хронічна ідіопатична кропив’янка).
Протипоказання Коли Ксизал не слід застосовувати
Не приймайте Ксізал
- якщо у вас алергія (гіперчутливість) до левоцетиризину дигідрохлориду або до антигістамінного засобу або до будь -якого іншого інгредієнта препарату Ксизал (див. "Що містить Ксизал").
- якщо у вас тяжка ниркова недостатність (тяжка ниркова недостатність з кліренсом креатиніну нижче 10 мл / хв). .
Заходи безпеки при застосуванні Що потрібно знати, перш ніж приймати Ксизал
Будьте особливо обережні з Xyzal
Застосування Ксизалу дітям до 6 років не рекомендується, оскільки таблетки, вкриті плівковою оболонкою, не дозволяють коригувати дозу.
Зверніться до лікаря за порадою, якщо ви, ймовірно, не зможете спорожнити сечовий міхур (при таких станах, як: травма спинного мозку або збільшення простати).
Взаємодії Які препарати або продукти харчування можуть змінити дію Ксизалу
Прийом з іншими лікарськими засобами
Повідомте свого лікаря або фармацевта, якщо ви приймаєте або нещодавно приймали інші ліки, включаючи ліки, відпущені без рецепта.
Прийом Xyzal з їжею та напоями
Рекомендується обережність, якщо Xyzal приймається разом з алкоголем.
У чутливих пацієнтів одночасний прийом цетиризину або левоцетиризину та алкоголю чи інших речовин із центральною дією може спричинити вплив на центральну нервову систему, хоча було показано, що цетиризин рацемічний не посилює дію цетиризину.
Попередження Важливо знати, що:
Вагітність та годування груддю
Попросіть поради у свого лікаря або фармацевта, перш ніж приймати будь -які ліки. Повідомте лікаря, якщо ви вагітні, намагаєтесь завагітніти або годуєте грудьми.
Водіння автомобіля та роботу з машинами
Деякі пацієнти можуть відчувати сонливість / сонливість, втому та втому після лікування Ксизалом. Рекомендується бути обережним під час керування транспортними засобами та роботи з механізмами, поки ви не дізнаєтесь про вплив цього препарату на Вашу людину. Однак специфічні тести, проведені на здорових добровольцях, однак не виявили жодного зниження пильності, здатності до реакції чи здатності впоратися. левоцетиризину у рекомендованій дозі.
Важлива інформація про деякі інгредієнти Xyzal
Таблетки містять лактозу; якщо лікар сказав вам, що у вас «непереносимість деяких цукрів, зверніться до лікаря перед прийомом цього ліки.
Доза, спосіб та час введення Як застосовувати Xyzal: дозування
Завжди приймайте Ксизал точно так, як вам сказав ваш лікар. Якщо є сумніви, зверніться до лікаря або фармацевта.
Дози:
Звичайна доза для дорослих та дітей віком від 6 років - одна таблетка на день.
Спеціальні вказівки щодо дози для конкретних груп населення:
Пацієнтам з порушеною функцією нирок може бути призначена менша доза відповідно до тяжкості захворювання нирок, а у дітей дозу вибиратимуть на основі маси тіла; дозу визначає лікар.
Пацієнтам з тяжкою нирковою недостатністю не слід приймати Ксизал.
Пацієнтам, які мають лише порушення функції печінки, слід приймати звичайну призначену дозу.
Пацієнтам, у яких одночасно знижена функція печінки та нирок, може бути призначена менша доза залежно від тяжкості захворювання нирок, а у дітей дозу також вибиратимуть на основі маси тіла; дозу визначає лікар.
Таблетки Xyzal не рекомендуються дітям до 6 років.
Пацієнтам літнього віку не потрібно коригувати дозу, якщо їхня функція нирок нормальна.
Як і коли слід приймати Ксизал?
Таблетки слід ковтати цілими, запиваючи водою, і їх можна приймати з їжею або без неї.
Передозування Що робити, якщо ви прийняли занадто багато Xyzal
Якщо ви прийняли більше Ксизалу, ніж слід
Прийом більшої кількості препарату Ксизал, ніж це необхідно, може викликати сонливість у дорослих. Спочатку діти можуть проявляти збудження та неспокій, а потім сонливість.
Якщо ви вважаєте, що вжили занадто багато Xyzal, повідомте свого лікаря, який вирішить, які дії необхідно вжити
Якщо ви забули прийняти Ксизал
Якщо ви забули прийняти Ксизал або прийняти меншу дозу, ніж призначено лікарем, не приймайте подвійну дозу, щоб компенсувати пропущену таблетку; просто почекайте до запланованого часу для наступної дози та прийміть свою звичайну дозу, як це призначив ваш лікар.
Якщо Ви припините прийом Ксизалу
Не очікується, що припинення лікування матиме будь -які побічні ефекти. Симптоми можуть з’явитися знову, але не повинні бути більш серйозними, ніж були до початку лікування. Якщо у вас виникнуть додаткові запитання щодо застосування цього ліки, зверніться до лікаря або фармацевта.
Побічні ефекти Які побічні ефекти від застосування Ксизалу
Як і всі ліки, Ксизал може викликати побічні ефекти, хоча вони виникають не у всіх.
Поширені: можуть вразити до 1 з 10 пацієнтів
Сухість у роті, головний біль, втома та сонливість / сонливість.
Нечасто: може вразити до 1 з 100 пацієнтів
Втома і біль у животі.
Невідомо: частоту неможливо оцінити за наявними даними
Повідомлялося про інші побічні ефекти, такі як серцебиття, почастішання серцебиття, судоми, поколювання, запаморочення, непритомність, тремор, дисгевзія (зміна відчуття смаку), відчуття обертання або руху, порушення зору, помутніння зору, біль або утруднення сечовипускання ., неможливість повністю спорожнити сечовий міхур, набряк, свербіж, висип, кропив’янка (набряк, почервоніння та свербіж шкіри), висип, задишка, збільшення ваги, біль у м’язах, агресивна чи збуджена поведінка, галюцинації, депресія, безсоння, тривоги або повторювані суїцидальні думки, гепатит, порушення функції печінки, блювота, підвищений апетит і нудота.
Припиніть прийом Xyzal при перших ознаках реакції гіперчутливості та негайно зверніться до лікаря.Симптоми реакції гіперчутливості можуть включати: набряк рота, язика, обличчя та / або горла, утруднене дихання або ковтання (стиснення грудей або хрипи) вулики, раптове падіння артеріального тиску, що може призвести до колапсу або шоку, що може привести до летального результату.
Якщо будь -який з побічних ефектів стає серйозним, або якщо Ви помітили будь -які побічні ефекти, не зазначені у цій інструкції, повідомте про це свого лікаря або фармацевта.
Термін придатності та утримання
Зберігайте Xyzal у недоступному для дітей місці.
Не використовуйте Xyzal після закінчення терміну придатності, зазначеного на внутрішній етикетці та коробці після EXP. Термін придатності відноситься до останнього дня цього місяця.
Цей лікарський засіб не вимагає особливих умов зберігання
Склад і лікарська форма
Що містить Ксизал
- Діюча речовина - 5 мг левоцетиризину дигідрохлориду
Кожна таблетка, вкрита плівковою оболонкою, містить 5 мг левоцетиризину дигідрохлориду.
- Допоміжні інгредієнти: целюлоза мікрокристалічна, моногідрат лактози, безводний колоїдний кремнезем, стеарат магнію, гіпромелоза (E464), діоксид титану (E171) та макрогол 400.
Як виглядає Ксизал та вміст упаковки
Таблетки, вкриті плівковою оболонкою, білі до майже білі, овальні, з логотипом Y на одній стороні. Вони поставляються в блістерах по 1, 2, 4, 5, 7, 10, 2 x 10, 10 x 10, 14, 15, 20, 21, 28, 30, 40, 50, 60, 70, 90 і 100 таблеток . Не всі розміри упаковок можна продавати. Джерело з інформацією про упаковку: AIFA (Італійське агентство з лікарських засобів). Вміст, опублікований у січні 2016 р. Наявна інформація може бути не актуальною.
Щоб мати доступ до найновішої версії, бажано зайти на веб-сайт AIFA (Італійське агентство з лікарських засобів). Відмова від відповідальності та корисна інформація.
01.0 НАЗВА ЛЕКАРСТВЕННОГО ПРОДУКТУ
XYZAL
02.0 ЯКІСНИЙ І КІЛЬКІСНИЙ СКЛАД
Кожна таблетка, вкрита плівковою оболонкою, містить 5 мг левоцетиризину дигідрохлориду.
Допоміжні речовини: 63,50 мг лактози моногідрату / таблетка
Повний список допоміжних речовин див. У розділі 6.1.
03.0 ФАРМАЦЕВТИЧНА ФОРМА
Планшет, вкритий плівковою оболонкою.
Білий до майже білого кольору, овальна таблетка, вкрита плівковою оболонкою, з логотипом Y на одній стороні.
04.0 КЛІНІЧНА ІНФОРМАЦІЯ
04.1 Терапевтичні показання
Симптоматичне лікування алергічного риніту (включаючи стійкий алергічний риніт) та хронічної ідіопатичної кропив’янки.
04.2 Дозування та спосіб введення
Таблетки слід приймати перорально і ковтати цілими за допомогою рідини. Їх можна приймати з їжею або без неї. Рекомендується приймати добову дозу за один прийом.
Дорослі та підлітки від 12 років
Рекомендована добова доза становить 5 мг (1 таблетка, вкрита плівковою оболонкою).
Літні громадяни
Рекомендується коригування дози пацієнтам літнього віку з помірною або тяжкою нирковою недостатністю (див. "Пацієнти з нирковою недостатністю" нижче).
Діти віком від 6 до 12 років
Рекомендована добова доза становить 5 мг (1 таблетка, вкрита плівковою оболонкою).
Для дітей у віці від 2 до 6 років коригування дози неможливо у формі таблеток, вкритих плівковою оболонкою. Тому рекомендується застосування дитячого складу левоцетиризину.
Пацієнти з нирковою недостатністю
Частоту дозування слід базувати на функції нирок. Щоб змінити дозування, зверніться до таблиці нижче. Для використання таблиці слід звернутись до значення кліренсу креатиніну пацієнта (CLcr) у мл / хв. Значення CLcr (мл / хв) можна визначити з рівня креатиніну в сироватці крові (мг / дл) за такою формулою:
Коригування дози для пацієнтів з нирковою недостатністю:
У педіатричних пацієнтів з нирковою недостатністю дозу необхідно коригувати індивідуально з урахуванням ниркового кліренсу та маси тіла пацієнта. Специфічних даних щодо дітей з нирковою недостатністю немає.
Пацієнти з печінковою недостатністю
Коригування дози лише пацієнтам з печінковою недостатністю не потрібне. У випадку пацієнтів з печінковою та нирковою недостатністю необхідно коригувати дозування (див. "Пацієнти з нирковою недостатністю" вище).
Тривалість лікування
Переривчастий алергічний риніт (симптоми проявляються менше 4 днів на тиждень або тривають менше 4 тижнів) необхідно лікувати відповідно до захворювання та його історії; лікування можна припинити, коли симптоми зникнуть, і можна розпочати знову, коли симптоми з’являться знову. У разі стійкого алергічного риніту (симптоми спостерігаються більше 4 днів на тиждень і більше 4 тижнів) пацієнту може бути запропонована безперервна терапія протягом періоду впливу алергенів.
Наразі є клінічні дані про лікування до 6 місяців для таблеток, вкритих оболонкою, левоцетиризину 5 мг. Клінічні дані про рацемічне лікування доступні протягом одного року у пацієнтів з хронічною кропив’янкою та хронічним алергічним ринітом.
04.3 Протипоказання
Підвищена чутливість до левоцетиризину, до інших похідних піперазину або до будь -якої з допоміжних речовин.
Левоцетиризин протипоказаний пацієнтам з тяжкою нирковою недостатністю з кліренсом креатиніну менше 10 мл / хв.
Пацієнти з рідкісними спадковими проблемами непереносимості галактози, дефіцитом лактази Лаппа або мальабсорбцією глюкози-галактози не повинні приймати цей препарат.
04.4 Спеціальні попередження та відповідні запобіжні заходи щодо використання
Застосування таблеток, вкритих плівковою оболонкою, дітям до шести років не рекомендується, оскільки ця форма не дозволяє належним чином коригувати дозу. Рекомендується використовувати дитячу форму левоцетиризину.
Не рекомендується введення левоцетиризину немовлятам та дітям до 2 років.
При вживанні алкоголю рекомендується бути обережним (див. "Взаємодія").
04.5 Взаємодія з іншими лікарськими засобами та інші форми взаємодії
Не проводились дослідження взаємодії з левоцетиризином (включаючи дослідження з індукторами CYP3A4); Дослідження, проведені з рацемічним цетиризином, продемонстрували відсутність клінічно значущих несприятливих взаємодій (з псевдоефедрином, циметидином, кетоконазолом, еритроміцином, азитроміцином, гліпізидом та діазепамом). У дослідженні з повторною дозою з теофіліном (400 мг 1 раз на добу) незначне зменшення спостерігався кліренс цетиризину (16%), тоді як одночасне застосування цетиризину не впливало на доступність теофіліну.
Наявність їжі не зменшує ступінь всмоктування левоцетиризину, хоча зменшує його швидкість.
У чутливих пацієнтів одночасний прийом цетиризину або левоцетиризину та алкоголю чи інших заспокійливих засобів з боку ЦНС може спричинити вплив на центральну нервову систему, хоча було доведено, що цетиризин -рацемік не посилює дію алкоголю на ЦНС.
04.6 Вагітність та період лактації
Для левоцетиризину відсутні клінічні дані про вагітність, що зазнала впливу.
Дослідження на тваринах не вказують на прямий чи опосередкований шкідливий вплив на вагітність, ембріональний / внутрішньоутробний розвиток, пологи чи постнатальний розвиток.
Слід бути обережним при призначенні лікарського засобу вагітним або годуючим жінкам.
04.7 Вплив на здатність керувати автомобілем та працювати з механізмами
Порівняльні клінічні дослідження не виявили жодних доказів того, що левоцетиризин у рекомендованій дозі знижує пильність, чуйність або здатність керувати автомобілем.
Однак у деяких пацієнтів під час лікування левоцетиризином можуть спостерігатися сонливість, втома та астенія. Тому пацієнти, яким потрібно керувати автомобілем, займатися потенційно небезпечною діяльністю або працювати з механізмами, повинні враховувати індивідуальну реакцію на ліки.
04.8 Побічні ефекти
Під час досліджень терапевтичної активності, проведених на чоловіках та жінках у віці від 12 до 71 року, у 15,1% пацієнтів, які отримували 5 мг левоцетиризину, спостерігалася принаймні одна побічна реакція на лікарські засоби порівняно з 11,3% у групі пацієнтів з плацебо. У 91,6% пацієнтів випадки, побічні реакції були легкими та помірними.
У клінічних дослідженнях відсоток пацієнтів, яким довелося припинити лікування через побічні ефекти, становив 1,0% (9/935) з 5 мг левоцетиризину та 1,8% (14/771) з плацебо.
У клінічних терапевтичних випробуваннях з левоцетиризином брали участь 935 пацієнтів, які зазнали впливу препарату у рекомендованій дозі 5 мг на день. Нижче наведено частоту побічних реакцій на ліки, виявлених у цих пацієнтів з відсотком, що дорівнює або перевищує 1% (часто:> 1/100,
Спостерігалися й інші нечасті побічні реакції (нечасто:> 1/1000, біль у животі.
Частота седативних побічних реакцій на лікарські засоби, таких як сонливість, втома та астенія, була загалом частіше (8,1%) після лікування 5 мг левоцетиризину, ніж із плацебо (3,1%).
На додаток до побічних реакцій клінічних випробувань, перерахованих вище, у постмаркетинговому досвіді повідомлялося про дуже рідкісні випадки побічних реакцій, наведені нижче.
Порушення з боку імунної системи: гіперчутливість, включаючи анафілаксію.
Психічні розлади: агресія, збудження.
Порушення з боку нервової системи: судоми.
З боку очей: порушення зору.
З боку серця: серцебиття.
Дихальні, грудні та середостінні порушення: задишка.
Шлунково -кишкові розлади: нудота.
Гепатобіліарні порушення: гепатит.
З боку шкіри та підшкірної клітковини: ангіоневротичний набряк, фіксоване висипання препарату, свербіж, висип, кропив’янка.
З боку опорно -рухового апарату та сполучної тканини: міалгія.
Дослідження: збільшення ваги, порушення функції печінки.
04.9 Передозування
Симптоми
Симптоми передозування можуть включати сонливість у дорослих та спочатку збудження та неспокій, а потім сонливість у дітей.
Лікування передозування
Специфічного антидоту левоцетиризину немає.
У разі передозування рекомендується симптоматичне або підтримуюче лікування. Промивання шлунка слід розглядати, якщо пройшло короткий час після прийому всередину. Гемодіаліз неефективний для усунення левоцетиризину.
05.0 ФАРМАКОЛОГІЧНІ ВЛАСТИВОСТІ
05.1 Фармакодинамічні властивості
Фармакотерапевтична група: антигістамінні препарати для системного застосування, похідне піперазину, код АТС: R06A E09
Левоцетиризин, (R) енантіомер цетиризину, є потужним і селективним антагоністом периферичних рецепторів Н1.
Дослідження зв'язування показали, що левоцетиризин має високу спорідненість до рецепторів Н1 людини (Ki = 3,2 нмоль / л). Спорідненість левоцетиризину вдвічі більше, ніж цетиризину (Ki = 6,3 нмоль / л). Левоцетиризин дисоціює від рецепторів Н1 з періодом напіввиведення 115 ± 38 хв.
Після одноразового введення левоцетиризин демонструє зайнятість рецепторів 90% через 4 години та 57% через 24 години.
Фармакодинамічні дослідження, проведені на здорових добровольцях, показали, що левоцетиризин проявляє «активність, порівнянну з цетиризином, у шкірі та носі, але удвічі меншою дозою.
Фармакодинамічну активність левоцетиризину вивчали у рандомізованих контрольованих дослідженнях: у дослідженні, яке порівнювало вплив левоцетиризину 5 мг, дезлоратадину 5 мг та плацебо на гістамінові та еритеми, лікування левоцетиризином порівняно з плацебо та дезлоратадином призвело до значного зменшення утворення пухирців та еритеми, яке було найвищим у перші 12 годин і тривало протягом 24 годин (p
Початок дії 5 мг левоцетиризину для контролю симптомів, викликаних пилком, спостерігався через 1 годину після прийому препарату у плацебо-контрольованих дослідженнях у моделі камери стимуляції алергену.
Дослідження in vitro (методи камери Бойдена та клітинного шару) показали, що левоцетиризин пригнічує езотаксин-індуковану трансендотеліальну міграцію еозинофілів як у дермі, так і в легеневій тканині. В експериментальному фармакодинамічному дослідженні в природних умовах (методика шкірної камери) у 14 дорослих пацієнтів протягом перших 6 годин реакції, спричиненої пилком, було показано три основні інгібуючі ефекти левоцетиризину 5 мг у порівнянні з плацебо: інгібування вивільнення VCAM-1, модуляція проникності судин та зниження залучення еозинофілів.
Ефективність та безпека левоцетиризину були продемонстровані у кількох подвійних сліпих плацебо-контрольованих клінічних дослідженнях у дорослих пацієнтів із сезонним алергічним ринітом, цілорічним алергічним ринітом або персистуючим алергічним ринітом. Показано, що левоцетиризин значно покращує симптоми. перешкоди в деяких дослідженнях.
6-місячне клінічне дослідження за участю 551 дорослого пацієнта (у тому числі 276 пацієнтів, які отримували левоцетиризин), що страждають на стійкий алергічний риніт (симптоми спостерігаються 4 дні на тиждень щонайменше 4 тижні поспіль) та сенсибілізувалося до кліщів домашнього пилу та пилку трави, показало, що левоцетиризин 5 мг був клінічно та статистично значно ефективнішим, ніж плацебо, у покращенні загальної оцінки симптомів алергічного риніту протягом усього періоду дослідження без будь -якої тахіфілаксії.
Безпеку та ефективність таблеток левоцетиризину у дітей вивчали у двох плацебо-контрольованих клінічних випробуваннях, які включали пацієнтів віком від 6 до 12 років із сезонним та цілорічним алергічним ринітом відповідно. В обох дослідженнях левоцетиризин значно покращив симптоми та підвищив якість життя.
У плацебо-контрольованому клінічному дослідженні, що включало 166 пацієнтів з хронічною ідіопатичною кропив’янкою, 85 пацієнтів отримували плацебо та 81 пацієнт-5 мг левоцетиризину 1 раз на добу протягом 6 тижнів. Результатом лікування левоцетиризином стало значне зниження інтенсивності свербіння протягом першого тижня та протягом усього періоду лікування порівняно з плацебо. Левоцетиризин також спричинив значне поліпшення відповідної якості життя порівняно з плацебо. Здоров'я, оцінене на основі дерматології Індекс якості життя.
Фармакокінетичний / фармакодинамічний зв’язок
Дія на шкірні реакції, викликані гістаміном, не корелює з концентрацією у плазмі крові.
Аналіз ЕКГ не виявив помітних ефектів левоцетиризину на інтервал QT.
05.2 Фармакокінетичні властивості
Фармакокінетика левоцетиризину лінійна і не залежить від дози та часу, з низькою мінливістю між суб’єктами. Фармакокінетичний профіль однаковий при застосуванні як окремого енантіомеру або як цетиризину.
Хіральна інверсія не відбувається під час процесів абсорбції та елімінації.
Поглинання
Левоцетиризин, що вводиться перорально, швидко і широко всмоктується. Максимальна концентрація у плазмі крові досягається через 0,9 години після введення. Рівні рівноважного стану досягаються через два дні лікування. Після одноразового або багаторазового введення 5 мг один раз на день досягається середня максимальна концентрація 270 нг / мл та 308 нг / мл відповідно. Ступінь всмоктування не залежить від дози і не залежить від прийому їжі, але пікова концентрація зменшується і затримується.
Розповсюдження
Немає даних про розподіл тканин у людей або про проходження левоцетиризину через гематоенцефалічний бар’єр. У щурів та собак найвищі рівні тканин були виявлені в печінці та нирках, найнижчий у ЦНС. Левоцетиризин на 90% зв’язується з білки плазми Розподіл левоцетиризину обмежений, на що вказує об’єм розподілу, який становить 0,4 л / кг.
Біотрансформація
У людей ступінь метаболізму левоцетиризину становить менше 14% дози; тому вважається, що відмінності, які можуть виникнути після генетичного поліморфізму або одночасного прийому інгібіторів ферментів, є незначними. Метаболічні шляхи включають ароматичне окислення, N- та O-деалкілування та кон’югацію з таурином. Шляхи деалкілування переважно опосередковуються CYP 3A4, тоді як різні та / або невпізнані ізоформи CYP вступають у гру для ароматичного окислення. Левоцетиризин не змінює активність ізоферментів CYP 1A2, 2C9, 2C19, 2D6, 2E1 і 3A4 у концентраціях, що значно перевищують максимальну концентрацію, досягнуту після перорального введення 5 мг.
Тому поганий метаболізм та відсутність гальмівного потенціалу на метаболізмі роблять взаємодію левоцетиризину з іншими речовинами малоймовірною, або навпаки.
Ліквідація
Період напіввиведення з плазми у дорослих становив 7,9 ± 1,9 години. Середній видимий загальний кліренс тіла становив 0,63 мл / хв / кг. Основним шляхом виведення левоцетиризину та метаболітів є сеча, через яку в середньому 85,4% введеної дози усувається. Середня фекальна екскреція становила лише 12,9% дози.
Порушення функції нирок
Очевидний кліренс левоцетиризину в організмі корелює з кліренсом креатиніну.
Тому рекомендується коригувати інтервал між дозами левоцетиризину, виходячи з кліренсу креатиніну, у пацієнтів з помірною або тяжкою нирковою недостатністю. У суб’єктів із термінальною стадією анурії ниркової недостатності загальний кліренс організму знижується приблизно на 80% порівняно з нормальні предмети. Кількість левоцетиризину, що виводиться за стандартний 4-годинний цикл гемодіалізу, становила менше 10%.
05.3 Дані доклінічної безпеки
Неклінічні дані не показують особливої небезпеки для людини на основі звичайних досліджень фармакологія безпеки, токсичність при повторних дозах, генотоксичність, канцерогенний потенціал, репродуктивна токсичність.
06.0 ФАРМАЦЕВТИЧНА ІНФОРМАЦІЯ
06.1 Допоміжні речовини
Ядро
Мікрокристалічна целюлоза
Моногідрат лактози
Безводний колоїдний кремнезем
Стеарат магнію
Покриття
OpadryÒ Y-1-7000 складається з:
Гіпромелоза (E464)
Діоксид титану (E171)
Макрогол 400.
06.2 Несумісність
Не актуально.
06.3 Строк дії
4 роки.
06.4 Особливі умови зберігання
Цей лікарський засіб не вимагає особливих умов зберігання.
06.5 Характер безпосередньої упаковки та вміст упаковки
Алюмінієвий блістер - OPA / алюміній / ПВХ
Упаковки по 1, 2, 4, 5, 7, 10, 2 x 10, 10 x 10, 14, 15, 20, 21, 28, 30, 40, 50, 60, 70, 90, 100 таблеток.
Не всі розміри упаковок можна продавати.
06.6 Інструкції з використання та поводження
Ніяких спеціальних вказівок.
07.0 ВЛАСНИК РОЗРОБНИЦТВА
UCB Pharma S.p.A.
Via Gadames 57,
20151 Мілан
08.0 НОМЕР РОЗВИТКУ З РОБОТИ
AIC n. 035666229 / М - упаковка з 1 таблеткою
AIC n. 035666231 / М - упаковка з 2 таблеток
AIC n. 035666015 / М - упаковка з 4 таблеток
AIC n. 035666243 / М - упаковка з 5 таблеток
AIC n. 035666027 / М - упаковка з 7 таблеток
AIC n. 035666039 / М - упаковка з 10 таблеток
AIC n. 035666041 / М - упаковка 2 х 10 таблеток
AIC n. 035666054 / М - упаковка 10 х 10 таблеток
AIC n. 035666066 / М - упаковка з 14 таблеток
AIC n. 035666078 / М - упаковка з 15 таблеток
AIC n. 035666080 / М - упаковка з 20 таблеток
AIC n. 035666092 / М - упаковка з 21 таблеткою
AIC n. 035666104 / М - упаковка з 28 таблеток
AIC n. 035666116 / М - упаковка з 30 таблеток
AIC n. 035666128 / М - упаковка з 40 таблеток
AIC n. 035666130 / М - коробка з 50 таблеток
AIC n. 035666142 / М - упаковка з 60 таблеток
AIC n. 035666155 / М - упаковка з 70 таблеток
AIC n. 035666167 / М - упаковка з 90 таблеток
AIC n. 035666179 / М - упаковка по 100 таблеток
09.0 ДАТА ПЕРШОГО ДОЗВІЛЕННЯ АБО ОНОВЛЕННЯ ДОЗВІЛЛЯ
27 травня 2003 року
Поновлення: лютий 2006 року
10.0 ДАТА ПЕРЕГЛЯНУ ТЕКСТУ
02/10/2010













.jpg)