Діючі речовини: Аванафіл
Spedra 50 мг таблетки
Пакети Spedra доступні для упаковок:- Spedra 50 мг таблетки
- ДОСТАВКА таблеток по 100 мг
- СПЕДРА таблетки 200 мг
Чому використовується Spedra? Для чого це?
Діюча речовина у складі Spedra називається аванафіл і належить до групи лікарських засобів, які називаються інгібіторами фосфодіестерази типу 5 (ФДЕ5).
Спедра застосовується для лікування дорослих чоловіків, які страждають на еректильну дисфункцію (також відому як імпотенція), тобто неможливість досягти або зберегти ерекцію, придатну для сексуальної активності.
Спедра діє, допомагаючи кровоносним судинам статевого члена розширюватися; збільшений приплив крові до статевого члена допомагає йому залишатися жорстким і ерегтованим під час сексуального збудження. Spedra не лікує вашу дисфункцію.
Важливо зауважити, що Spedra працює лише за умови сексуальної стимуляції. Вам і вашому партнерові все одно доведеться використовувати прелюдію для підготовки до статевого акту, так само як і вам, якщо вона не приймала ніяких ліків. Spedra не допоможе вам, якщо у вас немає еректильної дисфункції.
Спедра не є ліками для жінок.
Протипоказання При застосуванні Спедри не слід
Не приймайте Спедра:
- якщо у вас алергія на аванафіл або будь -який інший інгредієнт цього препарату (перерахований у розділі 6);
- якщо ви приймаєте нітратні ліки від болю в грудях (стенокардію), такі як амілітрит або нітрогліцерин. Спедра може посилити дію цих ліків і серйозно знизити артеріальний тиск;
- якщо ви приймаєте ліки від ВІЛ або СНІДу, такі як ритонавір, індинавір, саквінавір, нелфінавір або атазанавір;
- якщо ви приймаєте ліки від грибкових інфекцій, такі як кетоконазол, ітраконазол або вориконазол, або деякі антибіотики проти бактеріальних інфекцій, такі як кларитроміцин або телітроміцин;
- якщо у вас серйозні проблеми з серцем;
- якщо ви перенесли інсульт або інфаркт протягом останніх 6 місяців;
- якщо у вас низький кров'яний тиск або високий кров'яний тиск, які не контролюються ліками;
- якщо у вас болить грудна клітка (стенокардія) або біль виникає під час статевого акту
- якщо у вас серйозна проблема з печінкою або нирками;
- якщо ви втратили зір на одне око через хворобу (неартеріальна ішемічна оптична нейропатія [NAION]), яка зменшує кількість крові в оці;
- якщо інші люди у вашій родині мають серйозні проблеми з очима (наприклад, пігментний ретиніт);
- якщо ви наймаєте riociguat. Цей препарат використовується для лікування легеневої артеріальної гіпертензії (тобто високого кров’яного тиску в легенях) та хронічної тромбоемболічної легеневої гіпертензії (тобто високого кров’яного тиску в легенях через тромбів). Було показано, що інгібітори PDE5 посилюють гіпотензивну дію цього препарату. Якщо ви приймаєте ріоцигуат або не впевнені, зверніться до лікаря.
Не приймайте Spedra, якщо що -небудь із зазначеного вище стосується Вас. Якщо ви не впевнені, поговоріть зі своїм лікарем або фармацевтом, перш ніж приймати Spedra.
Заходи безпеки при застосуванні Що потрібно знати, перш ніж приймати Спедру
Поговоріть зі своїм лікарем або фармацевтом, перш ніж приймати Spedra:
- якщо у вас проблеми з серцем. Для вас може бути ризикованим статевий акт;
- якщо у вас "пріапізм", тобто "стійка ерекція, що триває 4 години і більше (це може статися у чоловіків з такими захворюваннями, як серповидноклітинна анемія, множинна мієлома або лейкемія);
- якщо у вас є відхилення у формі вашого пеніса (наприклад, кут нахилу, хвороба Пейроні або кавернозний фіброз);
- якщо у вас є порушення кровотечі або активна виразкова хвороба.
Якщо що -небудь з вищезазначеного стосується вас, поговоріть зі своїм лікарем або фармацевтом, перш ніж приймати Spedra. Якщо є сумніви, зверніться до лікаря або фармацевта.
Проблеми зі зором або слухом
Деякі чоловіки, які приймають такі ліки, як «Спедра», мали проблеми із зором або слухом (докладніше див. «Серйозні побічні ефекти» у розділі 4). Невідомо, чи є ці проблеми безпосередньо спричинені застосуванням Спедри, іншими супутніми захворюваннями або набір факторів.
Діти та підлітки
Діти та підлітки віком до 18 років не повинні приймати Спедру.
Взаємодії Які препарати або продукти харчування можуть змінити дію Spedra
Повідомте свого лікаря або фармацевта, якщо ви приймаєте, нещодавно приймали або могли б приймати будь -які інші ліки, оскільки Спедра може вплинути на дію деяких із них. Деякі інші ліки також можуть вплинути на дію Спедри.
Зокрема, повідомте свого лікаря та не приймайте Спедру, якщо ви приймаєте нітратні ліки від болю в грудях (стенокардію), такі як амілітрит або нітрогліцерин. Спедра посилює дію цих ліків і серйозно знижує артеріальний тиск. Також не приймайте Spedra, якщо ви приймаєте ліки від ВІЛ або СНІДу, такі як ритонавір, індинавір, саквінавір, нелфінавір або атазанавір або ліки від грибкових інфекцій, такі як кетоконазол, ітраконазол або вориконазол або деякі антибіотики для бактеріальних інфекцій, такі як кларитроміцин або телітроміцин (див. початок розділу 2 «Не приймайте Спедру»).
Повідомте свого лікаря або фармацевта, якщо ви приймаєте будь -яке з наступних ліків:
- так звані альфа-адреноблокатори, при проблемах з простатою або для зниження високого кров'яного тиску;
- ліки для нерегулярного серцебиття ("аритмія"), такі як хінідин, прокаїнамід, аміодарон або соталол;
- антибіотики для інфекцій, таких як еритроміцин;
- фенобарбітал або примідон при епілепсії;
- карбамазепін, для епілепсії, для стабілізації настрою або для певних видів болю;
- інші ліки, які можуть зменшити метаболізм спедри в організмі ("помірні інгібітори CYP3A4"), включаючи ампренавір, апрепітант, дилтіазем, флуконазол, фосампренавір та верапаміл;
- riociguat.
Не використовуйте Spedra разом з іншими засобами еректильної дисфункції, такими як силденафіл, тадалафіл або варденафіл.
Якщо що -небудь з вищезазначеного стосується вас, поговоріть зі своїм лікарем або фармацевтом, перш ніж приймати Spedra. Якщо є сумніви, зверніться до лікаря або фармацевта.
Спедра з напоями та алкоголем
Грейпфрутовий сік може збільшити вплив препарату, тому його слід уникати протягом 24 годин після прийому Спедри. Вживання алкоголю разом із прийомом Спедри може збільшити частоту серцевих скорочень і знизити тиск.Ви можете відчувати запаморочення (особливо стоячи) і головний біль або відчувати, як серце б’ється в грудях (серцебиття). Вживання алкоголю також може зменшити вашу здатність до «ерекції».
Попередження Важливо знати, що:
Родючість
Spedra не впливає на рухливість або форму сперматозоїдів після одноразових пероральних доз 200 мг у здорових добровольців.
На даний момент немає даних про розвиток сперми у здорових дорослих та дорослих, які страждають на легку еректильну дисфункцію.
Водіння автомобіля та роботу з машинами
Спедра може викликати запаморочення або погіршити зір. Якщо це сталося, не керуйте автомобілем, не їздіть на велосипеді та не користуйтесь інструментами та механізмами.
Доза, спосіб та час введення Спосіб застосування Spedra: Дозування
Завжди приймайте цей препарат точно так, як вам сказав ваш лікар. Якщо є сумніви, зверніться до лікаря або фармацевта.
Рекомендована доза - одна таблетка 100 мг за необхідності. Не приймайте Spedra частіше одного разу на день. Скажіть своєму лікарю, якщо ви вважаєте, що Спедра занадто сильна або занадто слабка. Він може запропонувати вам перейти на іншу дозу ліків. Коригування дози може також знадобитися при одночасному застосуванні Spedra з іншими ліками. Якщо ви приймаєте такі ліки, як еритроміцин, ампренавір, апрепітант, дилтіазем, флуконазол, фосампренавір та верапаміл ("помірні інгібітори CYP3A"), рекомендована доза Шпедри становить одну таблетку 100 мг з інтервалом не менше 2 днів між прийомами .
Приймайте Spedra приблизно за 30 хвилин до статевого акту. Пам’ятайте, що Spedra допоможе вам досягти ерекції лише за умови сексуальної стимуляції.
Спедри можна приймати з їжею або без неї; при прийомі з їжею дія може тривати довше.
Передозування Що робити, якщо ви передозували Spedra
Якщо ви приймаєте занадто багато препарату Спедра, негайно повідомте про це лікаря. Це може мати більше побічних ефектів, ніж зазвичай, і вони можуть бути більш серйозними.
Якщо у Вас виникнуть додаткові запитання щодо застосування препарату Спедра, зверніться до свого лікаря або фармацевта.
Побічні ефекти Які побічні ефекти у Spedra
Як і всі ліки, цей препарат може викликати побічні ефекти, хоча вони виникають не у всіх.
Серйозні побічні ефекти
Припиніть прийом Spedra і негайно зверніться до лікаря, якщо ви помітили будь -який із наведених нижче серйозних побічних ефектів (можливо, вам знадобиться термінове лікування):
- "ерекція, яка не зникає (" пріапізм "). Якщо у вас" ерекція, яка триває більше 4 годин, вам потрібно якомога швидше її вилікувати, інакше ваш пеніс може бути пошкоджений протягом тривалого періоду часу (у т.ч. неможливість досягти ерекції);
- затуманений зір;
- раптове зниження або втрата зору на одне або обидва ока;
- раптове зниження або втрата слуху (іноді ви також можете відчувати запаморочення або дзвін у вухах).
Припиніть прийом Spedra і негайно зверніться до лікаря, якщо помітите будь -який із серйозних побічних ефектів, зазначених вище.
Інші побічні ефекти включають:
Поширені (можуть виникнути до 1 з 10 осіб)
- головний біль;
- припливи;
- закладеність носа.
Нечасті (можуть виникнути у 1 з 100 осіб)
- запаморочення
- сонливість або втома;
- закладеність пазух;
- біль у спині;
- припливи;
- задишка під час фізичних навантажень;
- змінене серцебиття на електрокардіограмі (ЕКГ);
- почастішання пульсу;
- прискорене серцебиття (серцебиття);
- порушення травлення, відчуття болю в животі;
- затуманений зір;
- збільшення ферментів печінки.
Рідкісні (можуть виникнути до 1 з 1000 осіб)
- вплив;
- грипоподібна хвороба;
- закладений або нежить;
- алергічний риніт;
- закладеність носа, пазух або верхніх дихальних шляхів, що переносить повітря до легенів;
- подагра;
- порушення сну (безсоння);
- передчасна еякуляція;
- відчуття дискомфорту;
- неможливість сидіти на місці;
- біль у грудях;
- сильний біль у грудях;
- прискорене серцебиття;
- гіпертонія;
- сухість у роті;
- біль у шлунку або печія;
- біль або дискомфорт внизу живота;
- діарея;
- висип;
- біль у попереку або в нижній частині грудей;
- м’язові болі;
- посмикування м’язів;
- часта необхідність сечовипускання;
- порушення статевого члена;
- спонтанна ерекція без сексуальної стимуляції;
- свербіж в області геніталій;
- постійне відчуття слабкості і втоми;
- набряк ніг або щиколоток;
- підвищення артеріального тиску;
- рожева або червона сеча, кров у сечі;
- аномальний додатковий шум серця;
- аномальні результати тесту простати під назвою «PSA»;
- аномальні результати тесту на білірубін, хімічну речовину, що утворюється при нормальному руйнуванні еритроцитів;
- аномальні результати тесту на креатинін, хімічну речовину, що виділяється з сечею, що корисно для оцінки функції нирок;
- збільшення ваги;
- лихоманка.
Повідомлення про побічні ефекти
Якщо у Вас виникли будь -які побічні ефекти, зверніться до лікаря або фармацевта, що включає будь -які можливі побічні ефекти, не зазначені у цій інструкції. Ви також можете повідомляти про побічні ефекти безпосередньо за допомогою національної системи повідомлень, наведеної у Додатку V. Повідомляючи про побічні ефекти, ви можете допомогти надати більше інформації про безпеку застосування цього лікарського засобу.
Термін придатності та утримання
Зберігайте цей препарат подалі від очей та недоступного для дітей місця.
Не використовуйте цей препарат після закінчення терміну придатності, зазначеного на блістері та картонній упаковці після "EXP". Термін придатності відноситься до останнього дня цього місяця.
Цей лікарський засіб не вимагає особливих умов зберігання.
Не викидайте ліки через стічні води або побутові відходи. Попросіть свого фармацевта, як викинути ліки, які ви більше не використовуєте. Це допоможе захистити навколишнє середовище.
Інша інформація
Що містить Спедра
- Діюча речовина - аванафіл. Кожна таблетка містить 50 мг аванафілу.
- Інші інгредієнти: маніт, фумарова кислота, гідроксипропілцелюлоза, погано заміщена гідроксипропілцелюлоза, карбонат кальцію, стеарат магнію та жовтий оксид заліза (Е172).
Опис зовнішнього вигляду Спедри та вміст упаковки
Спедра - блідо -жовта овальна таблетка з тисненням «50» на одній стороні. Таблетки поставляються в блістерах, що містять 4, 8 або 12 таблеток.
Не всі розміри упаковок можуть продаватися у вашій країні.
Джерело з інформацією про упаковку: AIFA (Італійське агентство з лікарських засобів). Вміст, опублікований у січні 2016 р. Наявна інформація може бути не актуальною.
Щоб мати доступ до найновішої версії, бажано зайти на веб-сайт AIFA (Італійське агентство з лікарських засобів). Відмова від відповідальності та корисна інформація.
01.0 НАЗВА ЛЕКАРСТВЕННОГО ПРОДУКТУ
КОРАБЛЬНІ ТАБЛЕТКИ 50 МГ
▼ Лікарський засіб підлягає додатковому моніторингу. Це дозволить швидко ідентифікувати нову інформацію про безпеку. Медичних працівників просять повідомляти про будь -які підозрювані побічні реакції. Інформацію про те, як повідомляти про побічні реакції, дивіться у розділі 4.8.
02.0 ЯКІСНИЙ І КІЛЬКІСНИЙ СКЛАД
Кожна таблетка містить 50 мг аванафілу.
Повний список допоміжних речовин див. У розділі 6.1.
03.0 ФАРМАЦЕВТИЧНА ФОРМА
Планшет.
Блідо -жовті овальні таблетки з тисненням «50» на одній стороні.
04.0 КЛІНІЧНА ІНФОРМАЦІЯ
04.1 Терапевтичні показання
Лікування еректильної дисфункції у дорослих чоловіків.
Для ефективності Spedra необхідна сексуальна стимуляція.
04.2 Дозування та спосіб введення
Дозування
Застосування у дорослих чоловіків
Рекомендована доза становить 100 мг, що приймається за необхідності приблизно за 15-30 хвилин до статевого акту (див. Розділ 5.1). Виходячи з індивідуальної ефективності та переносимості, дозу можна збільшити максимум до 200 мг або зменшити до 50 мг. Максимальна рекомендована частота дозування - один раз на день. Для відповіді на лікування потрібна сексуальна стимуляція.
Особливі популяції
Чоловіки похилого віку (вік ≥ 65 років)
У пацієнтів літнього віку корекція дози не потрібна. Дані щодо літніх пацієнтів старше 70 років обмежені.
Порушення функції нирок
Пацієнтам з нирковою недостатністю легкого та помірного ступеня (кліренс креатиніну ≥ 30 мл / хв) коригування дози не потрібне. Спедра протипоказана пацієнтам з тяжкою нирковою недостатністю (кліренс креатиніну нормальна функція нирок.
Порушення функції печінки
Спедра протипоказана пацієнтам з тяжкою печінковою недостатністю (клас С за Чайлдом-П’ю) (див. Розділи 4.3 та 5.2). Пацієнтам з печінковою недостатністю легкого та помірного ступеня (клас А або В за Чайлдом-П’ю) слід розпочинати лікування найменшою ефективною дозою та коригувати дозування залежно від переносимості.
Застосування у чоловіків з діабетом
У хворих на цукровий діабет корекція дози не потрібна.
Педіатричне населення
Немає вказівок на застосування Spedra для лікування еректильної дисфункції у педіатричній популяції.
Застосування пацієнтам, які застосовують інші ліки
Одночасне застосування інгібіторів CYP3A4
Одночасне застосування аванафілу з потужними інгібіторами CYP3A4 (включаючи кетоконазол, ритонавір, атазанавір, кларитроміцин, індинавір, ітраконазол, нефадозон, нелфінавір, саквінавір та телітроміцин) протипоказане (див. Розділи 4.3, 4.4 та 4.5).
У пацієнтів, які одночасно приймають інгібітори CYP3A4 середньої тяжкості (включаючи еритроміцин, ампренавір, апрепітант, дилтіазем, флуконазол, фосампренавір та верапаміл), максимальна рекомендована доза аванафілу не повинна перевищувати 100 мг з інтервалом не менше 48 годин між прийомами. ( див. розділ 4.5).
Спосіб введення
Пероральне застосування. Якщо Spedra приймається з їжею, початок ефективності може бути затриманий порівняно з прийомом натщесерце (див. Розділ 5.2).
04.3 Протипоказання
Підвищена чутливість до активної речовини або до будь -якої з допоміжних речовин, перерахованих у розділі 6.1. Пацієнти, які використовують донори оксиду азоту (такі як амільні нітрити) або органічні нітрати в будь -якій формі (див. Розділ 4.5).
Одночасне застосування інгібіторів фосфодіестерази типу 5 (ФДЕ5), включаючи аванафіл, із стимуляторами гуанілатциклази, такими як ріоцигуат, протипоказано, оскільки це потенційно може призвести до симптоматичної гіпотензії (див. Розділ 4.5).
Перед призначенням препарату Спедра лікарі повинні врахувати потенційний серцевий ризик, пов’язаний із статевою активністю у пацієнтів із наявними серцево-судинними захворюваннями.
Застосування аванафілу протипоказане при:
- пацієнти, які перенесли інфаркт міокарда, інсульт або небезпечну для життя аритмію за 6 місяців до застосування;
- пацієнти з гіпотонією (артеріальний тиск (артеріальний тиск> 170/100 мм рт. ст.)) у спокої;
- Пацієнти з нестабільною стенокардією, стенокардією статевого акту або застійною серцевою недостатністю класу 2 або вище за даними Нью -Йоркської асоціації серця.
Пацієнти з тяжкою печінковою недостатністю (C за Чайлдом-П’ю).
Пацієнти з тяжкою нирковою недостатністю (кліренс креатиніну
Пацієнти, які втратили зір на одне око через неартеріальну передню ішемічну нейропатію зорового нерва (NAION), незалежно від того, чи був цей епізод пов'язаний з попереднім впливом інгібітора PDE5 (див. Розділ 4.4).
Пацієнти із спадковими дегенеративними розладами сітківки.
Пацієнти, які застосовують потужні інгібітори CYP3A4 (включаючи кетоконазол, ритонавір, атазанавір, кларитроміцин, індинавір, ітраконазол, нефазодон, нелфінавір, саквінавір та телітроміцин) (див. Розділи 4.2, 4.4 та 4.5).
04.4 Спеціальні попередження та відповідні запобіжні заходи щодо використання
Перш ніж розглядати медикаментозне лікування, слід пройти анамнез та пройти клінічне обстеження для діагностики еректильної дисфункції та визначення можливих причин.
Серцево -судинний стан
Перед початком будь -якого лікування еректильної дисфункції лікар повинен проаналізувати серцево -судинний стан пацієнтів, оскільки певний ступінь серцевого ризику пов’язаний із статевою діяльністю (див. Розділ 4.3). розділ 4.5), тим самим посилюючи гіпотензивну дію нітратів (див. розділ 4.3). Пацієнти з обструкцією відтоку лівого шлуночка (наприклад, стенозом аорти або ідіопатичним гіпертрофічним субаортальним стенозом) можуть бути чутливими до дії судинорозширювальних засобів, включаючи інгібітори ФДЕ5.
Пріапізм
Пацієнтам, у яких ерекція триває 4 години або більше (пріапізм), слід негайно звернутися за медичною допомогою. Якщо приапізм не лікувати негайно, це може призвести до пошкодження тканини статевого члена та постійної втрати статевої потенції. Аванафіл слід з обережністю застосовувати пацієнтам з анатомічними деформаціями пеніса (такими як кутовий опік, кавернозний фіброз або хвороба Пейроні) або пацієнтам із станами, які можуть спричинити пріапізм (наприклад, серповидноклітинна анемія, множинна мієлома або лейкемія).
Проблеми із зором
Повідомлялося про дефекти зору та випадки переднеартеріальної передньої ішемічної оптичної нейропатії (НАІОН) у зв'язку з прийомом інших інгібіторів ФДЕ5. Негайно зверніться до лікаря (див. Розділ 4.3).
Вплив на кровотечу
Дослідження тромбоцитів людини в пробірці вказують на те, що інгібітори ФДЕ5 самі по собі не впливають на агрегацію тромбоцитів, але у надтерапевтичних дозах посилюють антитромбоцитарний ефект донора нітропрусиду натрію оксиду азоту. У людей інгібітори PDE5 не впливають на час кровотечі окремо або в поєднанні з ацетилсаліциловою кислотою.
Немає інформації про безпеку введення аванафілу пацієнтам з порушеннями кровотечі або активною виразковою хворобою. Тому аванафіл слід призначати таким пацієнтам лише після «ретельної оцінки користі та ризику».
Раптове зниження або втрата слуху
Пацієнтам слід порекомендувати припинити прийом інгібіторів ФДЕ5, включаючи аванафіл, та негайно звернутися до лікаря у разі раптового зниження або втрати слуху. Про ці події, які можуть супроводжуватися шумом у вухах та запамороченням, повідомлялося у зв’язку з тим, що вони приймали інгібітори ФДЕ5.
Одночасне застосування альфа-адреноблокаторів
Одночасне застосування альфа-адреноблокаторів та аванафілу може спричинити симптоматичну гіпотензію у деяких пацієнтів через адитивну судинорозширювальну дію (див. Розділ 4.5). Слід звернути увагу на наступне:
• Пацієнтів, які приймають альфа-адреноблокатори, слід стабілізувати перед початком застосування Спедри.Пацієнти, у яких спостерігається гемодинамічна нестабільність під час лікування тільки альфа-блокаторами, мають підвищений ризик симптоматичної гіпотензії при одночасному застосуванні аванафілу;
• у тих пацієнтів, які приймають альфа-адреноблокатори та стабілізувалися, аванафіл слід розпочинати з найменшої дози (50 мг);
• у тих пацієнтів, які вже приймають оптимізовану дозу Спедри, терапію альфа -блокаторами слід розпочинати з найменшої дози. Поступове збільшення дози альфа-адреноблокаторів може бути пов'язане з подальшим зниженням артеріального тиску під час прийому аванафілу;
• безпека комбінованого застосування аванафілу та альфа-адреноблокаторів може бути порушена іншими змінами, включаючи зменшення внутрішньосудинного об’єму та застосування інших антигіпертензивних лікарських засобів.
Одночасне застосування інгібіторів CYP3A4
Одночасний прийом аванафілу та потужних інгібіторів CYP3A4, таких як кетоконазол або ритонавір, протипоказаний (див. Розділи 4.2, 4.3 та 4.5).
Одночасне застосування інших засобів лікування еректильної дисфункції
Безпека та ефективність супутнього лікування Spedra з іншими інгібіторами PDE5 або інших засобів лікування еректильної дисфункції не вивчалися. Пацієнтам слід попередити, що вони не повинні приймати Spedra у таких комбінаціях.
Одночасне вживання алкоголю
Вживання алкоголю в поєднанні з аванафілом може збільшити ризик симптоматичної гіпотензії (див. Розділ 4.5). Пацієнтів слід попередити, що одночасне застосування аванафілу та алкоголю може збільшити ймовірність виникнення гіпотензії, запаморочення або непритомності.
Популяції не вивчені
Аванафіл не вивчався у пацієнтів з еректильною дисфункцією, спричиненою травмою спинного мозку або іншими неврологічними розладами, а також у осіб з тяжкими порушеннями функції нирок або печінки.
04.5 Взаємодія з іншими лікарськими засобами та інші форми взаємодії
Можливі фармакодинамічні взаємодії з аванафілом
Нітрати
Було показано, що аванафіл посилює гіпотензивну дію нітратів порівняно з плацебо у здорових осіб. Вважається, що це є результатом поєднаної дії нітратів та аванафілу на шляху оксиду азоту / цГМФ. Введення аванафілу пацієнтам, які використовують органічні нітрати в будь -якій формі, або донорам оксиду азоту (наприклад, амілнітриту) протипоказано. Пацієнту які приймали аванафіл менше 12 годин і які вважаються необхідними з медичної точки зору у ситуації, що загрожує життю, ймовірність значного та потенційно небезпечного для життя зниження артеріального тиску підвищується. нітрати слід вводити лише під ретельним наглядом лікаря, з відповідним гемодинамічним моніторингом (див. розділ 4.3).
Ліки, що знижують системний артеріальний тиск
Будучи судинорозширювальним засобом, аванафіл може знижувати системний артеріальний тиск. Якщо Spedra використовується в поєднанні з іншими препаратами, що знижують системний артеріальний тиск, адитивні ефекти можуть спричинити симптоматичну гіпотензію (наприклад, запаморочення, запаморочення, непритомність або майже непритомність). У клінічних дослідженнях 3 -ї фази не спостерігалося подій "гіпотонії", але іноді спостерігалися епізоди "запаморочення" (див. Розділ 4.8). У клінічних дослідженнях фази 3 один епізод «синкопи» спостерігався під час лікування плацебо та один епізод під час лікування 100 мг аванафілу.
Пацієнти з обструкцією відтоку лівого шлуночка (наприклад, стеноз аорти, ідіопатичний гіпертрофічний субаортальний стеноз) та пацієнти з серйозним порушенням контролю артеріального тиску вегетативної нервової системи можуть бути особливо чутливими до дії судинорозширювальних засобів, включаючи аванафіл.
Альфа -блокатори
Гемодинамічні взаємодії з доксазозином та тамсулозином вивчали у здорових добровольців у двосторонньому кросоверному дослідженні. У пацієнтів, які отримували стабільне лікування доксазозином, середнє максимальне зниження, відняте від плацебо, при систолічному артеріальному тиску стоячи та лежачи після введення аванафілу становило відповідно 2,5 мм рт.ст. та 6,0 мм рт.ст. Або зменшується від вихідного рівня потенційного клінічного значення після введення аванафілу (див. Розділ 4.4).
У пацієнтів, які отримували стабільне лікування тамсулозином, середнє максимальне зниження, відняте від ефекту плацебо, при систолічному артеріальному тиску стоячи та лежачи після введення аванафілу становило відповідно 3,6 мм рт.ст. та 3,1 мм рт.ст. зниження від вихідного рівня потенційного клінічного значення після введення аванафілу (див. розділ 4.4). Немає випадків синкопи або інших серйозних побічних явищ, пов’язаних із зниженням артеріального тиску у будь -якої когорти суб’єктів.
Антигіпертензивні засоби, крім альфа -блокаторів
Було проведено клінічне дослідження для оцінки впливу аванафілу на посилення ефектів зниження артеріального тиску деяких антигіпертензивних препаратів (амлодипіну та еналаприлу). Результати показали середнє максимальне зниження артеріального тиску лежачи на 2/3 мм рт. Ст. Порівняно з плацебо з еналаприлом і 1 / -1 мм рт.ст. з амлодипіном при одночасному введенні аванафілу.Оцінка статистично значущої різниці у максимальному зниженні діастолічного артеріального тиску на лежачому положенні лежачи на спині при застосуванні лише еналаприлу та аванафілу -значення, яке повернулося до вихідного рівня через 4 години після дози аванафілу. когорти, у одного суб’єкта спостерігалося зниження артеріального тиску без симптомів гіпотензії, яке пройшло протягом 1 години від початку. Аванафіл не впливає на фармакокінетику амлодипіну, але амлодипін збільшив максимальну та загальну експозицію аванафілу на 28% та 60% відповідно.
Алкоголь
Вживання алкоголю в поєднанні з аванафілом може збільшити ймовірність симптоматичної гіпотензії. У тристоронньому перехресному дослідженні з одноразовою дозою у здорових добровольців середнє максимальне зниження діастолічного артеріального тиску було значно вищим після введення аванафілу разом із алкоголем, порівняно з одним аванафілом (3,2 мм рт. Ст.) Або алкоголем окремо (5,0 мм рт. Ст.) ( див. розділ 4.4).
Інші методи лікування еректильної дисфункції
Безпека та ефективність комбінації аванафілу та інших інгібіторів ФДЕ5 або інших засобів лікування еректильної дисфункції не вивчалися (див. Розділ 4.4).
Вплив інших речовин на аванафіл
Аванафіл є субстратом CYP3A4 і переважно метаболізується цим цитохромом. Дослідження показали, що лікарські засоби, що інгібують CYP3A4, можуть збільшити експозицію аванафілу (див. Розділ 4.2).
Інгібітори CYP3A4
Кетоконазол (400 мг на добу), селективний та дуже потужний інгібітор CYP3A4, збільшував Cmax та експозицію (AUC) одноразової дози 50 мг аванафілу у 3 та 14 разів відповідно та подовжував період напіввиведення. аванафілу близько 9 годин. Ритонавір (600 мг на день), дуже потужний інгібітор CYP3A4, який також інгібує CYP2C9, збільшував Cmax та AUC одноразової дози 50 мг аванафілу у 2 та 13 разів відповідно та подовжував період напіввиведення аванафілу у 1 раз. близько 9 годин. Очікується, що інші потужні інгібітори CYP3A4 (наприклад, ітраконазол, вориконазол, кларитроміцин, нефазодон, саквінавір, нелфінавір, індинавір, атазанавір та телітроміцин) мають подібну дію. Отже, одночасний прийом аванафілу та потужних інгібіторів CYP3A4 протипоказаний (див. Розділи 4.2, 4.3 та 4.4).
Еритроміцин (500 мг на добу), помірний інгібітор CYP3A4, збільшував Cmax та AUC одноразової дози 200 мг аванафілу приблизно у 2 та 3 рази відповідно та подовжував період напіввиведення аванафілу приблизно до 8 годин ... Очікується, що інші помірні інгібітори CYP3A4 (наприклад, ампренавір, апрепітант, дилтіазем, флуконазол, фосампренавір та верапаміл) мають подібну дію. Отже, максимальна рекомендована доза аванафілу становить 100 мг, яку не слід перевищувати раз на 48 годин для пацієнтів, які одночасно приймають інгібітори CYP3A4 середньої тяжкості (див. Розділ 4.2).
Незважаючи на те, що специфічні взаємодії не вивчалися, інші інгібітори CYP3A4, включаючи грейпфрутовий сік, ймовірно збільшать експозицію аванафілу.
Субстрати CYP3A4
Амлодипін (5 мг на добу) збільшував Cmax та AUC одноразової дози 200 мг аванафілу приблизно на 28% та 60% відповідно. Ці зміни експозиції не вважаються клінічно значущими. Разова доза аванафілу не впливала на рівні амлодипіну в плазмі крові.
Хоча специфічні взаємодії аванафілу з ривароксабаном та апіксабаном (обидва субстрати CYP3A4) не вивчалися, таких взаємодій не очікується.
Індуктори цитохрому Р450
Потенційний вплив індукторів CYP, особливо індукторів CYP3A4 (наприклад, бозентану, карбамазепіну, ефавіренцу, фенобарбіталу та рифампіцину) на фармакокінетику та ефективність аванафілу не оцінювався. Одночасне застосування аванафілу та індуктора CYP не рекомендується, оскільки це може знизити ефективність аванафілу.
Вплив аванафілу на інші лікарські засоби
Інгібування цитохрому Р450
У дослідженнях в пробірці у мікросомах печінки людини аванафіл виявив незначний потенціал взаємодії ліків з CYP1A1 / 2, 2A6, 2B6 та 2E1. Крім того, метаболіти аванафілу (M4, M16 та M & SUP2; 7) також продемонстрували мінімальне пригнічення CYP 1A1 / 2, 2A6, 2B6, 2C8, 2C9, 2C19, 2D6, 2E1 та 3A4. На підставі цих даних аванафіл не очікується істотного впливу на інші лікарські засоби, що метаболізуються цими ферментами.
Дані в пробірці виявлено потенційні взаємодії аванафілу з CYP 2C19, 2C8 / 9, 2D6 та 3A4, тоді як подальші клінічні дослідження з використанням омепразолу, росиглітазону та дезипраміну не виявили клінічно значущих взаємодій з CYP 2C19, 2C8 / 9 та 2D6.
Індукція цитохрому Р450
Оцінювали потенційну індукцію CYP1A2, CYP2B6 та CYP3A4 аванафілом у первинних гепатоцитах людини в пробірці не виявили потенційних взаємодій у клінічно значущих концентраціях.
Конвеєри
Результати в пробірці показав скромну здатність аванафілу діяти як субстрат для P-gp та як інгібітор P-gp з дигоксином як субстратом при концентраціях аванафілу нижче розрахункової концентрації в кишечнику. Потенціал впливу аванафілу на транспортування інших препаратів, опосередкованих P-gp, невідомий.
На підставі даних досліджень in vitro, аванафіл може діяти як інгібітор BCRP у клінічно значущих концентраціях.
У клінічно значущих концентраціях аванафіл не діє як інгібітор OATP1B1, OATP1B3, OCT1, OCT2, OAT1, OAT3 та BSEP.
Вплив аванафілу на інші транспортери невідомий.
Ріокігуат
Доклінічні дослідження показали додатковий системний ефект зниження артеріального тиску при одночасному прийомі інгібіторів ФДЕ5 з риоцигуатом. У клінічних дослідженнях було показано, що ріоцигуат посилює гіпотензивну дію інгібіторів ФДЕ5. У дослідженій популяції не було даних про сприятливий клінічний ефект після застосування комбінації.Одночасне застосування ріоцигуату з інгібіторами ФДЕ5, включаючи аванафіл, протипоказане (див. Розділ 4.3).
04.6 Вагітність та період лактації
Вагітність
Спедра не показана до застосування жінкам.
Немає даних про застосування аванафілу вагітним жінкам. Дослідження на тваринах не вказують на прямі чи непрямі шкідливі наслідки щодо вагітності, ембріонального / внутрішньоутробного розвитку, пологів або постнатального розвитку (див. Розділ 5.3).
Час годування
Немає даних про застосування аванафілу під час лактації.
Родючість
Не було впливу на рухливість або морфологію сперматозоїдів після одноразового перорального введення 200 мг аванафілу у здорових добровольців.
На даний момент немає даних про сперматогенез у здорових дорослих чоловіків та дорослих чоловіків з легкою еректильною дисфункцією.
04.7 Вплив на здатність керувати автомобілем та працювати з механізмами
Спедра має незначний вплив на здатність керувати автомобілем або працювати з механізмами. Оскільки у клінічних випробуваннях аванафілу повідомлялося про запаморочення та порушення зору, пацієнти повинні знати про свою реакцію на Spedra перед тим, як керувати автотранспортом або працювати з механізмами.
04.8 Побічні ефекти
Короткий опис профілю безпеки
Профіль безпеки Spedra базується на 2436 пацієнтах, які зазнали впливу аванафілу під час програми клінічного розвитку. Найбільш поширеними побічними реакціями, про які повідомлялося у клінічних випробуваннях, були головний біль, почервоніння, закладеність носа та пазух носа та біль у спині. Загальні побічні реакції та побічні реакції у пацієнтів, які отримували аванафіл, були більш частими у пацієнтів з нормальним індексом маси тіла (ІМТ)
У довгостроковому клінічному дослідженні частка пацієнтів, які відчували побічні реакції, зменшувалась із збільшенням тривалості лікування.
Зведена таблиця побічних реакцій
У наведеній нижче таблиці перераховані побічні реакції, які спостерігалися у плацебо-контрольованих клінічних випробуваннях згідно з умовою частоти MedDRA: дуже часто (≥ 1/10), часто (≥ 1/100,
Опис окремих побічних реакцій, що спостерігаються при застосуванні інших інгібіторів ФДЕ5
У невеликій кількості випадків клінічних випробувань та досвіду постмаркетингової діяльності повідомлялося про неартеріальну передню ішемічну оптичну нейропатію (NAION) та раптову втрату слуху з іншими інгібіторами ФДЕ5. Під час клінічних випробувань аванафілу не було зареєстровано жодного випадку (див. Розділ 4.4).
У постмаркетинговому дослідженні та клінічних випробуваннях повідомлялося про невелику кількість випадків пріапізму з іншими інгібіторами ФДЕ5.
У постмаркетинговому дослідженні та клінічних випробуваннях повідомлялося про невелику кількість випадків гематурії, гематоспермії та кровотечі з пеніса.
У постмаркетинговому досвіді з іншими інгібіторами ФДЕ5 повідомлялося про гіпотензію, а в клінічних випробуваннях з аванафілом повідомлялося про запаморочення, симптом, який зазвичай виникає через низький артеріальний тиск (див. Розділ 4.5).
Повідомлення про підозрювані побічні реакції
Повідомлення про підозрювані побічні реакції, що виникають після реєстрації лікарського засобу, є важливим, оскільки воно дозволяє здійснювати постійний моніторинг співвідношення користь / ризик лікарського засобу. Медичних працівників просять повідомляти про будь -які підозрювані побічні реакції через національну систему звітності. У Додатку V.
04.9 Передозування
Здоровим пацієнтам вводили разові дози до 800 мг аванафілу, а пацієнтам - кілька добових до 300 мг. Побічні реакції були подібними до тих, що спостерігалися при менших дозах, але частота та тяжкість були вищими.
У разі передозування при необхідності слід застосовувати стандартні підтримуючі заходи. Не очікується, що нирковий діаліз прискорить кліренс, оскільки аванафіл сильно зв’язується з білками плазми крові і не виводиться з сечею.
05.0 ФАРМАКОЛОГІЧНІ ВЛАСТИВОСТІ
05.1 Фармакодинамічні властивості
Фармакотерапевтична група: препарати, що застосовуються при еректильній дисфункції.
Код ATC: G04BE10.
Механізм дії
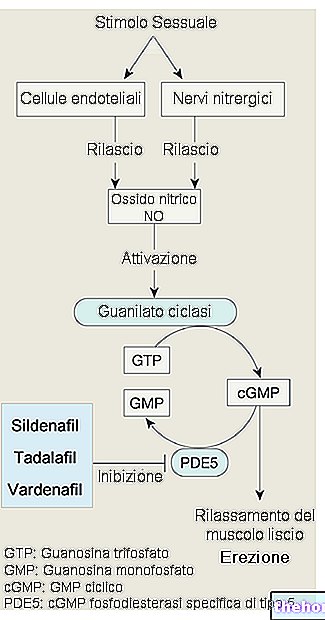
Аванафіл є оборотним, потужним і високоселективним інгібітором фосфодіестерази типу 5 (ФДЕ5), специфічним для циклічного гуанозинмонофосфату (цГМФ). Коли статева стимуляція викликає місцеве вивільнення оксиду азоту, інгібування ФДЕ5 аванафілом призводить до підвищення рівня цГМФ у кавернозних тілах пеніса. Це призводить до розслаблення гладкої мускулатури та припливу крові до тканин статевого члена, що призводить до ерекції. Аванафіл не має ефекту за відсутності сексуальної стимуляції.
Фармакодинамічні ефекти
Освіта в пробірці продемонстрували, що аванафіл є високоселективним щодо ФДЕ5. Його вплив на PDE5 більш сильний, ніж на інші відомі фосфодіестерази (> 100 разів у порівнянні з PDE6;> 1000 разів у порівнянні з PDE4, PDE8 та PDE10;> 5000 разів у порівнянні з PDE2 та PDE7;> 10000 разів у порівнянні з PDE1, PDE3 , PDE9 та PDE11). Аванафіл більш ніж у 100 разів сильніший у порівнянні з PDE5, ніж у PDE6, який міститься у сітківці ока та відповідає за фототрансдукцію.Приблизно 20 000-кратна селективність щодо ФДЕ5 щодо ФДЕ3, ферменту, що міститься в серці та кровоносних судинах, важлива, оскільки ФДЕ3 бере участь у контролі скорочення серця.
У дослідженні плетизмографії пеніса (RigiScan) 200 мг аванафілу викликало ерекцію, яку вважали достатньою для проникнення (жорсткість 60% відповідно до RigiScan) у деяких чоловіків вже через 20 хвилин після введення, і загальна реакція цих суб'єктів на аванафіл була статистично значущою, порівняно з плацебо, протягом часового інтервалу 20-40 хвилин.
Клінічна ефективність та безпека
У клінічних дослідженнях оцінювали вплив аванафілу на здатність чоловіків з еректильною дисфункцією (ЕД) досягати та підтримувати "ерекцію, достатню для задовільної статевої активності". Аванафіл оцінювали у 4 рандомізованих подвійних сліпих дослідженнях. контрольована паралельна група, що триває до 3 місяців у загальній популяції ЕД, у пацієнтів з діабетом 1 та 2 типу та ЕД, а у пацієнтів з ЕД після радикальної нервової простатектомії - двостороннє щадження. Четверте дослідження досліджувало початок дії аванафілу у двох концентраціях по 100 та 200 мг у відсотках статевих спроб, що призвели до успішного завершення статевого акту на одного суб’єкта. Загалом 1774 пацієнти отримували аванафіл за потреби та у дозах 50 мг (в одному дослідженні), 100 мг і 200 мг (у чотирьох дослідженнях) відповідно.Пацієнти повинні були приймати 1 дозу досліджуваного препарату приблизно 30 хвилин я до початку статевого життя. У четвертому дослідженні пацієнтам пропонували спробувати статевий акт приблизно через 15 хвилин після введення, щоб оцінити настання еректогенного ефекту аванафілу, прийнятого за необхідності, у дозі 100 або 200 мг.
Крім того, підгрупа пацієнтів була включена до відкритого подовженого дослідження, в якому 493 пацієнти отримували аванафіл щонайменше 6 місяців і 153 пацієнти щонайменше 12 місяців. Пацієнтам спочатку було призначено 100 мг аванафілу, і в будь -який час протягом дослідження вони могли попросити збільшити дозу аванафілу до 200 мг або зменшити її до 50 мг, виходячи з індивідуальної відповіді на лікування.
У всіх дослідженнях спостерігалося статистично значуще покращення всіх первинних показників ефективності для всіх трьох доз аванафілу порівняно з плацебо. Ці відмінності зберігаються при тривалому лікуванні (як виявлено у дослідженнях у загальній популяції ЕД, у діабетиків з ЕД, у чоловіків з ЕД після двосторонньої радикальної простатектомії, що зберігає нерви, та у відкритому подовженому дослідженні).
У загальній популяції ЕД середній відсоток спроб, що призвели до успішного статевого акту, становив приблизно 47%, 58% та 59% у групах аванафілу 50 мг, 100 мг та 200 мг відповідно, порівняно з приблизно 28% у групі плацебо.
У чоловіків із цукровим діабетом 1 -го та 2 -го типу середній відсоток спроб, що призвели до успішного статевого акту, становив приблизно 34% та 40% для груп, які отримували 100 мг та 200 мг відповідно. група плацебо.
У чоловіків з ЕД після двосторонньої радикальної радикальної простатектомії, середня частота спроб, що призвели до успішного статевого акту, становила приблизно 23% та 26% відповідно для груп лікування 100 мг та 200 мг відповідно. група.
У дослідженні "початок дії" аванафіл продемонстрував статистично значуще покращення первинної змінної ефективності (середній відсоток позитивних відповідей на суб'єкта, починаючи з моменту введення дози, до профілю сексуальної зустрічі 3 - SEP3) у порівнянні з плацебо, частота успішного статевого акту приблизно через 15 хвилин після прийому 24,71% для дози 100 мг та 28,18% для дози 200 мг порівняно з 13,78% для плацебо.
У всіх ключових дослідженнях аванафілу частота успішних спроб статевого акту була значно вищою для всіх доз аванафілу порівняно з плацебо для всіх досліджуваних інтервалів після прийому.
Педіатричне населення
Європейське агентство з лікарських засобів скасувало зобов’язання надсилати результати досліджень Spedra у всіх підгрупах педіатричної популяції з еректильною дисфункцією (див. Розділ 4.2 для інформації про застосування у педіатрії).
05.2 Фармакокінетичні властивості
Після перорального введення аванафіл швидко всмоктується, середній Tmax становить від 30 до 45 хвилин. Його фармакокінетика пропорційна дозі у рекомендованому діапазоні доз. Вона усувається головним чином шляхом метаболізму в печінці (переважно CYP3A4). Одночасне застосування потужних інгібіторів CYP3A4 (наприклад, кетоконазолу та ритонавіру) пов’язане із збільшенням експозиції аванафілу у плазмі крові (див. Розділ 4.5). Термін напіввиведення аванафілу становить приблизно 6-17 годин.
Поглинання
Аванафіл швидко всмоктується. Максимальні спостережувані концентрації в плазмі досягаються протягом 0,5-0,75 годин після перорального прийому натще. При прийомі аванафілу з їжею з високим вмістом жиру швидкість всмоктування зменшується із середньою затримкою T 1,25 години та середнім зниженням C на 39% (200 мг). Не впливає на величину експозиції (AUC). Вважається, що незначні зміни Cmax аванафілу мають мінімальне клінічне значення.
Розповсюдження
Приблизно на 99% аванафіл зв’язується з білками плазми крові. Зв’язування з білками не залежить від загальної концентрації активної речовини, віку та функції нирок або печінки.
Аванафіл не накопичується у плазмі крові при введенні двічі на день протягом 7 днів у дозі 200 мг. На підставі вимірювань аванафілу у спермі здорових добровольців через 45-90 хвилин після введення у спермі пацієнтів присутній менше 0,0002% введеної дози.
Біотрансформація
Аванафіл виводиться насамперед мікросомальними ізоферментами печінки CYP3A4 (основний шлях) та CYP2C9 (вторинний шлях). Концентрація основних метаболітів, що циркулюють у плазмі крові, М4 та М16, становить відповідно 23% та 29% вихідної сполуки. Метаболіт М4 демонструє профіль селективності щодо фосфодіестерази, подібний до профілю аванафілу та інгібуючу дію в пробірці для PDE5 дорівнює 18% від такої кількості аванафілу. Таким чином, M4 відповідає за приблизно 4% загальної фармакологічної активності. Метаболіт M16 неактивний щодо ФДЕ5.
Ліквідація
Аванафіл інтенсивно метаболізується у людини. Після перорального прийому аванафіл виводиться у вигляді метаболітів переважно з калом (приблизно 63% введеної пероральної дози) та меншою мірою з сечею (приблизно 21% введеної пероральної дози).
Інші особливі популяції
Пацієнти літнього віку
Пацієнти літнього віку (65 років і старше) мають порівнянну експозицію з такою у молодих пацієнтів (18-45 років). Однак дані про людей старше 70 років обмежені.
Порушення функції нирок
У пацієнтів з помірною нирковою недостатністю (кліренс креатиніну ≥ 50, тяжка ниркова недостатність або термінальна стадія ниркової недостатності, які проходять гемодіаліз.
Порушення функції печінки
Пацієнти з легкою печінковою недостатністю (Чайлд-П’ю А) мають аналогічний вплив на суб’єктів із нормальною функцією печінки при одноразовій дозі 200 мг аванафілу.
Експозиція через 4 години після введення аванафілу 200 мг є нижчою у пацієнтів з помірною печінковою недостатністю (B за Чайлдом-П’ю), ніж у пацієнтів з нормальною функцією печінки. ефективна доза аванафілу 100 мг.
05.3 Дані доклінічної безпеки
Неклінічні дані не показують особливої небезпеки для людини на основі звичайних досліджень фармакологія безпеки, токсичність при повторних дозах, генотоксичність, канцерогенний потенціал та репродуктивна токсичність.
У дослідженні щодо фертильності щурів та раннього ембріонального розвитку, зменшення фертильності та рухливості сперматозоїдів, зміни циклів еструсу та збільшення відсотка аномальних сперматозоїдів відбувалося при споживанні 1000 мг / кг / добу, що також спричиняло токсичність для батьків у самців та самок, які отримували лікування .Ніякого впливу на фертильність та параметри сперматозоїдів не спостерігалося у самців щурів у дозах до 300 мг / кг / добу (9-кратна експозиція на людині на основі незв’язаного препарату AUC у дозі 200 мг) у щурів або мишей, які отримували дози до 600 або 1000 мг / кг / добу протягом 2 років, а також у собак, які отримували аванафіл протягом 9 місяців при експозиції, що в 110 разів перевищує максимальну рекомендовану дозу для людини (MRHD - Максимальна рекомендована доза для людини).
У вагітних щурів не було виявлено жодних ознак тератогенності, ембріотоксичності чи фетотоксичності при дозах до 300 мг / кг / добу (приблизно у 15 разів більше МДГР на основі мг / м2 у пацієнта вагою 60 кг). При дозі 1 000 мг / кг / добу для матері, токсичній для матері (приблизно в 49 разів більше МРХД на основі мг / м2), спостерігалося зменшення маси тіла плода без ознак тератогенності. У вагітних кроликів не було виявлено жодних ознак тератогенності, ембріотоксичності чи фетотоксичності при дозах до 240 мг / кг / добу (приблизно у 23 рази більше МДГР на основі мг / м2). У дослідженні на кроликах токсичність для матері спостерігалася при 240 мг / кг / добу.
У дослідженні пренатального та постнатального розвитку на щурах щенята демонстрували стійке зменшення маси тіла у дозах 300 мг / кг / день або більше (приблизно в 15 разів більше МРХД на основі мг / м2) та затримку статевого розвитку при 600 мг / кг. / день (приблизно в 29 разів перевищує MRHD на основі мг / м2).
06.0 ФАРМАЦЕВТИЧНА ІНФОРМАЦІЯ
06.1 Допоміжні речовини
Маніт
Фумарова кислота
Гідроксипропілцелюлоза
Злегка заміщена гідроксипропілцелюлоза
Карбонат кальцію
Стеарат магнію
Жовтий оксид заліза (E172)
06.2 Несумісність
Не актуально.
06.3 Строк дії
5 років.
06.4 Особливі умови зберігання
Цей лікарський засіб не вимагає особливих умов зберігання.
06.5 Характер безпосередньої упаковки та вміст упаковки
Блістери з ПВХ / PCTFE / алюмінію у картонній упаковці по 4, 8 та 12 таблеток. Не всі розміри упаковок можна продавати.
06.6 Інструкції з використання та поводження
Ніяких спеціальних вказівок.
07.0 ВЛАСНИК РОЗРОБНИЦТВА
МЕНАРІНІ МІЖНАРОДНІ ОПЕРАЦІЇ ЛЮКСЕМБУРГ С.А.
1, Avenue de la Gare, L-1611 Люксембург
Люксембург
08.0 НОМЕР РОЗВИТКУ З РОБОТИ
ЄС / 1/13/841 / 001-003
042876019
042876021
042876033
09.0 ДАТА ПЕРШОГО ДОЗВІЛЕННЯ АБО ОНОВЛЕННЯ ДОЗВІЛЛЯ
Дата першого дозволу: 21 червня 2013 року
10.0 ДАТА ПЕРЕГЛЯНУ ТЕКСТУ
Березень 2016 року