Цей метаболічний шлях включає кілька фаз: холестерин передається з периферійних тканин до печінки спочатку через лімфатичну систему, потім через кровотік. Основними компонентами, які беруть участь у зворотному транспорті холестерину, є ЛПВЩ, АВСА1 та апо А-I.
периферичні клітини, що не є кишковою або печінковою, не здатні розщеплювати надлишок холестерину; тому для підтримки клітинного гомеостазу необхідна наявність механізму, призначеного для видалення холестерину.
Цей механізм, спрямований на відновлення печінкою надлишкового периферичного холестерину, називається «зворотним транспортом холестерину» (РКД: зворотний транспорт холестерину).
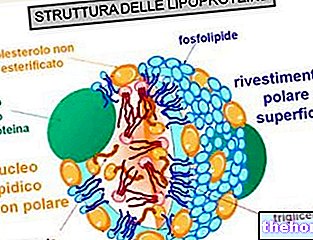
(фосфоліпіди та холестерин), що призводить до збирання та утворення зрілих частинок ЛПВЩ.Попередники HDL
Перша стадія зворотного транспорту холестерину полягає у виробленні кишечником і печінкою дискоїдних попередників ЛПВЩ, які виставляють на їх поверхню апопротеїни (переважно ApoA-I).
Таким чином, вивільняються молекули-попередники ЛПВЩ, які називаються пре-В-ЛПВЩ, які включають дуже невелику кількість холестерину та ліпідів, особливо фосфоліпідів. Наявність цих молекул -попередників на периферійному рівні сприяє перенесенню надлишкового вільного холестерину (ФК) - витікаючого з клітин периферичної тканини - до апо AI за допомогою втручання мембранного транспортера під назвою АТФ -зв’язувальна касета А1 (ABCA1).
Цей транспортер локалізований на поверхні клітини та в мембранах Гольджі і може транспортувати ліпіди з апарату Гольджі до клітинної мембрани, тим самим полегшуючи їх витік.
У цей момент, як тільки вільний холестерин надходить у природну ЛПВЩ, втручається плазмовий фермент печінкового походження, який називається плазмовий лецитин-холестерин ацилтрансфераза або простіше кажучи LCAT; цей фермент перетворює вільний холестерин, включений у пре-В-ЛПВЩ, в складні ефіри холестерину, перетворюючи пре-В-ЛПВЩ у їх зрілу форму α-ЛПВЩ; на практиці безперервне накопичення холестерину в ядрі ліпопротеїнів перетворює дискоїдні ЛПВЩ у сферичні та пухкі частинки, які можуть додатково набувати апопротеїни з частинок ліпопротеїнів, багатих на тригліцериди, та зливатися між собою.
У всьому процесі аполіпопротеїн ІІ відіграє ключову роль, стимулюючи як активність транспортера ABCA1, так і LCAT.Оскільки ApoAI є найбільш представленим аполіпопротеїном у ЛПВЩ, його концентрація у плазмі крові безпосередньо залежить від рівня холестерину ЛПВЩ.
ЗВЕРНІТЬ УВАГУ: процес естерифікації є важливим для запобігання повторній дифузії холестерину з ЛПВЩ на плазматичну мембрану; цей механізм використовує жирну кислоту у другому положенні, присутньому в молекулах фосфатидилхоліну.
Потім процес естерифікації, опосередкований LCAT, перетворює молекули пре-В-ЛПВЩ у їх «зрілу» сферичну форму α-ЛПВЩ. Потім ці ліпопротеїди транспортуються до печінки, де вони виділяють холестерин, згідно з двома різними шляхами.
Перший шлях до печінки
У першому випадку ЛПВЩ, багата естерифікованим холестерином, переносять цей ліпід у ліпопротеїди, багаті на тригліцериди (ліпопротеїди дуже низької та низької щільності), які потім перехоплюються печінкою через специфічні рецептори (ЛПНЩ-Р) і видаляються з циркуляції.
Метою є передача периферичного холестерину до печінки через рецепторну систему ЛПНЩ, потім «вивільнення» ЛПВЩ від надлишку холестерину на периферійному рівні, щоб знову зробити їх доступними для прийняття його з тканин; Знижуючи рівень холестерину, ЛПВЩ приймають тригліцериди в обмін, і це відбувається завдяки білку перенесення ефіру холестерину (CETP).
Тому завдання цього білка - сприяти перерозподілу та балансу складних ефірів холестерину та тригліцеридів між ліпопротеїнами ЛПВЩ, ЛПНЩ, IDL, VLDL, хіломікронами та залишками хіломікронів, що, як результат, призводить до збагачення тригліцеридів ЛПВЩ, за рахунок ефірів холестерину та зменшення розміру ЛПВЩ.
Другий шлях до печінки
Другий шлях включає печінкові рецептори SR-B1 для ЛПВЩ, багатих естерифікованим холестерином, за відсутності супутньої деградації білкової частини ЛПВЩ, яка потім переробляється. На практиці цей фермент дозволяє звільнити ЛПВЩ від їх вмісту та регенерувати нові пре-В-ЛПВЩ.
Частина ЛПВЩ та АроА-I інтерналізована та деградує на лізосомному рівні як у клітинах печінки, так і в нирках. Поглинання, опосередковане SR-B1, стає більш ефективним завдяки активності печінкової ліпази, здатної до ремоделювання ЛПВЩ шляхом гідролізу поверхневих фосфоліпідів та уможливлюючи потік естерифікованого холестерину з серцевини ліпопротеїну до плазматичної мембрани (передбачається, що між іншими , що ApoE також бере участь у селективному поглинанні, оскільки миші з дефіцитом гена ApoE демонструють зниження ефективності цього шляху.) SR-BI переважно експресується в печінці, надниркових залозах та яєчниках.