Діючі речовини: ботулотоксин типу А
BOTOX® 100 Allergan Units, порошок для розчину для ін’єкцій
BOTOX® 200 Allergan Units, порошок для розчину для ін’єкцій
Чому використовується ботокс? Для чого це?
Що таке BOTOX
Ботокс - препарат для розслаблення м’язів, який вводиться в м’язи, стінку сечового міхура або під шкіру. Він діє, частково блокуючи нервові імпульси в кожній м’язі, куди він вводиться, і зменшує надмірне скорочення цих м’язів.
Коли BOTOX вводиться під шкіру, він діє на потові залози, зменшуючи кількість виділеного поту.
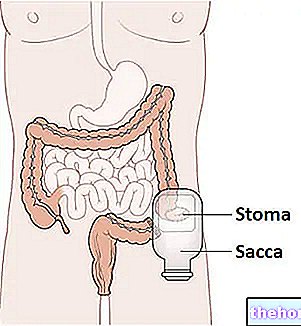
При введенні в стінку сечового міхура BOTOX діє на мускулатуру сечового міхура, зменшуючи втрату сечі (нетримання сечі). У разі хронічної мігрені вважається, що BOTOX може блокувати больові сигнали, які опосередковано блокують розвиток мігрені. Однак, як BOTOX діє при хронічній мігрені, до кінця не вивчено.
Для чого призначений BOTOX
У дорослих BOTOX використовується для контролю:
- постійні м’язові спазми на повіках та обличчі
- постійні м’язові спазми на шиї та плечах
- постійні м’язові спазми в зап’ясті та кисті у пацієнтів з інсультом
- надмірна пітливість пахв, що перешкоджає нормальній повсякденній діяльності, коли інші місцеві процедури не допомагають
- гіперактивний сечовий міхур з нетриманням сечі - раптова позива спорожнити сечовий міхур і необхідність відвідувати туалет частіше, ніж зазвичай - коли інші препарати (звані антихолінергіками) не допомогли
- нетримання сечі внаслідок розладів сечового міхура, пов’язаних з травмою спинного мозку або розсіяним склерозом.
Ботокс використовується для зменшення симптомів хронічної мігрені у дорослих:
- з головним болем протягом 15 і більше днів на місяць, з яких щонайменше 8 днів з мігренем і які не мали адекватної реакції або мають непереносимість препаратів проти мігрені, призначених для профілактики.
Хронічна мігрень - це захворювання, яке вражає нервову систему. Зазвичай пацієнти страждають від болю в голові, що часто супроводжується надмірною чутливістю до світла, гучних звуків або запахів / запахів, а також нудотою та / або блювотою. Голова виникає протягом 15 і більше днів на місяць Було показано, що BOTOX значно зменшує симптоми та покращує якість життя пацієнтів, які страждають на хронічну мігрень.
Ботокс слід призначати вам лише у випадку, якщо у вас діагностовано хронічну мігрень невропатологом, який спеціалізується в цій галузі. Ботокс слід вводити під наглядом невролога. BOTOX не використовується при гострій мігрені, хронічних головних болях напруженого типу або у пацієнтів з головним болем від надмірного вживання наркотиків.
У дітей віком від 2 років з церебральним паралічем, які не можуть ходити, Ботокс використовується для контролю:
- деформація стопи, викликана постійними спазмами м’язів ніг. BOTOX знімає постійні м’язові спазми в ногах.
Протипоказання Коли не слід застосовувати ботокс
Не використовуйте BOTOX
- якщо у вас алергія (гіперчутливість) до ботулотоксину типу А або до будь -якого іншого інгредієнта препарату Ботокс;
- якщо у вас є запропонована "інфекція в місці ін'єкції";
- якщо ви проходите лікування від нетримання сечі і у вас розвивається «інфекція сечовивідних шляхів або виникає» раптова нездатність спорожнити сечовий міхур (і не використовуйте регулярно катетер);
- якщо ви лікуєтесь від нетримання сечі і не маєте намір використовувати катетер, якщо це необхідно.
Будьте особливо обережні з BOTOX
Перед використанням BOTOX
Скажіть своєму лікарю, якщо:
- у минулому були проблеми з ін’єкціями (наприклад, непритомність);
- у вас запалення в м’язах або в ділянці шкіри, куди лікар має намір зробити ін’єкцію;
- мати значну слабкість або втрату м’язового тонусу, коли ваш лікар має намір зробити ін’єкцію;
- коли -небудь мали проблеми з ковтанням або з їжею або рідинами, що випадково потрапили в легені, особливо якщо ви лікуєтесь від постійних м’язових спазмів у шиї та плечах;
- страждати від будь -яких інших м’язових проблем або хронічних захворювань, що вражають м’язи (наприклад, міастенії гравіс або синдрому Ітона Ламберта);
- страждають певними захворюваннями нервової системи (такими як бічний аміотрофічний склероз або рухова нейропатія);
- у вас очна хвороба під назвою закритокутова глаукома (високий очний тиск) або вам сказали, що у вас є ризик розвитку цього типу глаукоми;
- перенесли будь -яку операцію або травму, які могли змінити м’яз, який потрібно ввести ін’єкцією;
- лікується від гіперактивного сечового міхура з нетриманням сечі і є людиною, у якої є ознаки та симптоми обструкції сечі, такі як утруднене сечовипускання або слабкий або переривчастий потік
Після лікування BOTOX
Зверніться до лікаря і негайно зверніться за допомогою, якщо станеться таке:
- утруднене дихання, ковтання або здатність говорити;
- кропив’янка, набряк, включаючи набряк обличчя або горла, хрипи, відчуття слабкості та задишка (можливі симптоми важкої алергічної реакції).
Заходи безпеки при застосуванні Що потрібно знати, перш ніж приймати Ботокс
Якщо ви отримуєте BOTOX занадто часто або доза занадто висока, ваше тіло може почати виробляти антитіла, які можуть зменшити ефект BOTOX.
Якщо ви довго не практикували багато фізичних навантажень до початку лікування BOTOX, будь -яку активність слід поступово відновлювати після процедур.
Навряд чи цей препарат покращить ступінь руху в суглобах, де навколишні м’язи втратили здатність до розтягування.
Коли BOTOX використовується для лікування постійних м’язових спазмів повік, він може зменшити моргання та пошкодити поверхню очей. захистити око. Ваш лікар скаже вам, якщо це необхідно.
Коли ви використовуєте BOTOX для контролю втрати сечі, ваш лікар повинен буде дати вам антибіотики до та після лікування, щоб запобігти будь -яким інфекціям сечовивідних шляхів.
Ваш лікар побачить вас приблизно через 2 тижні після ін’єкції, якщо ви не використовували катетер до ін’єкції. Вас попросять помочитися, а загальний об’єм сечі, що залишилася в сечовому міхурі, потім буде виміряно ультразвуком. Ваш лікар вирішить, чи потрібно вам повертатися на той же тест протягом наступних 12 тижнів. Поговоріть зі своїм лікарем, якщо ви не можете будь -коли помочитися, оскільки вам може знадобитися почати користуватися катетером. У пацієнтів з нетриманням сечі через порушення сечового міхура, пов’язані з травмою спинного мозку або розсіяним склерозом, приблизно одній третині тих, хто не використовував катетер до початку лікування, може знадобитися використання катетера після лікування. У пацієнтів з нетриманням сечі через гіперактивного сечового міхура приблизно 6 із 100 пацієнтів можуть потребувати використання катетера після лікування.
Взаємодії Які препарати або продукти харчування можуть змінити дію ботокса
Повідомте свого лікаря або фармацевта, якщо:
- приймаєте антибіотики (для лікування інфекцій), антихолінестеразні препарати, препарати серцевого ритму або міорелаксанти. Деякі з цих ліків можуть посилювати дію Ботокса.
- Ви нещодавно отримували лікування ліками, що містять ботулінічний токсин (активний інгредієнт у BOTOX), оскільки це може значно посилити ефект BOTOX.
- використовує будь -які антитромбоцитарні засоби (продукти, подібні до аспірину) та / або антикоагулянти (розріджувачі крові).
Повідомте свого лікаря або фармацевта, якщо ви приймаєте або нещодавно приймали інші ліки, включаючи ліки, відпущені без рецепта.
Попередження Важливо знати, що:
Вагітність та годування груддю
Ботокс не слід застосовувати під час вагітності та жінкам репродуктивного віку, які не використовують протизаплідні засоби, якщо це явно не потрібно. Попросіть свого лікаря поради, якщо ви вагітні, плануєте завагітніти або завагітніти під час лікування. Ваш лікар обговорить з вами, чи варто продовжувати лікування.
Ботокс не рекомендується годуючим жінкам.
Попросіть поради у свого лікаря або фармацевта, перш ніж приймати будь -які ліки.
Водіння автомобіля та роботу з машинами
BOTOX може викликати запаморочення, сонливість, втому або проблеми із зором. Якщо ви відчули будь -який з цих ефектів, не керуйте автомобілем та не працюйте з механізмами. Якщо ви не впевнені, зверніться за порадою до лікаря.
Доза, спосіб та час введення Як користуватися ботоксом: дозування
Ботокс слід вводити тільки лікарям, які мають певні навички використання ліків.
Спосіб і шлях введення
BOTOX вводять у м’язи (внутрішньом’язово), у стінку сечового міхура за допомогою спеціального інструменту (цистоскоп) для ін’єкцій у сечовий міхур або в шкіру (внутрішньошкірно). Ваш лікар зазвичай вводить BOTOX у кілька місць у кожній ураженій зоні.
Загальна інформація про дозування
- Кількість ін’єкцій на м’яз та доза змінюються відповідно до показань. Однак ваш лікар вирішить, скільки, як часто і в які м’язи вводити BOTOX. Рекомендується, щоб лікар використав найнижчу ефективну дозу.
- Дози для людей похилого віку такі ж, як і для дорослих.
Дозування Ботокса та тривалість його ефекту змінюються залежно від розладу, від якого ви лікуєтесь. Детально про кожен розлад наведено нижче.
Безпека та ефективність BOTOX у лікуванні постійних м’язових спазмів повік, обличчя, шиї та плечей у дітей (до 12 років) не були продемонстровані. Безпека та ефективність BOTOX у лікуванні хронічної мігрені у дітей (до 18 років) не вивчалися.
Безпека та ефективність препарату Ботокс у лікуванні надмірної пітливості пахв не вивчалися у дітей віком до 12 років. Досвід застосування препарату Ботокс для лікування надмірної пітливості пахв у підлітків віком від 12 до 17 років дуже обмежений.
Ефективність BOTOX у цій віковій групі не підтверджена. Для отримання додаткової інформації зверніться до лікаря.
Безпека та ефективність препарату Ботокс у лікуванні спастичності верхніх кінцівок, пов’язаних з інсультом, не встановлені у дітей та підлітків віком до 18 років.
Безпека та ефективність препарату Ботокс у лікуванні нетримання сечі у педіатричних пацієнтів віком до 18 років не встановлені.
Для стійких м’язових спазмів повіки та обличчя
Дозування
Під час першого сеансу лікування лікар може зробити декілька ін’єкцій в уражені м’язи в кількості від 1,25 до 2,5 одиниць BOTOX у кожне місце ін’єкції.
Максимальна доза для першого сеансу лікування становить 25 одиниць на уражену ділянку (наприклад, на око). Для наступних сеансів лікування максимальну загальну дозу можна збільшити до 100 одиниць, якщо це необхідно.
Тривалість ефекту лікування
Зазвичай ви помітите поліпшення протягом 3 днів після ін'єкції. Максимальний ефект зазвичай спостерігається через 1-2 тижні після лікування.
Коли ефект почне зникати, при необхідності лікування можна повторити, але не частіше ніж кожні 3 місяці.
Для стійких м’язових спазмів шиї та плечей
Дозування
Лікар може зробити декілька ін’єкцій в уражені м’язи до 50 одиниць BOTOX для кожного місця ін’єкції.
Максимальна доза для першого сеансу лікування становить 200 одиниць. Для наступних сеансів лікування максимальну дозу можна збільшити до 300 одиниць.
Тривалість ефекту лікування
Зазвичай ви помітите поліпшення протягом 2 тижнів після ін’єкції.
Максимальний ефект зазвичай спостерігається приблизно через 6 тижнів після лікування.
Коли ефект почне стихати, курс лікування можна повторити за необхідності, але не частіше ніж кожні 10 тижнів.
Для стійких м’язових спазмів зап’ястя та кистей рук у пацієнтів з інсультом
Дозування
Лікар може зробити кілька ін’єкцій в уражені м’язи. Доза та кількість ін’єкцій змінюються залежно від ряду факторів, включаючи ваші потреби, м’язи, що підлягають лікуванню, розмір м’язів, тяжкість спазмів тощо.
Тривалість ефекту лікування
Зазвичай ви помітите поліпшення протягом перших 2 тижнів після ін’єкції.
Максимальний ефект зазвичай спостерігається між 4 і 6 тижнями після лікування.
Коли ефект почне стихати, при необхідності лікування можна повторити, але не частіше ніж кожні 12 тижнів.
При надмірному потовиділенні пахв
Дозування
Ваш лікар може зробити ін’єкції BOTOX у декілька місць в пахвовій області. Загальна доза на пахву становить 50 одиниць BOTOX.
Тривалість ефекту лікування
Зазвичай ви помітите поліпшення протягом першого тижня після ін’єкції.
Ефект зазвичай триває в середньому 7,5 місяців після першої ін’єкції, і приблизно у 1 з 4 пацієнтів все ще спостерігається ефект лікування через рік.
Коли ефект почне стихати, курс лікування можна повторити за необхідності, але не частіше ніж кожні 16 тижнів.
Для стійких спазмів м’язів ніг у дітей з ДЦП
Дозування
Лікар може зробити кілька ін’єкцій в уражені м’язи. Доза буде залежати від ваги дитини.
Тривалість ефекту лікування
Зазвичай ви помітите поліпшення протягом перших 2 тижнів після ін’єкції.
Коли ефект почне зникати, можна повторити наступне лікування, але не частіше ніж кожні 3 місяці.Лікар може знайти дозу, яка виправдовує лікування на відстані до 6 місяців один від одного.
При нетриманні сечі внаслідок гіперактивного сечового міхура
Дозування
Лікар зробить кілька ін’єкцій в стінку сечового міхура. Загальна доза становить 100 одиниць BOTOX. Перед ін’єкціями вам може бути наданий місцевий анестетик (ваш сечовий міхур на деякий час наповниться розчином анестетика, а потім спорожніє.) Вам також можуть дати заспокійливий засіб.
Вам доведеться почекати 30 хвилин після процедури, щоб побачити, чи зможете ви спонтанно помочитися.
Тривалість ефекту лікування
Зазвичай покращення настає протягом перших 2 тижнів ін’єкцій.
Зазвичай ефект зберігається через 5-6 місяців після ін'єкції.
Якщо наслідки починають згасати, ви можете повернутися до лікування, якщо це необхідно, але не частіше ніж кожні 3 місяці.
При нетриманні сечі внаслідок розладів сечового міхура, пов’язаних із травмою спинного мозку або розсіяним склерозом
Дозування
Лікар зробить багаторазові ін’єкції в стінку сечового міхура. Загальна доза становить 200 одиниць BOTOX. Перед ін’єкціями вам може бути наданий місцевий або загальний анестетик. Вам також можуть дати заспокійливий засіб.
Тривалість терапевтичного ефекту
Зазвичай ви помітите поліпшення протягом 2 тижнів після ін’єкції.
Зазвичай ефект зберігається через 8-10 місяців після ін'єкції.
Коли наслідки почнуть згасати, ви можете повернутися до лікування, якщо це необхідно, але не частіше ніж кожні 3 місяці.
Для лікування головного болю у дорослих, які страждають на хронічну мігрень
Дозування
Ваш лікар може зробити кілька ін’єкцій у певні м’язи обличчя, голови та шиї, додавши до 5 одиниць BOTOX у кожне місце ін’єкції. Ін’єкції слід розподілити на 7 певних м’язових ділянок голови / шиї, причому половина кількості ін’єкцій робиться зліва, а половина - з правого боку голови та шиї.
Загальний діапазон дозування становить від 155 до 195 одиниць на сеанс лікування.
Тривалість ефекту лікування
Коли ефект почне зникати, лікування можна повторювати, але не частіше ніж кожні 12 тижнів.
Передозування Що робити, якщо ви прийняли занадто багато ботокса
Ознаки передозування BOTOX можуть не проявлятися протягом кількох днів після ін'єкції. Якщо ви проковтнули BOTOX або випадково ввели його, вам слід звернутися до лікаря, який може спостерігати за вами протягом кількох тижнів.
Якщо ви отримали передозування BOTOX, у вас можуть виникнути деякі з наведених нижче симптомів, і якщо це так, негайно зверніться до лікаря, який вирішить, чи варто звертатися до лікарні:
- утруднення дихання, ковтання або розмови через параліч м’язів;
- їжа або рідини, що випадково потрапили в легені, що може спричинити пневмонію (інфекцію легенів) через параліч м’язів;
- опущення повік, подвійне бачення;
- загальна слабкість.
Якщо у вас виникнуть додаткові запитання щодо застосування препарату Ботокс, зверніться до лікаря або фармацевта.
Побічні ефекти Які є побічні ефекти ботокса
Як і всі ліки, Ботокс може викликати побічні ефекти, хоча вони виникають не у всіх.
Загалом, побічні ефекти виникають протягом перших кількох днів після лікування. Вони зазвичай тривають лише короткий час, але можуть тривати кілька місяців, а в рідкісних випадках - навіть довше.
ЯКЩО У ВАС БУДУТЬ УСИЛКИ ВДИХАННЯ, ГЛАДАННЯ АБО МОВЛЕННЯ ПІСЛЯ ОТРИМАННЯ БОТОКС -ЛІКУВАННЯ, НЕМЕДЛЕННО ЗВЕРНІТЬСЯ ДО ЛІКАРА.
Якщо ви відчуваєте кропив’янку, набряк, включаючи набряк обличчя або горла, хрипи, відчуття слабкості та задишку, негайно зверніться до лікаря.
Побічні ефекти класифікуються за такими категоріями залежно від того, як часто вони виникають:
Нижче наведені побічні ефекти, які змінюються залежно від частини тіла, куди вводиться Ботокс:
Ін’єкції в повіку та обличчя
Дуже поширений побічний ефект:
- опущення повіки.
Поширені побічні ефекти:
- набряк обличчя;
- локальне пошкодження рогівки (чиста поверхня, що закриває передню частину ока);
- утруднення повного закриття ока;
- надмірне сльозотеча;
- роздратування;
- сухість очей, подразнення очей та чутливість до світла;
- синці під шкірою.
Нечасті побічні ефекти:
- запаморочення;
- порушення зору;
- затуманений зір;
- подвійне бачення;
- втома;
- запалення рогівки (чиста поверхня, що покриває передню частину ока);
- слабкість м’язів обличчя;
- розслаблення м’язів однієї сторони обличчя;
- висип;
- ненормальний рух повік всередину або назовні.
Рідкісний побічний ефект:
- набряк повіки.
Дуже рідкісні побічні ефекти:
- виразка, пошкодження рогівки (чиста поверхня, що покриває передню частину ока);
- високий тиск в оці.
Якщо будь -який з побічних ефектів стає серйозним або якщо Ви помітили будь -які побічні ефекти, не зазначені у цій інструкції, повідомте про це свого лікаря або фармацевта.
Ін’єкції в шию і плече
Дуже поширені побічні ефекти:
- утруднення ковтання;
- болить;
- м’язова слабкість.
Поширені побічні ефекти:
- запаморочення;
- синдром грипу;
- сонливість
- судоми м’язів;
- зниження чутливості шкіри;
- відчуття слабкості;
- відчуття загального нездужання;
- нудота;
- головний біль;
- скутість або хворобливість м’язів;
- набряк і подразнення верхніх дихальних шляхів (риніт);
- закладеність носа або нежить, кашель, біль у горлі, лоскотання або подразнення горла;
- сухість у роті.
Нечасті побічні ефекти:
- задишка;
- подвійне бачення;
- лихоманка;
- опущення повіки;
- зміна голосу.
Якщо будь -який з побічних ефектів стає серйозним або якщо Ви помітили будь -які побічні ефекти, не зазначені у цій інструкції, повідомте про це свого лікаря або фармацевта.
Ін’єкції у зап’ястя та кисть у пацієнтів з інсультом
Поширені побічні ефекти:
- м’язова слабкість;
- підвищена м’язова напруга;
- синці та кровотеча під шкірою, що викликають червоні ділянки (синці або пурпура);
- кровотеча або печіння в місці ін’єкції;
- біль в руках і пальцях;
- біль, коли робиться ін’єкція;
- лихоманка;
- синдром грипу.
Нечасті побічні ефекти:
- депресія;
- зниження артеріального тиску при стоянні, що викликає запаморочення, запаморочення або непритомність;
- відчуття запаморочення або «обертання» (запаморочення);
- відсутність координації рухів;
- втрата пам’яті;
- загальна слабкість;
- болить;
- біль у суглобах або запалення;
- зниження чутливості шкіри;
- оніміння або поколювання;
- набряки кінцівок, таких як руки і ноги;
- запалення шкіри (дерматит);
- головний біль;
- відчуття загального нездужання;
- нудота;
- підвищена чутливість в місці ін’єкції;
- висип;
- оніміння або поколювання навколо рота;
- утруднення сну (безсоння);
- свербіж.
Деякі з цих незвичайних побічних ефектів також можуть бути пов'язані з вашим захворюванням.
Якщо будь -який з побічних ефектів стає серйозним або якщо Ви помітили будь -які побічні ефекти, не зазначені у цій інструкції, повідомте про це свого лікаря або фармацевта.
Ін’єкції при надмірному потовиділенні пахв
Дуже поширені побічні ефекти:
- біль у місці ін’єкції.
Поширені побічні ефекти:
- біль у місці ін’єкції;
- головний біль;
- оніміння або поколювання;
- припливи;
- підвищена пітливість в інших місцях, крім пахв;
- ненормальний запах шкіри;
- свербіж;
- втрата волосся;
- набряк під шкірою;
- біль у кінцівках, таких як руки та пальці;
- болить;
- реакції та набряк, кровотеча або печіння та підвищена чутливість у місці ін’єкції.
Нечасті побічні ефекти:
- м’язова слабкість;
- відчуття слабкості;
- м’язові болі;
- проблеми з суглобами;
- нудота.
Якщо будь -який з побічних ефектів стає серйозним або якщо Ви помітили будь -які побічні ефекти, не зазначені у цій інструкції, повідомте про це свого лікаря або фармацевта.
Уколи ногами у дітей з ДЦП
Дуже поширені побічні ефекти:
- вірусна інфекція;
- вушна інфекція.
Поширені побічні ефекти:
- сонливість;
- м’язова слабкість;
- біль в кінцівках, таких як кисті і пальці;
- проблеми в ході;
- оніміння або поколювання;
- м’язові болі;
- нетримання сечі (неможливість контролювати спорожнення сечового міхура);
- відчуття загального нездужання;
- падає;
- висип;
- біль у місці ін’єкції;
- відчуття слабкості.
Були рідкісні повідомлення про смерть після лікування BOTOX, іноді пов'язану з аспіраційною пневмонією у дітей з ДЦП.
Якщо будь -який з побічних ефектів стає серйозним або якщо Ви помітили будь -які побічні ефекти, не зазначені у цій інструкції, повідомте про це свого лікаря або фармацевта.
Ін’єкції в стінку сечового міхура при нетриманні сечі через надмірно активного сечового міхура
Дуже поширені побічні ефекти:
- інфекції сечовивідних шляхів;
- хворобливе сечовипускання після ін’єкції *.
Поширені побічні ефекти:
- бактерії в сечі, лейкоцити в сечі;
- неможливість спорожнити сечовий міхур (затримка сечі);
- неповне спорожнення сечового міхура;
- часте сечовипускання протягом дня;
- кров у сечі після ін’єкції **.
* Цей побічний ефект також може бути пов'язаний з процедурою ін'єкції. ** Цей побічний ефект пов'язаний лише з процедурою ін'єкції
Якщо будь -який з побічних ефектів стає серйозним або якщо Ви помітили будь -які побічні ефекти, не зазначені у цій інструкції, повідомте про це свого лікаря або фармацевта.
Ін’єкції в стінку сечового міхура при нетриманні сечі через порушення сечового міхура, пов’язані з травмою спинного мозку або розсіяним склерозом
Дуже поширені побічні ефекти:
- інфекції сечовивідних шляхів;
- неможливість спорожнити сечовий міхур (затримка сечі).
Поширені побічні ефекти:
- утруднення засинання (безсоння);
- запор;
- м’язова слабкість;
- м'язові спазми;
- кров у сечі після ін’єкцій *;
- хворобливе сечовипускання після ін’єкцій *;
- набряк у стінці сечового міхура (дивертикул сечового міхура);
- втома;
- проблеми з ходьбою (порушення ходи);
- можлива неконтрольована рефлекторна реакція організму (наприклад, рясне потовиділення, пульсуючий головний біль або посилений пульс) приблизно спільно з ін’єкціями (вегетативна дисрефлексія) *;
- падає.
* Деякі з цих поширених побічних ефектів також можуть бути пов'язані з процедурою ін'єкції.
Якщо будь -який з побічних ефектів стає серйозним або якщо Ви помітили будь -які побічні ефекти, не зазначені у цій інструкції, повідомте про це свого лікаря або фармацевта.
Ін’єкції в голову та шию для лікування головного болю у пацієнтів, які страждають на хронічну мігрень
Поширені побічні ефекти:
- головний біль;
- мігрень;
- висип;
- свербіж;
- біль у місці ін’єкції;
- біль у шиї;
- слабкість м’язів обличчя;
- опущення повіки;
- м’язова слабкість;
- м’язові болі;
- м'язові спазми;
- болючість м’язів;
- скутість м’язів.
Нечасті побічні ефекти:
- утруднене ковтання;
- шкірні болі;
- біль у щелепі;
- набряк повік.
Якщо будь -який з побічних ефектів стає серйозним або якщо Ви помітили будь -які побічні ефекти, не зазначені у цій інструкції, повідомте про це свого лікаря або фармацевта.
Загальна інформація про інші побічні ефекти
Про небажані ефекти, пов'язані з поширенням BOTOX на відстані від місця ін'єкції, повідомлялося дуже рідко, і вони включають:
- м’язова слабкість;
- запор;
- утруднене ковтання;
- випадкове потрапляння їжі або рідини в легені, що в деяких випадках може викликати пневмонію.
Утруднення ковтання може коливатися від легкого до важкого і в деяких випадках вимагає лікування. У рідкісних випадках люди помирали через утруднене ковтання.
Побічні ефекти з боку серця повідомлялися рідко:
- нерегулярне серцебиття;
- серцеві напади.
Деякі з цих людей померли. Однак деякі з цих пацієнтів вже мали проблеми з серцем.
Рідко повідомлялося про важкі або негайні алергічні реакції, включаючи:
- кропив’янка;
- набряк, включаючи набряк обличчя або горла;
- брязкальце;
- відчуття непритомності;
- задишка.
Випадки
- судоми або судоми після лікування BOTOX, особливо у пацієнтів, які раніше відчували ці симптоми. Ці ефекти в основному виникали, коли БОТОКС використовувався для лікування стійких спазмів м’язів ніг у дітей з ДЦП.
Як і при будь -якій ін'єкції, можуть бути повідомлені побічні ефекти, пов'язані з інокулятом:
- біль, синці, кровотеча або інфекція в місці ін’єкції;
- оніміння або поколювання;
- зниження чутливості шкіри;
- хворобливість;
- набряк / набряк;
- еритема (почервоніння);
- спека артеріального тиску та непритомність, спричинені болем та / або голкою "тривоги". Після ін’єкції BOTOX у пацієнтів також були:
- лихоманка та грипоподібні симптоми.
У наведеному нижче списку перераховані додаткові небажані ефекти, про які повідомлялося при застосуванні Ботокса, що застосовується при будь -яких захворюваннях, оскільки він надходив у продаж:
- алергічна реакція;
- втрата іннервації до / скорочення введеного м’яза;
- утруднення дихання та / або дихальна недостатність;
- аспіраційна пневмонія (запалення легенів, викликане випадковою аспірацією їжі, напоїв, слини або блювоти);
- хронічні захворювання м’язів (міастенія гравіс);
- затуманений зір;
- утруднення чіткого бачення;
- косоокість;
- непритомність;
- біль / оніміння / або слабкість, що починається в хребті;
- падіння м’язів щодо частини обличчя;
- слабкість м’язів обличчя;
- утруднення руху рук і плечей;
- зниження чутливості шкіри;
- м’язові болі;
- біль у животі;
- діарея, блювота, втрата апетиту;
- лихоманка;
- різні види червоних плямистих висипань;
- відчуття загального нездужання;
- проблеми з розмовою;
- свербіж;
- надмірна пітливість;
- втрата волосся;
- зниження слуху;
- дзвін у вусі;
- відчуття запаморочення або «обертання» (запаморочення);
- оніміння або поколювання.
Якщо будь -який з побічних ефектів стає серйозним або якщо Ви помітили будь -які побічні ефекти, не зазначені у цій інструкції, повідомте про це свого лікаря або фармацевта.
Термін придатності та утримання
Зберігайте Ботокс у недоступному для дітей місці.
Ваш лікар не повинен використовувати BOTOX після закінчення терміну придатності, зазначеного на етикетці після EXP. Термін придатності відноситься до останнього дня місяця.
Зберігати в холодильнику (2 ° C - 8 ° C) або в морозильній камері (-5 ° C або нижче).
Після розчинення рекомендується негайне використання розчину; однак продукт можна зберігати до 24 годин у холодильнику (2 ° C - 8 ° C).
Склад та лікарська форма
Що містить BOTOX
- Діюча речовина: Clostridium botulinum botulinum токсин типу А. Кожен флакон містить 50, 100 або 200 одиниць алергену ботулотоксину типу А.
- Інші інгредієнти - людський альбумін та хлорид натрію.
Опис зовнішнього вигляду BOTOX та вмісту упаковки
BOTOX поставляється у вигляді білого порошку у флаконі з прозорого скла. Перед ін’єкцією продукт слід розчинити у стерильному розчині для ін’єкцій хлориду натрію 9 мг / мл (0,9%).
Упаковки можуть бути з 1, 2, 3 і 6 флаконів. Крім того, BOTOX 50 та 100 одиниць алергену ботулотоксину типу А також присутні в упаковках по 10 флаконів.
Не всі розміри упаковок можна продавати.
Джерело з інформацією про упаковку: AIFA (Італійське агентство з лікарських засобів). Вміст, опублікований у січні 2016 р. Наявна інформація може бути не актуальною.
Щоб мати доступ до найновішої версії, бажано зайти на веб-сайт AIFA (Італійське агентство з лікарських засобів). Відмова від відповідальності та корисна інформація.
01.0 НАЗВА ЛЕКАРСТВЕННОГО ПРОДУКТУ
BOTOX 100 ОДІНЦІВ АЛЛЕРГАНОВИЙ ПОРОШ РОЗЧИНУ ДЛЯ ІНЖЕКЦІЙ
02.0 ЯКІСНИЙ І КІЛЬКІСНИЙ СКЛАД
Ботулінічний токсин * типу А, 100 одиниць алергену у флаконі.
* від Clostridium botulinum
Одиниці ботулотоксину не взаємозамінні від одного продукту до іншого.
Повний список допоміжних речовин див. У розділі 6.1.
03.0 ФАРМАЦЕВТИЧНА ФОРМА
Порошок для розчину для ін’єкцій.
Білий порошок.
04.0 КЛІНІЧНА ІНФОРМАЦІЯ
04.1 Терапевтичні показання
Ботокс призначений для лікування:
• блефароспазм, геміфаціальний спазм та пов’язані з ним вогнищеві дистонії;
• цервікальна дистонія (спазматична кривошия);
• фокусна спастичність:
- пов'язані з динамічною деформацією клишоногості через спастичність у ходячих педіатричних пацієнтів з ДЦП у віці від двох років і старше;
- зап'ястя і кисті у дорослих пацієнтів з інсультом.
• Стійкий та тяжкий первинний гіпергідроз пахв, який перешкоджає нормальній повсякденній діяльності та стійкий до місцевого лікування.
• Нетримання сечі у дорослих пацієнтів з нейрогенною гіперактивністю м’язів детрузора сечового міхура, спричиненим стабілізованим ураженням спинного мозку, починаючи від шийного відділу до нижніх рівнів або з розсіяним склерозом.
• Полегшення симптомів у дорослих пацієнтів, які відповідають діагностичним критеріям хронічної мігрені (головні болі тривалістю ≥ 15 днів на місяць, включаючи щонайменше 8 днів з мігренню) і які виявили недостатню відповідь або мають непереносимість препаратів для профілактики мігрені (див. Розділ 4.4).
04.2 Дозування та спосіб введення
Дозування
Будь ласка, зверніться до конкретних рекомендацій щодо кожної ознаки, описаної нижче.
Одиниці ботулотоксину не можуть бути взаємозамінні від одного продукту до іншого. Рекомендовані дози в одиницях Аллергана відрізняються від доз інших препаратів ботулотоксину.
Важлива наступна інформація: Якщо під час однієї обробки використовуються пачки з різною міцністю BOTOX, будьте особливо обережні, використовуючи потрібну кількість розчинника для відновлення конкретної кількості одиниць на 0,1 мл. Кількість розчинника варіюється між одиницями алергону BOTOX 50, одиницями алергону BOTOX 100 та одиницями алергону BOTOX 200. Кожен шприц повинен бути належним чином маркований.
BOTOX слід відновлювати лише стерильним розчином для ін’єкцій хлориду натрію 9 мг / мл (0,9%). Необхідно набрати правильну кількість розчинника за допомогою шприца (див. Таблицю розведення нижче).
Інструкції щодо розведення 100 флаконів для нетримання сечі через нейрогенну гіперактивність м’язів детрузора сечового міхура:
• Відновіть дві флакони 100 одиниць BOTOX з 6 мл 0,9% неконсервованого фізіологічного розчину і обережно перемішайте флакон.
• Вийміть 4 мл з кожного флакона за допомогою двох різних шприців по 10 мл.
• Вийміть решту 2 мл з кожної флакону за допомогою третього шприца об’ємом 10 мл.
• завершити відновлення, додавши 6 мл 0,9% фізіологічного розчину без консервантів до кожного з трьох шприців по 10 мл і обережно перемішати.
Ви отримаєте три шприци об'ємом 10 мл, що містять загалом 200 одиниць відновленого BOTOX.
Використовувати одразу після розчинення у шприці. Викиньте будь -який невикористаний фізіологічний розчин.
Таблиця розведення для упаковки BOTOX 100 Allergan Unit для всіх інших показань:
Цей продукт призначений лише для одноразового використання, і будь -який невикористаний залишковий розчин слід викинути.
Інструкції щодо використання, поводження та утилізації флаконів див. У розділі 6.6.
Пацієнти літнього віку
Адекватні дослідження дозування не проводилися у пацієнтів літнього віку. Рекомендується вводити найнижчу ефективну дозу з найдовшим клінічно відповідним інтервалом між процедурами. Будьте особливо обережними у пацієнтів літнього віку зі значним анамнезом, які отримують одночасно з іншими ліками.
Педіатричне населення
Безпека та ефективність препарату Ботокс у лікуванні блефароспазму, спазму геміфациалів або цервікальної дистонії не були продемонстровані у дітей (віком до 12 років).
Безпека та ефективність BOTOX у лікуванні нетримання сечі внаслідок гіперактивності нейрогенних детрузорів не встановлені у педіатричній популяції (населення віком до 18 років).
Безпека та ефективність препарату Ботокс при лікуванні хронічної мігрені не вивчалися у педіатричній популяції (населення віком до 18 років).
Безпека та ефективність препарату Ботокс у лікуванні первинного гіпергідрозу пахв не вивчалися у дітей віком до 12 років. Безпека та ефективність Ботокса у підлітків віком від 12 до 17 років при лікуванні важкого пахвового гіпергідрозу не встановлені. Наявні на даний момент дані описані у розділах 4.8 та 5.1, однак жодних рекомендацій щодо дозування зробити не можна (див. Розділи 4.8 та 5.1).
Безпека та ефективність препарату Ботокс у лікуванні спастичності верхніх кінцівок, пов’язаної з інсультом, не встановлені у дітей та підлітків віком до 18 років.
Спосіб введення
Будь ласка, зверніться до конкретних рекомендацій щодо кожної ознаки, описаної нижче.
BOTOX повинні вводити лише кваліфіковані лікарі, які мають досвід роботи з необхідним обладнанням та користування ним.
Оптимальні рівні загальної достовірності не були встановлені для всіх показань дозування та кількості місць ін’єкцій у кожній м’язі. У цих випадках лікар повинен встановити індивідуальні схеми лікування. Оптимальні рівні для дози слід визначити шляхом титрування, але не слід перевищувати максимальну рекомендовану дозу.
Блефароспазм / геміфациальний спазм
Відновлений BOTOX слід вводити за допомогою стерильної голки калібру 27-30 / 0,40-0,30 мм. Електроміографічне керівництво не потрібно. Рекомендована початкова доза становить від 1,25-2,5 одиниць для ін’єкцій у медіальну та бічну ділянку орбікулярного м’яза верхньої повіки та бічну область орбікулярного м’яза нижньої повіки. Додаткові ділянки можуть бути введені в область брів, бічну орбікулярну м’язову область та верхню частину обличчя, якщо спазми в цих областях заважають зору. Уникнення ін’єкцій поблизу м’яза верхньої повіки леватора може зменшити можливість виникнення птозу. Уникнення ін’єкцій у медіальну частину нижня повіка, зменшуючи таким чином дифузію в нижньому косому м’язі, може зменшити ускладнення диплопії.
Загалом, початковий ефект від ін’єкцій спостерігається протягом трьох днів і досягає свого максимуму через 1-2 тижні після лікування. Кожне лікування триває приблизно три місяці, після чого процедуру можна повторити за необхідності. У наступні сеанси доза може бути може бути збільшено вдвічі, якщо відповідь на початкове лікування вважається недостатньою. Однак, мабуть, мало користі від збільшення дози понад 5 одиниць на місце. Початкова доза не повинна перевищувати 25 одиниць на око. Зазвичай ніякої додаткової користі не досягається від лікування частіше ніж раз на три місяці.
При лікуванні блефароспазму загальна доза не повинна перевищувати 100 одиниць протягом 12 -тижневого періоду.
Пацієнтів з геміфаціальним спазмом або розладами сьомого нерва слід лікувати так само, як і з одностороннім блефароспазмом, при необхідності вводячи інші уражені м’язи обличчя.
Дистонія шийки матки
Відновлений BOTOX слід вводити за допомогою голки відповідного розміру (зазвичай 25-30 калібру / 0,50-0,30 мм).
У клінічних випробуваннях лікування дистонії шийки матки, як правило, полягало у введенні БОТОКСу в грудино -ключично -соскоподібну кістку, піднімальні лопатки, луску, спленіус голови, півпінальні, дуже довгі та / або трапецієподібні м’язи. Цей список не є вичерпним. усі м’язи, відповідальні за контроль положення голови, можуть бути залучені і тому потребують лікування.
Маса і ступінь гіпертрофії або атрофії м’язів - це фактори, які необхідно враховувати при виборі відповідної дози. Шаблони активації м’язів можуть спонтанно змінюватися при цервікальній дистонії без зміни клінічного прояву дистонії.
У разі утруднення ізоляції окремих м’язів ін’єкції слід проводити за допомогою електроміографічного керівництва. У перших контрольованих клінічних випробуваннях для визначення безпеки та ефективності препарату для лікування цервікальної дистонії дози відновленого BOTOX коливалися від 140 до 280 одиниць. в середньому близько 240 одиниць.) Як і для будь -якого іншого препарату, початкова доза у нелікованого пацієнта повинна бути найнижчою ефективною дозою. Не слід вводити більше 50 одиниць на кожну ділянку. м'язи Щоб мінімізувати частоту дисфагії, груднино -ключично -соскоподібний не слід вводити двосторонньо. Загалом у перший цикл терапії слід ввести не більше 200 одиниць, вносячи відповідні корекції дози у наступних циклах на основі початкової відповіді.
Не слід перевищувати загальну дозу 300 Одиниць за один сеанс. Оптимальна кількість місць ін’єкції залежить від розміру м’яза.
Клінічне поліпшення зазвичай спостерігається протягом перших двох тижнів після ін'єкції. Максимальна клінічна користь зазвичай настає приблизно через шість тижнів після ін'єкції. Перерви в лікуванні менше 10 тижнів не рекомендуються. Тривалість сприятливого ефекту в клінічних дослідженнях показала істотну мінливість (від 2 до 33 тижнів) з типовою тривалістю приблизно 12 тижнів.
Дитячий церебральний параліч
Відновлений BOTOX слід вводити стерильною голкою 23-26 калібру / 0,60 - 0,45 мм. Продукт вводять у вигляді розділеної дози шляхом одноразових ін’єкцій у медіальну та бічну верхівки ураженого м’яза ікробної кістки. При геміплегії рекомендована загальна загальна доза становить 4 одиниці / кг маси тіла в ураженій кінцівці. При диплегії загальна рекомендована початкова доза становить 6 одиниць / кг маси тіла, розподілених між ураженими кінцівками. Загальна доза не повинна перевищувати 200 одиниць.
Клінічне поліпшення зазвичай настає протягом перших двох тижнів після ін’єкції.
Подальші дози слід вводити, коли клінічний ефект попередньої ін’єкції зменшується, але не частіше ніж раз на три місяці.Режим дозування можна коригувати для досягнення інтервалу щонайменше шести місяців між наступними курсами лікування.
Фокальна спастичність верхньої кінцівки, пов'язана з інсультом
Відновлений BOTOX слід вводити стерильною голкою калібру 25, 27 або 30 для поверхневих м’язів та довшою голкою для більш глибоких м’язів. Для локалізації уражених м’язів може бути корисним використовувати методи електроміографічного наведення або нервову стимуляцію. Кілька місць ін’єкцій забезпечують більш рівномірний контакт BOTOX з зонами іннервації м’язів і особливо корисні у випадку більших м’язів.
Правильна дозування та кількість місць ін’єкції повинні бути адаптовані до індивідуальних потреб, виходячи з розміру, кількості та розташування залучених м’язів, тяжкості спастичності, будь -якої локальної м’язової слабкості та реакції пацієнта на попереднє лікування.
Нижче наведені дози, які вводяться в контрольованих клінічних випробуваннях:
У контрольованих та неконтрольованих відкритих клінічних випробуваннях під час певного курсу лікування використовували дози між 200 та 240 одиницями, розподілені між вибраними м’язами.
У контрольованих клінічних випробуваннях пацієнти проходили спостереження протягом 12 тижнів після одноразового лікування.
Поліпшення м’язового тонусу було помічено протягом 2 тижнів, а найбільший ефект зазвичай спостерігався протягом 4-6 тижнів.
У поточному безконтрольному відкритому дослідженні більшість пацієнтів відступали через інтервал 12-16 тижнів, коли вплив на м’язовий тонус зменшувався.
Ці пацієнти отримали до 4 щеплень з максимальною сукупною дозою 960 одиниць протягом 54 тижнів. Якщо лікар вважає це за доцільне, можна повторно вводити дози, коли ефект від попередньої ін’єкції зменшується. Повторне лікування не слід проводити раніше 12 тижнів. Ступінь і тип спастичності м’язів, наявний під час ринокуляції, може спричинити необхідність дозування регулювання BOTOX та варіації м’язів, що підлягають лікуванню.
Слід використовувати найнижчу ефективну дозу.
Первинний гіпергідроз пахв
Відновлений BOTOX (100 одиниць / 4 мл) вводять за допомогою голки 30 калібру.
50 одиниць BOTOX інокулюються внутрішньошкірно, розподіляються порівну на кількох ділянках приблизно на 1-2 см один від одного, при гіпергідрозі кожної пахви.
Ділянку гіпергідрозу можна визначити, використовуючи стандартні методи фарбування, такі як тест на незначний крохмаль-йодатний тест. Не можна рекомендувати дози більше 50 одиниць на пахву.
Клінічне поліпшення зазвичай настає протягом першого тижня щеплення.
Ботокс можна повторно інокулювати, коли клінічний ефект попередньої ін’єкції зменшується і коли лікуючий лікар вважає це за необхідне. Щеплення не слід повторювати частіше ніж кожні 16 тижнів (див. Розділ 5.1).
Нетримання сечі через нейрогенну гіперактивність детрузора сечового міхура
На час лікування пацієнти не повинні мати інфекцій сечовивідних шляхів.
Антибіотики слід призначати для профілактики за 1–3 дні до початку лікування, у день лікування та 1–3 дні після лікування.
Пацієнтам рекомендується припинити антитромбоцитарну терапію принаймні за 3 дні до процедури ін’єкції. Пацієнтів, які перебувають на антикоагулянтній терапії, необхідно належним чином контролювати, щоб зменшити ризик кровотечі.
Перед ін’єкцією можна виконати внутрішньоміхурову інстиляцію розведеного анестетика (з седацією або без неї) або перейти до загальної анестезії відповідно до місцевої практики діючого медичного закладу. Якщо проводиться місцеве закапування анестетика, сечовий міхур перед наступними етапами процедури ін’єкції необхідно спорожнити та промити стерильним фізіологічним розчином.
Рекомендована доза становить 200 одиниць BOTOX, тобто 1 мл ін'єкцій (~ 6,7 одиниць) у 30 ділянок м'язів детрузора.
Відновлений BOTOX (200 одиниць / 30 мл) вводять у м’яз детрузора за допомогою жорсткого або гнучкого цистоскопа, уникаючи тригону. Залийте в сечовий міхур достатню кількість фізіологічного розчину, щоб отримати "адекватну візуалізацію для ін'єкцій, але уникнути" надмірного розтягнення.
Щоб видалити присутній повітря, ін’єкційну голку потрібно заповнити приблизно 1 мл розчину (залежно від довжини голки) перед початком ін’єкцій.
Введіть голку в м’яз детрузора приблизно на 2 мм і виконайте 30 ін’єкцій по 1 мл кожна (загальний об’єм 30 мл) на відстані 1 см один від одного (див. Схему). призначити повну дозу. Після того, як ін’єкції були зроблені, злийте фізіологічний розчин, який використовується для візуалізації стінки сечового міхура. Спостерігайте за пацієнтом не менше 30 хвилин після ін’єкцій.
Клінічне поліпшення зазвичай спостерігається протягом 2 тижнів. Оцініть можливість повторного введення пацієнтів на новий курс лікування, якщо клінічний ефект від попереднього лікування зменшиться (середня тривалість у клінічних випробуваннях фази III становила 256-295 днів для 200 одиниць BOTOX), але не раніше ніж через 3 місяці попередні ін’єкції в сечовий міхур.
Хронічна мігрень
Діагностика хронічної мігрені та введення препарату Ботокс слід проводити лише під наглядом невропатологів, які мають досвід лікування хронічної мігрені.
Рекомендована доза відновленого BOTOX для лікування хронічної мігрені становить від 155 до 195 одиниць, які вводяться внутрішньом’язово (внутрішньом’язово) за допомогою голки діаметром 30 дюймів 0,5 дюйма з ін’єкціями, розподіленими між 7 певними ділянками м’язів голови та шиї.
Може знадобитися використання голки діаметром 1 дюйм у шийному відділі для пацієнтів з надзвичайно товстими шийними м’язами. За винятком відросткового м’яза, де слід вводити лише одну ділянку (середню лінію), всі інші м’язи потрібно вводити двосторонньо, причому половина ін’єкцій робиться зліва, а половина - з правого боку голови та голови. у разі переважного болючого місця або ділянок, можна вводити подальші ін’єкції в одну або обидві сторони максимум у 3 конкретні групи м’язів (потиличну, скроневу та трапецієподібну), до максимальної дози на одну м’яз.
Рекомендований графік повторної обробки - кожні 12 тижнів.
Дозування Ботокс на м’яз при хронічній мігрені:
За всіма показаннями
У разі невдачі лікування після першого курсу терапії, наприклад, через відсутність через місяць після ін’єкції значного клінічного поліпшення порівняно з вихідним показником, необхідно виконати такі дії:
• клінічна перевірка, яка може включати електроміографічне обстеження у спеціалізованому контексті, дії токсину на м’язи, які вводяться;
• аналіз причин несправності, напр. поганий вибір м’язів для введення, недостатня доза, неправильна техніка введення, поява фіксованої контрактури, занадто слабкі м’язи -антагоністи, утворення антитіл, що нейтралізують токсини;
• переоцінка доцільності лікування ботулотоксином типу А;
• за відсутності побічних ефектів, вторинних до першого курсу лікування, призначити другий курс лікування таким чином: i) коригувати дозу, беручи до уваги аналіз попередньої невдачі терапії; ii) використовувати техніку ЕМГ; і iii) спостерігати інтервал у три місяці між двома наступними курсами терапії.
У разі неефективності терапії або зниження ефекту після повторних ін’єкцій слід застосовувати альтернативні методи терапії.
04.3 Протипоказання
Ботокс протипоказаний:
• у пацієнтів з відомою гіперчутливістю до ботулотоксину типу А або до будь -якої з допоміжних речовин;
• при наявності інфекції в пропонованих місцях ін’єкцій.
Ботокс для лікування нетримання сечі через нейрогенну гіперактивність детрузора сечового міхура також протипоказаний:
• у пацієнтів, які мають інфекції сечовивідних шляхів на час лікування;
• у пацієнтів з гострою затримкою сечі на час лікування, які регулярно не проходять катетеризацію;
• у пацієнтів, які не бажають та / або не можуть розпочати катетеризацію після лікування, якщо це необхідно.
04.4 Спеціальні попередження та відповідні запобіжні заходи щодо використання
Перед введенням BOTOX необхідно знати про відносну нормальну анатомію ураженої ділянки та про будь -яку аномальну анатомічну ситуацію через попередню операцію та інокуляцію раніше пошкоджених анатомічних структур. Повідомлялося про серйозні побічні реакції, включаючи летальні наслідки які отримували неуточнені ін’єкції BOTOX безпосередньо в слинні залози, оролінгвально-глоткову область, стравохід та шлунок У деяких пацієнтів вже існувала дисфагія або значне виснаження.
Не слід перевищувати рекомендовані дози та частоту введення Ботокса.
Рідко повідомлялося про важкі та / або негайні реакції гіперчутливості, включаючи анафілаксію, захворювання сироватки крові, кропив’янку, легкий набряк тканин та задишку. Повідомлялося про деякі з цих реакцій після застосування BOTOX окремо або з іншими продуктами, які, як виявилося, викликають подібні реакції.
Якщо такі реакції виникають, уникайте лікування пацієнта новою ін’єкцією Ботокса та негайно розпочніть відповідну медикаментозну терапію, наприклад, з адреналіном. Повідомлялося про випадок анафілаксії, у якому брав участь пацієнт, який помер після ін’єкції неналежним чином розведеного ботокса 5 мл 1% лідокаїну (див. "Додаткова інформація" у розділі 4.8).
Повідомлялося про побічні реакції через поширення токсину, віддаленого від місця введення (див. Розділ 4.8), що іноді призводить до смерті, іноді пов'язане з дисфагією, пневмонією та / або профузною астенією.
Пацієнти, які отримують терапевтичні дози, можуть відчувати сильну м’язову слабкість. Пацієнти з основними неврологічними розладами, включаючи проблеми з ковтанням, мають підвищений ризик розвитку цих реакцій. Продукт ботулотоксину слід застосовувати таким пацієнтам під наглядом спеціаліста, і його слід застосовувати лише в тому випадку, якщо користь від лікування перевищує ризик. Пацієнтів з анамнезом дисфагії та аспіраційної пневмонії слід лікувати вкрай обережно.
Пацієнтам або особам, які їх опікують, слід порадити негайно звернутися за допомогою у разі ковтання, розмови або дихання.
Також повідомлялося про дисфагію після щеплення в інших місцях, крім шийних м’язів (див. Розділ 4.4 «Дистонія шийки матки»).
Клінічні коливання під час неодноразового застосування BOTOX (як і у випадку всіх ботулінічних токсинів) можуть бути обумовлені різними процедурами відновлення флаконів, інтервалами введення, введеними м’язами та невеликими різними значеннями потенції, що визначаються використовуваним біологічним тестом.
Утворення антитіл, що нейтралізують ботулотоксин типу А, може знизити ефективність лікування БОТОКСОМ через інактивацію біологічної активності токсину. Результати деяких досліджень свідчать про те, що застосування Ботоксу з більш частими інтервалами або у вищих дозах може призвести до більшої частоти утворення антитіл. У разі необхідності потенційний ризик утворення антитіл можна мінімізувати шляхом введення найефективнішої дози. з більшим, клінічно доцільним інтервалом між процедурами.
Як і будь -яке лікування, яке може дозволити пацієнтам, які раніше вели малорухливий спосіб життя, відновити свою діяльність, пацієнту, який малорухливий, слід порекомендувати поступово відновлювати свою діяльність.
Слід бути обережним при застосуванні BOTOX за наявності запалення у вибраному місці (місцях) ін’єкції або за наявності надмірної слабкості або атрофії в м’язах -мішенях. склероз або рухова нейропатія).
Ботокс слід застосовувати з особливою обережністю та під ретельним наглядом у пацієнтів з клінічними або субклінічними ознаками дефектів нервово-м’язової передачі, наприклад, міастенією гравіс або синдромом Ламберта-Ітона; у таких пацієнтів може бути підвищена чутливість до агентів, таких як Ботокс, що може призвести до надмірної м’язової слабкості. Пацієнти з нервово -м’язовими розладами можуть мати підвищений ризик клінічно значущих системних реакцій, включаючи важку дисфагію та порушення дихання, при типовій дозі BOTOX.
Як і будь-яка ін'єкція, можуть виникнути пошкодження, пов'язані з процедурою. Ін’єкція може призвести до локалізованої інфекції, болю, запалення, парестезії, гіпестезії, болючості, набряку, еритеми та / або кровотечі / синяків. тощо. Слід бути обережним при ін’єкції поблизу слабких анатомічних зон.
Повідомлялося про пневмоторакс, пов'язаний з процедурою ін'єкції, після введення BOTOX близько до грудей. Слід бути обережним при ін’єкції поблизу легенів, особливо в апікальній зоні.
Педіатричне застосування
Безпека та ефективність застосування Ботокса у показаннях, відмінних від тих, що описані у розділі 4.1, для педіатричної популяції не встановлені. Постмаркетингові повідомлення про можливе віддалене поширення токсину у педіатричних пацієнтів із супутніми захворюваннями, переважно з паралічем, надходили дуже рідко. Загалом, доза, що використовується в цих випадках, перевищувала рекомендовану (див. Розділ 4.8).
Повідомлялося про рідкісні випадки спонтанної смерті, іноді асоційованої з аспіраційною пневмонією у дітей з тяжкою формою церебрального паралічу після лікування ботулотоксином, включаючи випадки несподіваного застосування (наприклад, область шиї). Необхідно бути гранично обережними при лікуванні пацієнтів, які мають значну неврологічну слабкість, дисфагію або нещодавно перенесли аспіраційну пневмонію або захворювання легенів. Лікування у пацієнтів із поганим базовим станом здоров’я слід проводити лише в тому випадку, якщо потенційна користь для пацієнта перевищує ризики.
Блефароспазм
Зменшення моргання, спричинене введенням ботулінічного токсину в орбікулярний м’яз, може призвести до впливу рогівки, стійкого дефекту епітелію та виразки рогівки, особливо у пацієнтів із розладом 7 -го нерва. Бажано ретельно обстежити чутливість рогівки в попередньо прооперованих очах, уникати ін’єкцій у область нижньої повіки, щоб уникнути ектропіону, та прийняти ефективне профілактичне лікування будь -якого дефекту епітелію. Для цього може знадобитися використання очних крапель, офтальмологічних мазей, м’яких лікувальних контактних лінз або закриття ока бинтом або іншими засобами.
Синці можуть легко виникнути в м’яких тканинах століття. Цього можна звести до мінімуму, обережно стиснувши місце ін'єкції відразу після ін'єкції.
Зважаючи на антихолінергічну активність ботулінічного токсину, слід бути особливо обережним при лікуванні пацієнтів з ризиком розвитку вузькокутової глаукоми, включаючи пацієнтів з анатомічно вузькими кутами.
Дистонія шийки матки
Пацієнтів з цервікальною дистонією слід попередити про можливість дисфагії, яка може бути дуже легкою, але й важкою. Дисфагія може зберігатися протягом 2-3 тижнів після ін'єкції, але описано, що вона триває до 5 місяців після ін'єкції.
Як наслідок дисфагії існує ймовірність аспірації, задишки, а іноді й необхідність годування трубкою. У рідкісних випадках повідомлялося про дисфагію, що супроводжувалася аспіраційною пневмонією та смертю.
Обмеження дози, введеної в грудино -ключично -соскоподібний м’яз, до дози нижче 100 одиниць може зменшити появу дисфагії. Пацієнти з меншою м’язовою масою шиї або пацієнти, які отримують ін’єкції в обидві сторони грудино -ключично -соскоподібного м’яза, описуються як такі, що мають підвищений ризик розвитку дисфагії. Дисфагія пояснюється поширенням токсину в мускулатуру стравоходу. Ін’єкції в м’яз підйому лопатки можуть бути пов’язані з підвищеним ризиком інфекції верхніх дихальних шляхів та дисфагії.
Дисфагія може допомогти зменшити споживання їжі та води, що призведе до втрати ваги та зневоднення. Пацієнти з субклінічною дисфагією можуть мати підвищений ризик розвитку важкої дисфагії після ін’єкції БОТОКС.
Фокальна спастичність, пов'язана з дитячим церебральним паралічем, спастичністю кисті та зап'ястя у дорослих пацієнтів після інсульту
Ботокс - це лікування фокальної спастичності, що вивчається лише у поєднанні з іншими стандартними схемами лікування, і не призначене як заміна таким методам терапії. Ботокс навряд чи буде ефективним для поліпшення діапазону рухів у суглобі з постійною патологічною контрактурою.
Постмаркетингові повідомлення про можливе поширення токсину у педіатричних пацієнтів із супутніми захворюваннями, переважно з ДЦП, надходили рідко. Загалом у цих випадках доза була вищою, ніж рекомендована (див. Розділ 4.8).
Повідомлялося про рідкісні спонтанні повідомлення про смерть, іноді пов'язану з аспіраційною пневмонією у дітей з важким церебральним паралічем після лікування ботулінічним токсином. Особливу обережність слід дотримуватись при лікуванні педіатричних пацієнтів із значними неврологічними вадами, дисфагією або недавньою історією аспіраційної пневмонії або легеневої хвороби.
Первинний гіпергідроз пахв
Для виключення можливих причин вторинного гіпергідрозу (наприклад, гіпертиреозу, феохромоцитоми) слід провести анамнез хвороби та фізичний огляд пацієнта, а також будь -які подальші дослідження, які можуть бути визнані необхідними. Це дозволить уникнути симптоматичного лікування гіпергідрозу без діагностики та / або лікування основних захворювань.
Нетримання сечі внаслідок гіперактивності нейрогенного детрузора
Лікарі повинні бути обережними при проведенні цистоскопії.
У пацієнтів, які не піддаються катетеризації, залишковий об’єм сечі після порожнини слід оцінювати протягом 2 тижнів лікування та періодично відповідно до думки лікаря до 12 тижнів. Пацієнтам слід порадити проконсультуватися з лікарем, якщо у них виникають труднощі з сечовипусканням, оскільки може знадобитися катетеризація.
Може виникнути вегетативна дисрефлексія, пов'язана з процедурою. Можливо, буде потрібно негайне обстеження пацієнта, якого лікують.
Хронічна мігрень
Безпека та ефективність не встановлені у профілактиці головних болів у пацієнтів з епізодичною мігренью (головні болі при хронічному головному болі напруженого типу). Безпека та ефективність препарату Ботокс у пацієнтів із головним болем від надмірного вживання лікарських засобів (вторинний головний біль) не вивчалися.
04.5 Взаємодія з іншими лікарськими засобами та інші форми взаємодії
Теоретично, ефект ботулінічного токсину може бути посилений аміноглікозидними антибіотиками або спектиноміцином або іншими препаратами, що перешкоджають нервово -м’язовій передачі (наприклад, нервово -м’язові блокатори).
Ефект від одночасного введення або протягом кількох місяців застосування різних серотипів нейротоксину ботуліну невідомий. Введення іншого ботулотоксину до завершення дії раніше введеного ботулотоксину може спричинити погіршення нервово -м’язової слабкості.
Досліджень взаємодії не проводилося. Не повідомлялося про взаємодії, що мають клінічне значення.
04.6 Вагітність та лактація
Вагітність
Немає адекватних даних про застосування ботулотоксину типу А у вагітних жінок. Дослідження на тваринах показали репродуктивну токсичність (див. Розділ 5.3). Потенційний ризик для людини невідомий. Ботокс не слід застосовувати під час вагітності та жінкам в дітородному віці вік, які не використовують контрацептиви, якщо це не є крайньою необхідністю.
Час годування
Інформації про виділення BOTOX у молоко немає. Застосування BOTOX у період годування груддю не рекомендується.
Родючість
Немає належних даних про вплив на фертильність внаслідок застосування ботулотоксину типу А у фертильних жінок. Дослідження на щурах обох статей показали зниження фертильності (див. Розділ 5.3).
04.7 Вплив на здатність керувати автомобілем та працювати з механізмами
Досліджень щодо здатності керувати транспортними засобами та працювати з механізмами не проводилося, проте Ботокс може спричинити астенію, м’язову слабкість, запаморочення та порушення зору, що може вплинути на керування автомобілем та роботу з механізмами.
04.8 Побічні ефекти
Загальні
У контрольованих клінічних випробуваннях побічні ефекти, які, на думку дослідників, пов’язані з BOTOX, були зареєстровані у 35% пацієнтів з блефароспазмом, у 28% пацієнтів з цервікальною дистонією, у 17% пацієнтів з дитячим церебральним паралічем, у 11% пацієнтів з первинного пахвового гіпергідрозу та у 16% пацієнтів з осередковою спастичністю верхніх кінцівок, пов’язаною з інсультом. друге лікування. У клінічних дослідженнях щодо хронічної мігрені частота склала 26% при першому лікуванні і знизилася до 11% при другому лікуванні.
Загалом, побічні реакції виникають протягом перших кількох днів після ін’єкції і, як правило, минущі, можуть тривати кілька місяців, а в рідкісних випадках - довше.
Локалізована м’язова слабкість являє собою очікуваний фармакологічний ефект ботулотоксину в м’язовій тканині.
Як і очікувалося для будь -якої процедури ін’єкції, ін’єкція пов’язана з локалізованим болем, запаленням, парестезією, гіпестезією, хворобливістю, набряком / набряком, еритемою, локалізованою інфекцією, кровотечею та / або синяками. Вазовагальна відповідь, включаючи минущу симптоматичну гіпотензію та непритомність, також повідомлялося про синдром лихоманки та грипу після щеплення ботулотоксином.
Побічні реакції - частота за показаннями
Нижче наведено частоту побічних реакцій за ознаками, задокументовану під час клінічних випробувань.
Частота визначається так: дуже часто (> 1/10); поширені (> 1/100 до 1/1000 до 1/10000 до
Блефароспазм / Напівфаміальний спазм
Розлади нервової системи
Нечасто: запаморочення, парез обличчя та параліч обличчя.
Очні розлади
Дуже часто: птоз повік.
Часто: точковий кератит, лагофтальм, сухість очей, світлобоязнь, подразнення очей та посилення сльозотечі.
Нечасто: кератит, ектропіон, диплопія, ентропіон, порушення зору та помутніння зору.
Рідко: набряк повіки.
Дуже рідко: виразковий кератит, зміна епітелію рогівки, перфорація рогівки.
Порушення з боку шкіри та підшкірної клітковини
Поширені: синці.
Нечасто: висип / дерматит.
Загальні розлади та стан на місці введення
Поширені: роздратування обличчя та набряк.
Нечасто: виснаження.
Дистонія шийки матки
Інфекції та інвазії
Поширені: риніт та інфекція верхніх дихальних шляхів.
Розлади нервової системи
Часто: запаморочення, гіпертонус, гіпестезія, сонливість та головний біль.
Очні розлади
Нечасто: диплопія та птоз повік.
Порушення дихання, грудної клітки та середостіння
Нечасто: задишка та дисфонія.
Шлунково -кишкові розлади
Дуже часто: дисфагія (див. Розділ «Додаткова інформація»).
Поширені: сухість у роті та нудота.
Порушення опорно -рухового апарату та сполучної тканини
Дуже часто: м’язова слабкість.
Поширені: скелетно -м’язова скутість і хворобливість.
Загальні розлади та стан на місці введення
Дуже часто: біль.
Поширені: астенія, грипоподібні симптоми та нездужання.
Нечасто: лихоманка.
Дитячий церебральний параліч
Інфекції та інвазії
Дуже часто: вірусна інфекція та інфекція вуха.
Розлади нервової системи
Поширені: сонливість, некоординована ходьба та парестезії.
Порушення з боку шкіри та підшкірної клітковини
Поширені: шкірні висипання.
Порушення опорно -рухового апарату та сполучної тканини
Часто: міалгія, м’язова слабкість і біль у кінцівках.
Ниркові та сечові розлади
Часто: нетримання сечі.
Травми, отруєння та процедурні ускладнення
Поширені: падіння.
Загальні розлади та стан на місці введення
Поширені: нездужання, біль у місці ін’єкції та астенія.
Фокальна спастичність верхньої кінцівки, пов'язана з інсультом
Психічні розлади
Нечасто: депресія та безсоння.
Розлади нервової системи
Часто: гіпертонус.
Нечасто: гіпестезія, головний біль, парестезія, порушення координації та амнезія.
Порушення у вусі та лабіринті
Нечасто: запаморочення.
Судинні патології
Нечасто: ортостатична гіпотензія.
Шлунково -кишкові розлади
Нечасто: нудота в роті та парестезії.
Порушення з боку шкіри та підшкірної клітковини
Поширені: екхімоз та пурпура.
Нечасто: дерматит, свербіж та висип.
Порушення опорно -рухового апарату та сполучної тканини
Часто: біль у кінцівках і м’язова слабкість.
Нечасто: артралгія та бурсит.
Загальні розлади та стан на місці введення
Поширені: біль у місці ін’єкції, лихоманка, синдром грипу, крововилив та подразнення в місці ін’єкції.
Нечасто: астенія, біль, гіперчутливість у місці ін’єкції, нездужання та периферичні набряки.
Деякі незвичні події можуть бути пов’язані з хворобою.
Первинний гіпергідроз пахв
Розлади нервової системи
Часто: головний біль та парестезія.
Судинні патології
Поширені: припливи.
Шлунково -кишкові розлади
Нечасто: нудота.
Порушення з боку шкіри та підшкірної клітковини
Поширені: гіпергідроз (не пахвова пітливість), аномальний запах шкіри, свербіж, підшкірна грудка та облисіння.
Порушення опорно -рухового апарату та сполучної тканини
Поширені: біль у кінцівках.
Нечасто: м’язова слабкість, міалгія та артропатія.
Загальні розлади та стан на місці введення
Дуже часто: біль у місці ін’єкції.
Часто: біль, набряк у місці ін’єкції, крововилив у місце ін’єкції, гіперчутливість у місці ін’єкції, подразнення в місці ін’єкції, астенія та реакції в місці ін’єкції.
Під час лікування первинного пахвового гіпергідрозу спостерігалося збільшення неаксилярного поту у 4,5% пацієнтів протягом 1 місяця після щеплення, без прямого посилання на анатомічні ділянки.
Цей ефект вирішився приблизно у 30% пацієнтів протягом 4 місяців.
Слабкість верхніх кінцівок також повідомлялася як нечаста (0,7%), легка, минуща, що не потребує лікування і проходить без наслідків. Ця побічна реакція може бути пов’язана з лікуванням, технікою ін’єкції або з обома.
Крім того, може знадобитися переоцінити методику інокуляції під час наступних процедур, щоб забезпечити внутрішньошкірне позиціонування інокуляту.
У неконтрольованому дослідженні безпеки з використанням BOTOX (50 ОД на пахву) у педіатричних пацієнтів віком від 12 до 17 років (N = 144) побічні реакції, що виникали у більш ніж одного пацієнта (кожні 2 пацієнти), включали біль у місці ін’єкції та гіпергідроз ( не пахвова пітливість).
Нетримання сечі через нейрогенну гіперактивність детрузора сечового міхура
Інфекції та інвазії
Дуже часто: інфекції сечовивідних шляхів.
Психічні розлади
Поширені: безсоння.
Шлунково -кишкові розлади
Поширені: запор.
Порушення опорно -рухового апарату та сполучної тканини
Поширені: м’язова слабкість, м’язовий спазм.
Ниркові та сечові розлади
Дуже часто: затримка сечі.
Поширені: гематурія *, дизурія *, дивертикул сечового міхура.
Загальні розлади та стан на місці введення
Поширені: втома, порушення ходьби.
Травми, отруєння та процедурні ускладнення
Поширені: вегетативна дисрефлексія *, падіння.
* побічні реакції, пов'язані з процедурою
У клінічних дослідженнях інфекції сечовивідних шляхів були зареєстровані у 49,2% пацієнтів, які отримували 200 ОД BOTOX, і у 35,7% пацієнтів, які отримували плацебо (53,0% пацієнтів із розсіяним склерозом, які отримували 200 ОД, у порівнянні з 29,3%, які отримували плацебо; 45,4 % пацієнтів з травмою спинного мозку, які отримували 200 ОД порівняно з 41,7%, які отримували плацебо). Затримка сечі повідомлялася у 17,2% пацієнтів, які отримували 200 ОД BOTOX, і у 2,9% пацієнтів, які отримували плацебо (28,8% пацієнтів із розсіяним склерозом, які отримували 200 ОД, у порівнянні з 4,5%, які отримували плацебо; 5,4% пацієнтів з травми спинного мозку, які отримували 200 ОД проти 1,4%, які отримували плацебо).
При повторному дозуванні не спостерігалося змін у типі побічних реакцій.
У ключових дослідженнях не було різниці у щорічній частоті спалахів розсіяного склерозу (РС) (тобто кількість спалахів РС на рік у пацієнта) (BOTOX = 0,23, плацебо = 0,20).
Серед пацієнтів, які до початку лікування не були катетеризовані, катетеризацію розпочали у 38,9% після лікування 200 одиницями BOTOX порівняно з 17,3% з плацебо.
Хронічна мігрень
Розлади нервової системи
Часто: головний біль, мігрень, парез обличчя.
Очні розлади
Поширені: птоз повік.
Порушення з боку шкіри та підшкірної клітковини
Поширені: свербіж, висип.
Нечасто: біль у шкірі.
Порушення опорно -рухового апарату та сполучної тканини
Поширені: біль у шиї, міалгія, м’язово -скелетні болі, артралгія, м’язово -скелетні болі, м’язові спазми, скутість м’язів та м’язова слабкість.
Нечасто: біль у щелепі.
Загальні розлади та стан на місці введення
Часто: біль у місці ін’єкції.
Шлунково -кишкові розлади
Нечасто: дисфагія.
Рівень припинення через побічні ефекти у цих дослідженнях фази III становив 3,8% для BOTOX та 1,2% для плацебо.
Подальша інформація
Дисфагія коливається від легкої до важкої, з можливістю аспірації, яка іноді потребує медичної допомоги (див. Розділ 4.4).
Побічні реакції (надмірна м’язова слабкість, дисфагія, запор, аспіраційна / аспіраційна пневмонія, у деяких випадках з летальним результатом), пов’язані з дифузією токсину, віддаленого від місця введення, повідомлялися рідко (див. Розділ 4.4).
Оскільки ліки були на ринку, повідомлялося про такі інші побічні реакції: денервація / атрофія м’язів; пригнічення дихання та / або дихальна недостатність; аспіраційна пневмонія; дизартрія; косоокість, периферична нейропатія; біль у животі; затуманений зір; порушення зору; лихоманка; параліч обличчя; парез обличчя; гіпестезія; нездужання; міалгія; свербіж; гіпергідроз; алопеція (включаючи мадароз); діарея; анорексія; втрата слуху; шум у вухах; запаморочення; радикулопатія; непритомність; міастенія гравіс; парестезії; багатоформна еритема; псоріазиформний дерматит; блювота і плечова плексопатія.
Повідомлялося також про рідкісні повідомлення про побічні ефекти, що впливають на серцево -судинну систему, включаючи аритмії та інфаркт міокарда, деякі з яких були смертельними. Деякі з цих пацієнтів мали фактори ризику, включаючи серцево -судинні захворювання.
Рідко повідомлялося про важкі та / або негайні реакції гіперчутливості, такі як анафілаксія та захворювання сироватки крові, а також інші прояви гіперчутливості, включаючи кропив’янку, набряк м’яких тканин та задишку. інші агенти, які, як відомо, викликають подібні реакції.
Дуже рідко повідомлялося про закритокутову глаукому після лікування блефароспазму ботулотоксином.
Були повідомлення про початкові або повторні судоми, особливо у пацієнтів, схильних до таких реакцій. Точний зв’язок цих подій з ін’єкціями ботулотоксину не встановлений.
У дітей такі реакції повідомлялися переважно у осіб з ДЦП, які лікувалися від спастичності.
Біль, пов'язаний із застосуванням голки та / або тривога, може викликати вазовагальну реакцію.
04.9 Передозування
Концепція передозування BOTOX є відносною і залежить від дози, місця ін’єкції та фонових характеристик тканини. Випадків системної токсичності після випадкового щеплення BOTOX не спостерігалося. Надмірні дози можуть призвести до місцевого або віддаленого, генералізованого та глибокого нервово -м’язового паралічу.
Випадків прийому BOTOX всередину не зафіксовано.
Ознаки та симптоми передозування не виявляються одразу після ін’єкції. У разі випадкової ін’єкції або прийому всередину або підозри на передозування пацієнта слід протягом кількох тижнів клінічно контролювати на наявність будь -яких ознак та симптомів м’язової слабкості, які можуть бути локальними або віддаленими від місце ін'єкції, яке може включати птоз, диплопію, дисфагію, дизартрію, генералізовану астенію або дихальну недостатність. Ці пацієнти повинні пройти подальшу медичну оцінку та негайно призначити відповідне медичне лікування, яке також може потребувати госпіталізації.
Якщо уражені м’язи ротоглотки та стравоходу, може виникнути аспірація, що може призвести до розвитку аспіраційної пневмонії. У разі паралічу дихальних м’язів або достатнього ослаблення необхідно буде вдатися до інтубації та допоміжного дихання до одужання, а також потребувати трехеостомії та тривалої штучної вентиляції легенів на додаток до іншого загального підтримуючого лікування.
05.0 ФАРМАКОЛОГІЧНІ ВЛАСТИВОСТІ
05.1 Фармакодинамічні властивості
Фармакотерапевтична група: інші міорелаксанти периферичної дії.
Код ATC M03A X01
Ботулінічний токсин типу А блокує периферичне вивільнення ацетилхоліну в пресинаптичних холінергічних нервових закінченнях, порушуючи вивільнення SNAP-25, білка, який доповнює успішне збирання та вивільнення ацетилхоліну з везикул, розташованих у нервових закінченнях.
Після ін'єкції відбувається початкове швидке високоафінне зв'язування токсину з специфічними рецепторами клітинної поверхні, що супроводжується перенесенням токсину через плазматичну мембрану шляхом опосередкованого рецепторами ендоцитозу. Нарешті, токсин вивільняється в цитозоль.
Цей останній процес супроводжується прогресуючим пригніченням вивільнення ацетилхоліну, і клінічні ознаки виникають протягом 2-3 днів, максимальний ефект спостерігається протягом 5-6 тижнів після ін’єкції.
Відновлення після внутрішньом'язового щеплення зазвичай відбувається протягом 12 тижнів після ін'єкції, оскільки нервові закінчення регенеруються і знову з'єднуються з кінцевими пластинками. Після внутрішньошкірного щеплення, де мішенню є екзокринні потові залози, ефект тривав у середньому 7,5 місяців після першої ін'єкції у пацієнтів, які отримували 50 одиниць на пахвову западину. Однак у 27,5% пацієнтів тривалість ефекту становила 1 рік або більше. Відновлення симпатичних нервових закінчень потових залоз після внутрішньошкірного щеплення БОТОКС не вивчалося.
BOTOX після внутрішньотрусової ін’єкції впливає на еферентні шляхи самої активності детрузора, пригнічуючи вивільнення ацетилхоліну. Крім того, BOTOX може пригнічувати вивільнення аферентних нейромедіаторів та шляхи чутливості.
КЛІНІЧНІ ДОСЛІДЖЕННЯ
Первинний гіпергідроз пахв
Подвійне сліпе, багатоцентрове клінічне дослідження було проведено у пацієнтів, які мали персистуючий двосторонній первинний пахвовий гіпергідроз, встановлений на початку, за допомогою гравіметричного вимірювання, що дорівнює щонайменше 50 мг спонтанного поту, виробленого кожною пахвою протягом більше 5 хвилин при кімнатній температурі, відпочити. Триста двадцять пацієнтів були рандомізовані для отримання 50 одиниць BOTOX (N = 242) або плацебо (N = 78). Пацієнти -респонденти були визначені такими, що мали зменшення від вихідного рівня щонайменше на 50% у пахвовій пітливості.
На першому кінцевому етапі, через 4 тижні після ін’єкції, частота відповіді у групі, яка отримувала БОТОКС, становила 93,8% порівняно з 35,9% у пацієнтів, які отримували плацебо (p
Частота пацієнтів, які відповіли, серед пацієнтів, які отримували BOTOX, продовжувала бути значно вищою (стор
У відкритому подальшому клінічному дослідженні було включено 207 відповідних пацієнтів, які отримали до 3 процедур BOTOX. Зокрема, 174 пацієнти завершили повну 16-місячну тривалість 2 об'єднаних досліджень (4-місячне подвійне сліпе дослідження та 12-місячне спостереження за відкритим дослідженням). Частота клінічної відповіді на 16 тижні після першого ( n = 287), друге (n = 123) та третє (n = 30) лікування становили відповідно 85,0%, 86,2% та 80%. Середня тривалість ефекту на основі комбінованого одноразового продовження дослідження та відкритого дослідження становила 7,5 місяців від першого лікування; крім того, у 27,5% пацієнтів тривалість ефекту тривала 1 рік або більше.
Досвід клінічних випробувань щодо застосування Ботокса при пахвовому гіпергідрозі у дітей віком від 12 до 18 років обмежений.
Однорічне, однорічне, неконтрольоване дослідження безпеки повторної дози було проведено в США у педіатричних пацієнтів віком 12-17 років (N = 144) з важким первинним гіпергідрозом пахвових западин. Пацієнти були переважно жінками (86,1%) та європеоїдами (82,6%). Пацієнтів лікували у дозі 50 ОД на пахву, загалом 100 ОД на пацієнта за одне лікування. Однак жодних досліджень дозування у підлітків не проводилося, тому рекомендації щодо дозування не можуть бути надані. Ефективність та безпека застосування BOTOX у цій групі пацієнтів остаточно не встановлені.
Нетримання сечі внаслідок гіперактивності нейрогенного детрузора
Два багатоцентрові, рандомізовані, подвійні сліпі, плацебо-контрольовані клінічні випробування III фази були проведені у пацієнтів з нетриманням сечі через надмірну активність нейрогенного детрузора, здатного до спонтанного сечовипускання або за допомогою катетера. Всього було зараховано 691 пацієнта з травмою спинного мозку або розсіяним склерозом, які не отримували належного лікування принаймні одним антихолінергічним засобом. Ці пацієнти були рандомізовані для отримання 200 одиниць BOTOX (n = 227), 300 одиниць BOTOX (n = 223) або плацебо (n = 241).
В обох дослідженнях фази III було відзначено значні поліпшення на користь BOTOX (200 одиниць та 300 одиниць) у порівнянні з плацебо у первинній змінній ефективності зміни тижневої частоти нетримання сечі на вихідний рівень на момент виявлення первинної ефективності на 6 тижні, включаючи відсоток пацієнтів без епізодів нетримання сечі. Значні поліпшення спостерігалися в уродинамічних параметрах, включаючи збільшення максимальної цистометричної ємності та зниження пікового тиску детрузора під час першого мимовільного скорочення детрузора. Також спостерігалося поліпшення. Значне, порівняно з плацебо, у оцінках, повідомлених пацієнтами якість життя, пов'язана зі здоров'ям та нетриманням мочі, що вимірюється за допомогою опитувальника якості нетримання сечі (I-QOL) (включаючи обмеження поведінки уникнення, "психосоціальний вплив та" соціальне збентеження). Ніякої додаткової користі з 300 одиницями BOTOX не було виявлено порівняно з 200 одиницями, а більш сприятливий профіль безпеки спостерігався з 200 одиницями BOTOX.
Нижче наведені результати ключових досліджень із зведеними даними:
Первинні та вторинні кінцеві точки на вихідному рівні та відхилення від вихідного рівня у об’єднаних основних дослідженнях:
Середня тривалість відповіді у двох ключових дослідженнях на основі запиту на повторне лікування становила 256-295 днів (36-42 тижні) для групи з 200 дозовими одиницями порівняно з 92 днями (13 тижнів) з плацебо.
Для всіх кінцевих показників ефективності пацієнти мали відповіді, відповідні повторному лікуванню.
У ключових дослідженнях жоден із 475 пацієнтів з надмірною активністю нейрогенного детрузора у досліджуваних зразках не виробляв нейтралізуючих антитіл.
Хронічна мігрень
BOTOX блокує вивільнення нейромедіаторів, пов'язаних з патогенезом болю. Механізм дії BOTOX для полегшення симптомів при хронічній мігрені до кінця не вивчений.
Клінічні та доклінічні фармакодинамічні дослідження показують, що Ботокс пригнічує периферичну сенсибілізацію, тому, ймовірно, також пригнічує центральну сенсибілізацію.
У наведеній нижче таблиці наведені основні результати, отримані в результаті об’єднаного аналізу ефективності після двох курсів лікування BOTOX з інтервалом у 12 тижнів у двох клінічних випробуваннях фази III у пацієнтів з хронічною мігренью, які протягом базового періоду протягом 28 днів мали не менше 4 епізодів та страждав від головного болю ≥ 15 днів (принаймні 4 години безперервного головного болю), принаймні 50% днів головного болю як для мігрені, так і для ймовірної мігрені.
Хоча дослідження не мали достатнього значення для демонстрації відмінностей підгруп, ефект лікування виявився меншим у чоловічої (N = 188) та некавказької (N = 137) пацієнтів, ніж у всій досліджуваній популяції.
05.2 Фармакокінетичні властивості
Загальна характеристика діючої речовини
Дослідження розподілу, проведені на щурах, показали повільну дифузію м’язів комплексу нейротоксинів 125I-ботуліну типу А у м’яз шлунково-кишкового м’яза після ін’єкції з подальшим швидким системним метаболізмом та виведенням із сечею. Кількість радіоактивно міченого матеріалу в м’язах зменшилася з періодом напіврозпаду приблизно 10 год. У місці ін’єкції радіоактивність була зв’язана з великими молекулами білка, тоді як у плазмі-з малими молекулами, що свідчить про швидкий системний метаболізм субстрату. Протягом 24 годин після введення 60% радіоактивності виводилося з сечею. Ймовірно, токсин метаболізується протеазами, а молекулярні компоненти переробляються нормальними метаболічними шляхами.
Через природу продукту класичні дослідження поглинання, розподілу, біотрансформації та усунення активного начала не проводилися.
Характеристика у пацієнтів
Вважається, що терапевтичні дози BOTOX спричиняють поганий системний розподіл. Клінічні дослідження, проведені за допомогою методів електроміографії з одним волокном, продемонстрували підвищену нервово-м’язову електрофізіологічну активність у м’язах, віддалених від місця ін’єкції, що не супроводжується жодними клінічними ознаками чи симптомами.
05.3 Дані доклінічної безпеки
Дослідження репродукції
Піддаючи вагітних мишей, щурів та кроликів внутрішньом’язовим ін’єкціям BOTOX протягом періоду органогенезу, рівень видимих небажаних побічних ефектів (NOAEL) на розвиток становив 4, 1 та 0,125 одиниць / кг відповідно. Більші дози були пов’язані зі зменшенням у кролів спостерігали масу тіла плода та / або затримку окостеніння та аборти.
Родючість і відтворення
Піддаючи самцям та самкам щурам внутрішньом’язові ін’єкції BOTOX, репродуктивний NOEL становив 4 та 8 одиниць / кг відповідно. Більш високі дози були пов'язані з дозозалежним зниженням фертильності.
Після запліднення не було жодного негативного впливу на кількість чи життєздатність ембріонів, бажаних або зачаттях від оброблених самців та самок щурів.
Інші дослідження
На додаток до репродуктивних токсикологічних досліджень, для BOTOX були проведені такі доклінічні дослідження безпеки: гостра токсичність, токсичність при повторних дозах, місцева толерантність, мутагенність, антигенність, сумісність з кров’ю людини. Ці дослідження не виявили особливих ризиків для людини при клінічно значущих рівнях дози. Максимальна рекомендована доза для сеансу лікування становить 300 одиниць (що відповідає 6 одиницям / кг на людину вагою 50 кг). Опублікований внутрішньом’язовий LD50 у молодих мавп становить 39 одиниць / кг.
Системної токсичності не було виявлено після одноразової інтрадетрузіальної ін’єкції передміхурової залози та проксимальної частини прямої кишки, насіннєвого міхура та стінки сечового міхура або матки мавпи (~ 3 одиниці / кг) без побічних ефектів. 9 місяців при повторних дозах, введених у м’яз детрузора (4 ін'єкції), спостерігався птоз із 24 одиницями / кг та смертність при дозах ≥24 одиниць / кг. Дегенерація / регенерація м'язових волокон спостерігалася у скелетних м'язах тварин, яким вводили дозу щонайменше 24 одиниць / кг. Ці міопатичні зміни вважалися вторинними наслідками системного впливу. Крім того, у однієї тварини, яка зазнала дозування 12 одиниць / кг, спостерігалася дегенерація м’язових волокон. Ураження у цієї тварини мало мінімальний ступінь тяжкості і вважалося, що воно не пов’язане з будь -якими клінічними проявами. Не вдалося з упевненістю визначити, чи пов’язано це з лікуванням БОТОКС. Доза 12 одиниць / кг відповідає втричі більшому впливу BOTOX, ніж рекомендована клінічна доза 200 одиниць при нетриманні сечі через нейрогенну гіперактивність м’яза детрузора (у людини вагою 50 кг).
06.0 ФАРМАЦЕВТИЧНА ІНФОРМАЦІЯ
06.1 Допоміжні речовини
Альбумін людини
Хлористий натрій
06.2 Несумісність
За відсутності досліджень сумісності цей лікарський засіб не можна змішувати з іншими продуктами.
06.3 Строк дії
3 роки.
Мікробіологічні дослідження та дослідження потенції показали, що продукт може зберігатися до 5 днів при температурі 2 ° -8 ° C після розчинення.
Тривалість зберігання та умови зберігання перед використанням є відповідальністю користувача, і вони не повинні тривати більше 24 годин при температурі від 2 ° C до 8 ° C.
Після розчинення у флаконі стабільність продукту була продемонстрована протягом 24 годин при температурі від 2 ° C до 8 ° C.
06.4 Особливі умови зберігання
Зберігати в холодильнику (2 ° C - 8 ° C) або в морозильній камері (-5 ° C або нижче).
Щодо умов зберігання відновленого лікарського засобу, див. Розділ 6.3.
06.5 Характер негайної упаковки та вміст упаковки
Флакон із безбарвного скла типу I, номінальною ємністю 10 мл, оснащений пробкою з хлоробутилової гуми та алюмінієвим ущільнювачем.
Упаковки можуть містити 1, 2, 3, 6 або 10 флаконів.
Не всі розміри упаковок можна продавати.
06.6 Інструкції з використання та поводження
Рекомендується відновлювати флакон і готувати шприц поверх пластифікованого абсорбуючого паперу, щоб зібрати будь -який розлитий продукт.
BOTOX слід відновлювати лише стерильним розчином для ін’єкцій хлориду натрію 9 мг / мл (0,9%). Відповідну кількість розріджувача слід набрати за допомогою шприца (див. Розділ 4.2 для вказівок щодо розведення при нетриманні сечі через нейрогенну гіперактивність м’яза детрузора).
Таблиця розведення для упаковки BOTOX 100 Allergan Unit для всіх інших показань:
Якщо під час однієї обробки використовуються пачки з різною міцністю BOTOX, будьте особливо обережні, використовуючи потрібну кількість розчинника для відновлення конкретної кількості одиниць на 0,1 мл. Кількість розчинника варіюється між одиницями алергону BOTOX 100 та одиницями алергону BOTOX 200. Кожен шприц повинен бути належним чином маркований.
Оскільки BOTOX денатурирується шляхом випаровування або інтенсивного перемішування, розчинник слід повільно вводити у флакон. Флакон слід викинути, якщо сила його вакууму не така, щоб втягнути розчинник у флакон. Відновлений BOTOX повинен бути прозорим безбарвним або блідо -жовтим розчином, без частинок. Відновлений розчин перед використанням необхідно візуально перевірити на прозорість та відсутність частинок. Після розчинення у флаконі, BOTOX можна зберігати в холодильнику (2-8 ° C) до 24 годин перед використанням. Дата та час розчинення повинні бути зазначені у вільному місці на етикетці.
При подальшому розведенні BOTOX від нетримання сечі в шприці, його слід негайно використати. Цей продукт призначений лише для одноразового застосування, і будь -який залишковий невикористаний розчин слід викинути.
З міркувань безпеки невикористані флакони слід розчинити з невеликою кількістю води і потім автоклавувати. Будь -які невикористані флакони, шприци та розсипаний матеріал слід автоклавувати або залишити будь -який залишковий БОТОКС за допомогою розчину гіпохлориту натрію (0,5%) протягом 5 хвилин.
Невикористані ліки та відходи, отримані з цього препарату, слід утилізувати відповідно до місцевих правил.
07.0 ВЛАСНИК РОЗРОБНИЦТВА
Allergan Pharmaceuticals Ірландія
Каслбар -роуд
Вестпорт
Округ Майо
Ірландія
Торговий представник в Італії
Allergan SpA, Via Salvatore Quasimodo n ° 134/138, Рим
08.0 НОМЕР РОЗВИТКУ З РОБОТИ
AIC n. 034883013 / М "100 одиниць порошок алергена для розчину для ін'єкцій" 1 флакон містить 100 одиниць алергену
09.0 ДАТА ПЕРШОГО ДОЗВІЛЕННЯ АБО ОНОВЛЕННЯ ДОЗВІЛЛЯ
Перша авторизація: 4 серпня 2000 року
Поновлення: 28 лютого 2009 року
10.0 ДАТА ПЕРЕГЛЯНУ ТЕКСТУ
Рішення АІФА від 23 січня 2013 року