Діючі речовини: Фамцикловір
Фамцикловір Сандоз, таблетки, вкриті оболонкою, 125 мг
Фамцикловір Сандоз таблетки, вкриті оболонкою, 250 мг
Фамцикловір Сандоз, таблетки, вкриті оболонкою, 500 мг
Чому використовується Фамцикловір - загальний препарат? Для чого це?
Фамцикловір Сандоз - противірусний препарат. Це запобігає розмноженню заражаючого вірусу. Оскільки вірус швидко розмножується, коли інфекція починається, ви отримаєте кращі результати лікування, якщо приймете Фамцикловір Сандоз, як тільки з’являться перші симптоми.
Фамцикловір Сандоз використовується для лікування двох видів вірусних інфекцій у дорослих:
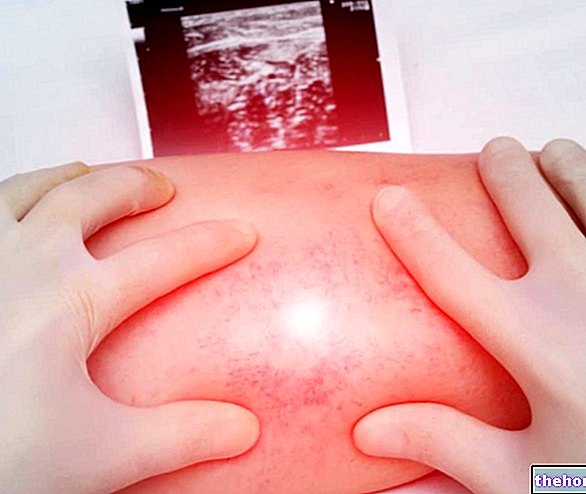
- Оперізуючий герпес - це «вірусна інфекція, спричинена вірусом вітряної віспи (той самий вірус, що викликає вітряну віспу). Фамцикловір Сандоз запобігає поширенню вірусу в організмі, тому загоєння може наступити швидше.
- Фамцикловір Сандоз також використовується для лікування інфекцій в області навколо ока або навіть у самому оці (офтальмологічний зостер).
- Генітальний герпес. Генітальний герпес - це вірусна інфекція, спричинена вірусом простого герпесу типу 1 або 2. Вона зазвичай передається статевим шляхом. Вона викликає утворення пухирів і печіння або свербіж статевих органів, що може бути болісним. Фамцикловір Сандоз використовується для лікування інфекцій з генітальним герпесом дорослі Люди, які мають часті епізоди генітального герпесу, також можуть приймати Фамцикловір Сандоз, щоб запобігти появі нових епізодів.
Протипоказання Коли Фамцикловір не слід застосовувати - препарат загального призначення
Не приймайте Фамцикловір Сандоз
- Якщо у вас алергія на фамцикловір, будь -який інший інгредієнт цього препарату (перелічений у розділі 6) або пенцикловір (активний метаболіт фамцикловіру та компонент деяких інших ліків).
Зверніться до лікаря за порадою, якщо ви думаєте, що у вас алергія.
Заходи безпеки при застосуванні Що потрібно знати перед прийомом Фамцикловіру - генеричного препарату
Попередження та запобіжні заходи Перед застосуванням Фамцикловіру Сандоз поговоріть зі своїм лікарем.
- Якщо у вас є проблеми з нирками (або вони були раніше). Ваш лікар може прийняти рішення про призначення меншої дози Фамцикловіру Сандозу.
- Якщо у вас є якісь порушення імунної системи.
- Якщо у вас проблеми з печінкою. Якщо що -небудь з перерахованого стосується вас, перед прийомом Фамцикловіру Сандоз поговоріть зі своїм лікарем.
Діти та підлітки (до 18 років)
Застосування Фамцикловіру Сандозу у дітей та підлітків не рекомендується.
Профілактика передачі генітального герпесу іншим особам
Якщо ви приймаєте Фамцикловір Сандоз для лікування або придушення генітального герпесу, або якщо ви раніше страждали від генітального герпесу, вам слід продовжувати безпечний секс із використанням презервативів. Це важливо для запобігання передачі інфекції іншим людям . Не варто займатися сексом, якщо у вас є пухирі на статевих органах.
Взаємодії Які препарати або продукти харчування можуть змінити дію Фамцикловіру - загального препарату
Повідомте свого лікаря або фармацевта, якщо ви приймаєте, нещодавно приймали або могли б приймати будь -які інші ліки, включаючи ліки, відпущені без рецепта.
Особливо важливо повідомити свого лікаря або фармацевта, якщо ви приймаєте будь -яке з наступних ліків:
- Ралоксифен (використовується для профілактики та лікування остеопорозу).
- Пробенецид (використовується для лікування високого рівня сечової кислоти в крові, пов’язаної з подагрою, та для підвищення рівня антибіотиків, подібних до пеніциліну в крові), або будь-які інші ліки, які можуть пошкодити нирки.
Фамцикловір Сандоз з їжею та напоями
Фамцикловір Сандоз можна приймати з їжею або без їжі.
Попередження Важливо знати, що:
Вагітність, грудне вигодовування та фертильність
Якщо ви вагітні або годуєте грудьми, думаєте, що можете бути вагітними або плануєте народження дитини, зверніться до лікаря за порадою, перш ніж приймати цей препарат.
Фамцикловір Сандоз не слід застосовувати під час вагітності, якщо це не є крайньою необхідністю. Ваш лікар обговорить з вами потенційні ризики прийому Фамцикловіру Сандозу під час вагітності. Ваш лікар обговорить з вами можливі ризики прийому Фамцикловіру Сандоз під час годування груддю.
Водіння автомобіля та роботу з машинами
Фамцикловір Сандоз може викликати запаморочення, сонливість або сплутаність свідомості. Не керуйте автомобілем та не працюйте з механізмами, якщо під час прийому Фамцикловіру Сандоз ви відчуваєте будь -які з цих симптомів.
Фамцикловір Сандоз 125 мг, вкриті плівковою оболонкою, містить лактозу
Якщо ваш лікар сказав вам, що у вас непереносимість деяких цукрів, таких як лактоза, зверніться до лікаря, перш ніж приймати цей препарат.
Фамцикловір Сандоз 250 мг, вкриті плівковою оболонкою, містить лактозу
Якщо ваш лікар сказав вам, що у вас непереносимість деяких цукрів, таких як лактоза, зверніться до лікаря, перш ніж приймати цей препарат.
Доза, спосіб та час введення Як застосовувати Фамцикловір - загальний препарат: дозування
Завжди приймайте цей препарат точно так, як вам сказав ваш лікар. Якщо є сумніви, зверніться до лікаря або фармацевта.
- Добова доза та тривалість лікування залежатимуть від типу вашої вірусної інфекції - див. Нижче. Ваш лікар призначить вам правильну дозу.
- Для досягнення найкращих результатів почніть прийом препарату якомога швидше після появи перших ознак та симптомів.
- Уникайте статевих контактів, якщо ви відчуваєте симптоми генітального герпесу - навіть якщо ви вже почали лікування Фамцикловіром Сандозом. Це тому, що він може передати інфекцію вашому партнерові.
- Якщо у вас є або були проблеми з нирками, ваш лікар може прийняти рішення про зниження дози Фамцикловіру Сандозу.
Доза при оперізувальному герпесі
Якщо у вас нормальна імунна система, рекомендована доза становить
- 500 мг тричі на день протягом семи днів
Якщо ваш імунний захист знижений, рекомендована доза становить
- 500 мг тричі на день протягом десяти днів
Доза для генітального герпесу
Доза залежить від стану вашої імунної системи та стадії інфекції.
Якщо у вас нормальна імунна система, дози такі:
Для першої висипки рекомендована доза становить:
- 250 мг тричі на день протягом п’яти днів.
Для лікування подальших висипань рекомендована доза становить:
- 125 мг двічі на день протягом п’яти днів.
Для профілактики майбутніх висипань рекомендована доза становить:
- 250 мг двічі на день.
Ваш лікар скаже вам, як довго продовжувати приймати таблетки.
Якщо ваш імунний захист низький, дози такі:
Для лікування триваючої висипки рекомендована доза становить:
- 500 мг двічі на день протягом семи днів.
Для профілактики майбутніх висипань доза становить:
500 мг двічі на день.
Ваш лікар скаже вам, як довго продовжувати приймати таблетки.
Якщо ви забули прийняти Фамцикловір Сандоз
Якщо ви забули прийняти дозу Фамцикловіру Сандозу, ви повинні прийняти її, як тільки пригадаєте.
Потім прийміть наступну дозу відповідно до плану. Однак не приймайте дві дози менше ніж за 1 годину: у цьому випадку слід пропустити пропущену дозу. Також не приймайте подвійну дозу, щоб компенсувати пропущену дозу.
Якщо у вас виникнуть додаткові запитання щодо застосування цього препарату, зверніться до лікаря або фармацевта.
Передозування Що робити, якщо ви передозували Фамцикловір - загальний препарат
Якщо ви прийняли більше таблеток, ніж вам сказали, або якщо хтось інший випадково прийняв ваше ліки, негайно зверніться до лікаря або до лікарні. Покажіть їм свою коробку з планшетами.
Прийом занадто великої кількості Фамцикловіру Сандозу може вплинути на нирки. У пацієнтів, які вже мають проблеми з нирками, якщо дози не зменшуються належним чином, це рідко може призвести до ниркової недостатності.
Побічні ефекти Які побічні ефекти Фамцикловіру - загального препарату
Як і всі ліки, цей препарат може викликати побічні ефекти, хоча вони виникають не у всіх.
Серйозними побічними ефектами Фамцикловіру Сандозу є:
Більшість з цих побічних ефектів рідкісні або нечасті (вражають від 1 до 100 з 10000 пацієнтів).
- Важкі висипання пухирів на шкірі або слизових оболонках губ, очей, рота, носових проходів або статевих органів (це можуть бути ознаками важкої шкірної алергічної реакції).
- Синці без пояснюваної причини, червонуваті або фіолетові плями на шкірі або кровотеча з носа (це можуть бути ознаками зменшення кількості тромбоцитів).
- Набряк під поверхнею шкіри (наприклад, набряк обличчя, набряк навколо ока, набряк повік, набряк горла).
- Жовте забарвлення шкіри та / або очей (ознаки жовтяниці).
- Пурпурні ділянки шкіри, свербіж, печіння (ознаки запалення кровоносних судин).
Зверніться до лікаря або зверніться до відділення невідкладної допомоги найближчої лікарні, якщо відчуєте будь -який із цих побічних ефектів.
Дуже поширені побічні ефекти (ці побічні ефекти виникають більш ніж у 1 з 10 осіб)
- Головний біль
Поширені побічні ефекти (ці побічні ефекти вражають до 1 з 10 осіб)
- Почуття нудоти (нудота)
- Він смикався
- Біль у животі
- Діарея
- Запаморочення
- Висип
- Сверблячий
- Аномальні значення у функціональних тестах печінки
Рідкісні побічні ефекти (ці побічні ефекти зачіпають до 1 із 100 осіб)
- Спантеличеність
- Сонливість (зазвичай у літніх людей)
- Сверблячий висип (кропив’янка)
Рідкісні побічні ефекти (ці побічні ефекти зачіпають до 1 з 1000 осіб)
- Галюцинації (побачити або почути те, чого насправді немає)
- Серцебиття (ознаки ненормального серцебиття)
- Якщо будь -який з побічних ефектів стає серйозним, або якщо Ви помітили будь -які побічні ефекти, не зазначені у цій інструкції, повідомте про це свого лікаря або фармацевта.
Повідомлення про побічні ефекти
Якщо у Вас виникли будь -які побічні ефекти, зверніться до лікаря або фармацевта, що включає будь -які можливі побічні ефекти, не зазначені у цій інструкції. Ви також можете повідомити про побічні ефекти безпосередньо через національну систему звітності на веб -сайті www.agenziafarmaco.it/it/responsabili.Повідомляючи про побічні ефекти, ви можете допомогти надати більше інформації про безпеку застосування цього препарату.
Термін придатності та утримання
- Зберігайте цей препарат подалі від очей та недоступного для дітей місця.
- Не використовуйте цей лікарський засіб після закінчення терміну придатності, зазначеного на етикетці після "Термін придатності". Термін придатності відноситься до останнього дня цього місяця.
- Не зберігати при температурі вище 25 ° C.
- Зберігати в оригінальній упаковці для захисту від вологи.
- Не використовуйте цей препарат, якщо ви помітили, що упаковка пошкоджена або має ознаки втручання.
- Не викидайте ліки через стічні води або побутові відходи. Попросіть свого фармацевта, як викинути ліки, які ви більше не використовуєте. Це допоможе захистити навколишнє середовище.
Інша інформація
Що містить Фамцикловір Сандоз
Фамцикловір Сандоз, таблетки, вкриті оболонкою, 125 мг
- Діюча речовина - фамцикловір.
- Інші інгредієнти: безводна лактоза, натрію крохмальгліколят (тип А), гідроксипропілцелюлоза та стеарат магнію. Покриття таблетки складається з: гіпромелози, діоксиду титану (Е 171), Макроголу 4000 та Макроголу 6000.
Фамцикловір Сандоз таблетки, вкриті оболонкою, 250 мг
- Діюча речовина - фамцикловір.
- Інші інгредієнти: безводна лактоза, натрію крохмальгліколят (тип А), гідроксипропілцелюлоза та стеарат магнію. Покриття таблетки складається з гіпромелози, діоксиду титану (E171), макроголу 4000 та макроголу 6000.
Фамцикловір Сандоз, таблетки, вкриті оболонкою, 500 мг
- Діюча речовина - фамцикловір.
- Інші інгредієнти: натрію крохмальгліколят (тип А), гідроксипропілцелюлоза та стеарат магнію. Покриття таблетки складається з гіпромелози, діоксиду титану (E171), макроголу 4000 та макроголу 6000.
Як виглядає Фамцикловір Сандоз та вміст упаковки
Фамцикловір Сандоз випускається у формі таблеток, вкритих оболонкою.
Фамцикловір Сандоз 125 мг, вкриті плівковою оболонкою:
Біла кругла двоопукла таблетка, вкрита плівковою оболонкою, зі скошеними краями, з тисненням "FV" з одного боку та "125" з іншого.
Фамцикловір Сандоз 250 мг, вкриті плівковою оболонкою:
Біла кругла двоопукла таблетка, вкрита плівковою оболонкою, зі скошеними краями, з тисненням "FV" з одного боку та "250" з іншого.
Фамцикловір Сандоз, таблетки, вкриті оболонкою, 500 мг:
Біла, овальна, двоопукла таблетка, вкрита плівковою оболонкою, зі скошеними краями, з гравіюванням "FV 500" тільки з одного боку.
Джерело з інформацією про упаковку: AIFA (Італійське агентство з лікарських засобів). Вміст, опублікований у січні 2016 р. Наявна інформація може бути не актуальною.
Щоб мати доступ до найновішої версії, бажано зайти на веб-сайт AIFA (Італійське агентство з лікарських засобів). Відмова від відповідальності та корисна інформація.
01.0 НАЗВА ЛЕКАРСТВЕННОГО ПРОДУКТУ
ТАБЛЕТКИ FAMCICLOVIR SANDOZ, ПОКРИТІ ПЛЕНКОЮ
02.0 ЯКІСНИЙ І КІЛЬКІСНИЙ СКЛАД
Кожна таблетка, вкрита плівковою оболонкою, містить 125 мг, 250 мг або 500 мг фамцикловіру.
Повний список допоміжних речовин див. У розділі 6.1.
03.0 ФАРМАЦЕВТИЧНА ФОРМА
Планшет, вкритий плівковою оболонкою.
04.0 КЛІНІЧНА ІНФОРМАЦІЯ
04.1 Терапевтичні показання
Інфекції вірусу вітряної віспи (VZV) - оперізуючий герпес
Фамцикловір Сандоз показаний для:
- лікування оперізувального герпесу та офтальмологічного зостору у дорослих з імунокомпетентністю (див. розділ 4.4)
- лікування оперізувального герпесу у дорослих з ослабленим імунітетом (див. розділ 4.4)
Інфекції вірусу простого герпесу (ВПГ) - генітальний герпес
Фамцикловір Сандоз показаний для:
- лікування перших і рецидивуючих епізодів генітального герпесу у дорослих з імунокомпетентністю
- лікування рецидивуючих епізодів генітального герпесу у дорослих з ослабленим імунітетом
- придушення рецидивуючого генітального герпесу у дорослих з імунокомпетентністю та імунодефіцитом
Клінічних досліджень з імунодефіцитними пацієнтами з ВПГ з інших причин, крім ВІЛ -інфекції, не проводилося (див. Розділ 5.1).
04.2 Дозування та спосіб введення
Оперізуючий герпес у імунокомпетентних дорослих
500 мг тричі на день протягом семи днів для гострого лікування офтальмологічного зостеру.
Лікування слід починати якомога швидше після діагностики оперізувального герпесу.
Оперізуючий герпес у дорослих з ослабленим імунітетом
500 мг тричі на день протягом десяти днів.
Лікування слід починати якомога швидше після діагностики оперізувального лишаю.
Генітальний герпес у імунокомпетентних дорослих
Перший епізод генітального герпесу: 250 мг тричі на день протягом п’яти днів. Рекомендується починати лікування якомога швидше після діагностики першого епізоду генітального герпесу.
Епізодичне лікування рецидивуючого генітального герпесу: 125 мг двічі на день протягом п’яти днів. Рекомендується починати лікування якомога швидше після появи продромальних симптомів (наприклад, поколювання, свербіння, печіння, болю) або ушкоджень.
Рецидивуючий генітальний герпес у дорослих з ослабленим імунітетом
Епізодичне лікування рецидивуючого генітального герпесу: 500 мг двічі на день протягом семи днів. Рекомендується починати лікування якомога швидше після появи продромальних симптомів (наприклад, поколювання, свербіння, печіння, болю) або ушкоджень.
Пригнічення рецидивуючого генітального герпесу у імунокомпетентних дорослих
250 мг двічі на день. Супресивну терапію слід припинити максимум через 12 місяців безперервного противірусного лікування, щоб повторно оцінити частоту та тяжкість рецидивів. Мінімальний період переоцінки повинен включати два періоди. Пацієнти, які продовжують мати важкі захворювання, можуть знову почати супресивне лікування.
Придушення рецидивуючого генітального герпесу у дорослих з ослабленим імунітетом
500 мг двічі на день.
Пацієнти з порушенням функції нирок
Оскільки знижений кліренс пенцикловіру пов'язаний із зниженням функції нирок, що вимірюється кліренсом креатиніну, особливу увагу слід приділити дозуванню у пацієнтів з порушенням функції нирок. Рекомендовані дози для дорослих пацієнтів з нирковою недостатністю наведені в таблиці 1.
Таблиця 1 Рекомендовані дози для дорослих пацієнтів з порушенням функції нирок
Пацієнти з нирковою недостатністю на гемодіалізі
Оскільки 4-годинний гемодіаліз призвів до 75% зниження концентрації пенцикловіру в плазмі, фамцикловір слід вводити одразу після діалізу.
Пацієнти з порушенням функції печінки
Пацієнтам з печінковою недостатністю легкого та помірного ступеня коригування дози не потрібне. Дані щодо пацієнтів з тяжкою печінковою недостатністю відсутні (див. Розділи 4.4 та 5.2).
Пацієнти літнього віку (≥ 65 років)
Коригування дози не потрібне, за винятком випадків порушення функції нирок.
Педіатричне населення
Безпека та ефективність застосування фамцикловіру у дітей та підлітків віком до 18 років не встановлені. Наразі наявні дані описані у розділах 5.1 та 5.2.
Спосіб введення
Фамцикловір Сандоз можна приймати з їжею або без неї (див. Розділ 5.2).
04.3 Протипоказання
Підвищена чутливість до активної речовини або до будь -якої з допоміжних речовин.
Підвищена чутливість до пенцикловіру.
04.4 Спеціальні попередження та відповідні запобіжні заходи щодо використання
Застосування у пацієнтів з нирковою недостатністю
Пацієнтам з порушеннями функції нирок слід коригувати дозу (див. Розділи 4.2 та 4.9).
Застосування у пацієнтів з печінковою недостатністю
Фамцикловір не вивчався у пацієнтів з тяжкою печінковою недостатністю. У цих пацієнтів може бути порушена трансформація фамцикловіру до його активного метаболіту пенцикловіру, що призведе до зниження концентрації пенцикловіру в плазмі; Тому може спостерігатися зниження ефективності фамцикловіру.
Використовується для лікування оперізувального герпесу
Клінічну відповідь слід ретельно контролювати, особливо у пацієнтів з ослабленим імунітетом. Якщо відповідь на пероральну терапію вважається недостатньою, слід розглянути можливість внутрішньовенної противірусної терапії.
Пацієнтів із ускладненим оперізувальним герпесом, тобто з ураженням внутрішніх органів, розповсюдженим зостором, моторними нейропатіями, енцефалітом та цереброваскулярними ускладненнями, слід лікувати внутрішньовенною противірусною терапією.
Крім того, пацієнтів з ослабленим імунітетом з офтальмологічним зостром або хворих з високим ризиком поширення захворювання та ураження вісцеральних органів слід лікувати внутрішньовенною противірусною терапією.
Передача генітального герпесу
Пацієнтам слід порадити уникати статевих контактів за наявності симптомів, навіть якщо розпочато лікування противірусним засобом. Під час супресивної терапії противірусними засобами частота випадання вірусу значно зменшується. Однак передача все ж можлива. Тому пацієнтам рекомендується вживати безпечніших заходів під час статевого акту, на додаток до терапії фамцикловіром.
Інший
Фамцикловір Сандоз у таблетках 125 мг та 250 мг містить лактозу. Пацієнти з рідкісними спадковими формами непереносимості галактози, дефіцитом лактази Лаппа або синдромом мальабсорбції глюкози-галактози не повинні приймати цей препарат..
04.5 Взаємодія з іншими лікарськими засобами та інші форми взаємодії
Вплив інших лікарських засобів на фамцикловір
Клінічно значущих взаємодій не виявлено.
Одночасне застосування пробенециду може призвести до збільшення концентрації пенцикловіру, активного метаболіту фамцикловіру, у плазмі крові через конкуренцію у виведенні.
Тому пацієнтів, які отримують фамцикловір у дозі 500 мг тричі на день, які приймають одночасно з пробенецидом, слід контролювати на предмет токсичності. Якщо у пацієнтів виникає сильне запаморочення, сонливість, сплутаність свідомості або інші порушення центральної нервової системи, можна розглянути можливість зменшення дози фамцикловіру до 250 мг тричі на день.
Фамцикловір вимагає перетворення ферменту альдегідоксидази в його активний метаболіт пенцикловір.Ралоксифен виявився потужним інгібітором цього ферменту. в пробірці. Одночасне застосування ралоксифену може вплинути на утворення пенцикловіру, а отже, і на ефективність фамцикловіру.При одночасному застосуванні ралоксифену з фамцикловіром слід контролювати клінічну ефективність противірусної терапії.
04.6 Вагітність та період лактації
Вагітність
Дані щодо застосування фамцикловіру вагітним жінкам обмежені (менше 300 епізодів вагітності).На основі цих обмежених даних кумулятивний аналіз потенційної та ретроспективної вагітності не надав доказів того, що лікарський засіб викликає специфічні зміни плоду або вроджені аномалії. фамцикловір) Фамцикловір слід застосовувати під час вагітності, лише якщо потенційна користь перевищує потенційний ризик.
Час годування
Невідомо, чи виділяється фамцикловір у жіноче молоко. Дослідження на тваринах показали екскрецію пенцикловіру в грудне молоко.Якщо стан жінки потребує лікування фамцикловіром, можна розглянути можливість переривання грудного вигодовування.
Родючість
Клінічні дані не показують впливу фамцикловіру на фертильність чоловіків після тривалого лікування при пероральній дозі 250 мг двічі на день (див. Розділ 5.3).
04.7 Вплив на здатність керувати автомобілем та працювати з механізмами
Не проводилося досліджень щодо впливу на здатність керувати автомобілем та працювати з механізмами. Однак пацієнтам, які приймають Фамцикловір Сандоз, у яких спостерігається запаморочення, сонливість, сплутаність свідомості чи інші порушення центральної нервової системи, слід утримуватися від керування транспортними засобами та від використання механізмів.
04.8 Побічні ефекти
У клінічних дослідженнях повідомлялося про головний біль та нудоту. Ці ефекти, як правило, були легкими або помірними за інтенсивністю, а також спостерігалися з подібною частотою у пацієнтів, які приймали плацебо. Усі інші побічні реакції спостерігалися з боку маркетингу.
Загальний пул плацебо-або активних контрольованих клінічних досліджень (n = 2326 у групі Фамвір) був ретроспективно проаналізований, щоб отримати класифікацію частоти спостереження побічних реакцій, наведених нижче. У таблиці нижче оцінювана частота Побічні реакції ґрунтуються на всіх спонтанних повідомленнях та випадках, описаних у літературі, про які повідомлялося про Фамвір з моменту його створення.
Побічні реакції (Таблиця 2) перераховані за частотою, використовуючи таку умову: дуже часто (≥ 1/10); поширені (≥ 1/100,
Таблиця 2 Побічні реакції
Загалом, побічні реакції, що спостерігалися в клінічних дослідженнях у пацієнтів з ослабленим імунітетом, були порівнянні з тими, що були зареєстровані в імунокомпетентній популяції. Частіше повідомлялося про нудоту, блювоту та порушення функції печінки, особливо у високих дозах.
04.9 Передозування
Випадки передозування фамцикловіру обмежені. У разі передозування слід розпочати відповідну симптоматичну та підтримуючу терапію. Про гостру ниркову недостатність рідко повідомлялося у пацієнтів із латентною нирковою недостатністю, у яких доза фамцикловіру не була адекватно знижена у порівнянні з рівнем функції нирок. Пенцикловір піддається діалізу; плазмові концентрації знижуються приблизно на 75% після 4 годин гемодіалізу.
05.0 ФАРМАКОЛОГІЧНІ ВЛАСТИВОСТІ
05.1 Фармакодинамічні властивості
Фармакотерапевтична група: нуклеозиди та нуклеотиди, за винятком інгібіторів зворотної транскриптази.
Код ATC: JO5A B09.
Механізм дії
Фамцикловір є пероральним проліком пенцикловіру. Фамцикловір швидко перетворюється в природних умовах до пенцикловіру, який має активність в пробірці проти вірусів простого герпесу (ВПГ 1 та 2 типу), вірусу вітряної віспи, вірусу Епштейна-Барр та цитомегаловірусу.
Противірусний ефект перорального введення фамцикловіру був продемонстрований на кількох моделях тварин: цей ефект обумовлений перетворенням в природних умовах до пенцикловіру. У інфікованих вірусом клітинах вірусна тимідинкіназа (ТК) фосфорилює пенцикловір в монофосфатну форму, яка, у свою чергу, клітинними кіназами перетворюється на пенцикловір трифосфат. Цей трифосфат залишається в інфікованих клітинах більше 12 годин і інгібує подовження ланцюга вірусної ДНК шляхом конкурентного пригнічення дезоксигуанозинтрифосфатом для включення у зростаючу вірусну ДНК, тим самим блокуючи реплікацію вірусної ДНК. У клітинах, не інфікованих вірусом, концентрація пенцикловіру трифосфату знаходиться на межі порогу визначення. Тому ймовірність токсичності для клітин -господарів ссавців низька, а терапевтичні концентрації пенцикловіру навряд чи призведуть до фармакологічного впливу на неінфіковані клітини.
Стійкість
Як і у випадку з ацикловіром, найбільш поширеною формою резистентності, що спостерігається у штамів вірусу простого герпесу (ВПГ), є дефіцит вироблення ферменту тимідинкінази (ТК) до пенцикловіру.
Результати 11 міжнародних клінічних досліджень, проведених у пацієнтів з імунокомпетентністю або з ослабленим імунітетом, які отримували пенцикловір (препарати для місцевого застосування та внутрішньовенні введення) або фамцикловір, включаючи ті дослідження, в яких пацієнти лікувалися фамцикловіром протягом 12 місяців, показали загальну низьку частоту вірусних ізолятів, стійких до пенцикловір: 0,2% (2/913) у імунокомпетентних пацієнтів та 2,1% (6/288) у пацієнтів з ослабленим імунітетом. Резистентні ізоляти були виявлені переважно на початку терапії або у групі плацебо, а резистентність виникала під час або після лікування фамцикловіром або пенцикловіром лише у двох пацієнтів з імунодефіцитом.
Клінічна ефективність
У плацебо-та активно контрольованих дослідженнях як у імунокомпетентних, так і у пацієнтів з ослабленим імунітетом із неускладненим оперізувальним герпесом фамцикловір був ефективним у загоєнні ран. У активному контрольованому клінічному дослідженні фамцикловір виявився ефективним у лікуванні офтальмологічного зостеру у імунокомпетентних пацієнтів.
Ефективність фамцикловіру у імунокомпетентних пацієнтів з першим епізодом генітального герпесу була продемонстрована у трьох дослідженнях з активним контролем. Два плацебо-контрольованих дослідження у пацієнтів з імунокомпетентністю та одне дослідження з активним контролем у ВІЛ-інфікованих пацієнтів з рецидивуючим генітальним герпесом показали, що фамцикловір є ефективним.
Дві 12-місячні плацебо-контрольовані дослідження, проведені у пацієнтів з імунокомпетентністю з рецидивуючим генітальним герпесом, показали, що пацієнти, які отримували фамцикловір, мали значне зменшення рецидивів порівняно з пацієнтами, які отримували плацебо. Плацебо-контрольовані та неконтрольовані дослідження тривалістю до 16 тижнів показали, що фамцикловір ефективний у пригніченні рецидивуючого генітального герпесу у ВІЛ-інфікованих пацієнтів; плацебо-контрольоване дослідження показало, що фамцикловір значно зменшує частку днів симптоматичного та безсимптомного поширення вірусу простого герпесу.
Педіатричне населення
Досліджений склад гранул фамцикловіру для перорального застосування вивчався у 169 педіатричних пацієнтів віком від 1 місяця до 12 років. Сто таких пацієнтів у віці від 1 до 12 років отримували пероральні гранули фамцикловіру (у дозах від 150 до 500 мг) двічі на день (47 пацієнтів з інфекцією простого герпесу) або тричі на день (53 пацієнти з вітрянкою) протягом 7 днів . Решта 69 пацієнтів (18 пацієнтів віком від 1 до 12 місяців, 51 пацієнт віком від 1 до 12 років) брали участь у фармакокінетиці та безпеки застосування разових доз фамцикловіру для пероральних гранул (у дозах від 25 до 500 мг). Дози фамцикловіру, виходячи з маси тіла, були обрані для отримання подібної «системної експозиції пенцикловіру» до системної експозиції пенцикловіру, яка спостерігалася у дорослих після введення 500 мг фамцикловіру. Жодне з цих досліджень не включало контрольну групу; тому не можна зробити висновок щодо ефективності досліджуваних режимів дозування. Профіль безпеки був подібним до такого, що спостерігався у дорослих. Однак системна експозиція препарату була низькою у дітей віком до 6 місяців, що запобігало будь -якій оцінці безпеки фамцикловір у цій популяції.
05.2 Фармакокінетичні властивості
Загальні ознаки
Поглинання
Фамцикловір є пероральним проліком пенцикловіру, активного метаболіту проти вірусів. Після перорального застосування фамцикловір швидко і широко всмоктується і перетворюється на пенцикловір. Біодоступність пенцикловіру після перорального застосування фамцикловіру становила 77%. Пікова концентрація пенцикловіру в плазмі після пероральних доз 125 мг, 250 мг, 500 мг та 750 мг фамцикловіру становила 0,8 мкг / мл, 1,6 мкг / мл, 3,3 мкг / мл відповідно та 5,1 мкг / мл, і було отримано в середньому 45 хвилин після введення.
Криві концентрації пенцикловіру у плазмі у порівнянні з часом є подібними як при одноразовому, так і при повторному введенні (тричі та двічі на день), що вказує на відсутність накопичення пенцикловіру після повторного введення фамцикловіру.
На системну доступність (AUC) перорально введеного фамцикловіру пенцикловіру не впливає їжа.
Розповсюдження
Пенцикловір та його попередник 6-дезокси погано зв’язуються з білками плазми (менше 20%).
Метаболізм та виведення
Фамцикловір виводиться переважно у вигляді пенцикловіру та у вигляді попередника 6-дезокси, обидва з яких виводяться із сечею. Концентрації незміненого фамцикловіру в сечі відсутні. Канальцева секреція сприяє нирковій елімінації пенцикловіру.
Кінцевий період напіввиведення пенцикловіру з плазми після одноразового та багаторазового введення фамцикловіру становив приблизно 2 години.
Результати доклінічних досліджень не продемонстрували потенціалу індукції ферментів цитохрому Р450 та інгібування CYP3A4.
Характеристика особливих груп населення
Пацієнти з оперізуваним герпесом
Неускладнена інфекція оперізувального герпесу істотно не змінює фармакокінетику пенцикловіру після перорального застосування фамцикловіру.Після одноразового та багаторазового введення фамцикловіру пацієнтам із оперізувальним герпесом кінцевий період напіввиведення пенцикловіру у плазмі крові становив 2 відповідно. 8 та 2,7 години.
Пацієнти з нирковою недостатністю
Після одноразового і повторного застосування очевидний плазмовий кліренс, нирковий кліренс та постійна швидкість виведення пенцикловіру з плазми зменшувалися пропорційно зменшенню ниркової функції. Пацієнтам з нирковою недостатністю необхідно коригувати дозу (див. Розділ 4.2).
Пацієнти з печінковою недостатністю
Помірне та помірне порушення функції печінки не продемонструвало впливу на системну доступність пенцикловіру після перорального застосування фамцикловіру. Для пацієнтів з печінковою недостатністю легкого та помірного ступеня коригування дози не потрібне (див. Розділи 4.2 та 4.4). Фармакокінетика пенцикловіру не вивчалася у пацієнтів з тяжкою печінковою недостатністю. У цих пацієнтів може бути порушена конверсія фамцикловіру в активний метаболіт пенцикловір, що призведе до зниження концентрації пенцикловіру в плазмі крові, а отже, до можливого зниження ефективності фамцикловіру.
Літні люди (≥ 65 років)
Згідно порівняльних досліджень, після перорального застосування фамцикловіру середнє значення AUC було приблизно на 30% вище, а нирковий кліренс пенцикловіру приблизно на 20% нижчий у добровольців літнього віку (65-79 років) порівняно з молодшими добровольцями. Частково ці відмінності можуть бути обумовлені відмінностями у функції нирок у двох групах. Не потрібно коригувати дозу залежно від віку, доки функція нирок не порушена (див. Розділ 4.2).
Секс
Повідомлялося про невеликі відмінності в нирковому кліренсі пенцикловіру між жінками та чоловіками, що пояснюється статевими відмінностями у функції нирок. Не потрібно коригувати дозування залежно від статі.
Педіатричні пацієнти
Повторні пероральні дози фамцикловіру (250 або 500 мг тричі на день), введені педіатричним пацієнтам (6-11 років) з інфекцією гепатиту В, не мали значного впливу на фармакокінетику пенцикловіру порівняно з одноразовим введенням. Не було накопичення пенцикловіру.
У дітей (1-12 років) з інфекцією простого герпесу або з вітряною віспою, які отримували разові дози фамцикловіру (див. Розділ 5.1), очевидний кліренс пенцикловіру збільшувався із збільшенням маси тіла нелінійно. L "Період напіввиведення з плазми Пенцикловір мав тенденцію зменшуватися зі зменшенням віку, із середнього значення 1,6 години у пацієнтів у віці від 6 до 12 років, до середнього значення у 1,2 години у пацієнтів у віці від 6 до 12 років.
05.3 Дані доклінічної безпеки
Загальна токсичність
Дослідження фармакологічної безпеки та токсичності при повторних дозах не виявляють особливих ризиків для людини.
Генотоксичність
Фамцикловір не був генотоксичним у комплексній серії тестів in vitro та in vivo, здатних виявити генну мутацію, хромосомні пошкодження та пошкодження ДНК, які можна відновити. Як і інші речовини того ж класу, пенцикловір викликав хромосомні пошкодження, але не викликав ні мутації гена в клітинних системах бактерій або ссавців, ні збільшення репарації ДНК. в пробірці.
Канцерогенез
Повідомлялося про підвищену захворюваність на аденокарциному молочної залози, пухлину, яка зазвичай спостерігається у цього виду щурів, що використовуються у дослідженнях канцерогенності, у високих дозах у самок щурів.
Репродуктивна токсичність
Порушення фертильності (включаючи патофізіологічні зміни яєчок, зміну морфології сперматозоїдів, зниження концентрації та рухливості сперматозоїдів та зниження фертильності) було виявлено у самців щурів, яким давали 500 мг / кг / добу. Крім того, у дослідженнях загальної токсичності спостерігалися дегенеративні зміни епітелію яєчок. Цей ефект був оборотним і також спостерігався з іншими речовинами цього класу.
06.0 ФАРМАЦЕВТИЧНА ІНФОРМАЦІЯ
06.1 Допоміжні речовини
Фамцикловір Сандоз 125 та 250 мг, вкриті плівковою оболонкою:
гідроксипропілцелюлоза, безводна лактоза, натрію карбоксиметилкрохмаль, магнію стеарат, гіпромелоза, діоксид титану (Е 171), макрогол 4000, макрогол 6000.
Фамцикловір Сандоз, таблетки, вкриті оболонкою, 500 мг:
гідроксипропілцелюлоза, натрію карбоксиметилкрохмаль, магнію стеарат, гіпромелоза, діоксид титану (Е 171), макрогол 4000, макрогол 6000.
06.2 Несумісність
Не актуально.
06.3 Строк дії
3 роки.
06.4 Особливі умови зберігання
Зберігати при температурі не вище 25 ° C.Зберігати в оригінальній упаковці для захисту від вологи.
06.5 Характер безпосередньої упаковки та вміст упаковки
Фамцикловір Сандоз, таблетки, вкриті оболонкою, 125 мг
Блистерні упаковки по 10 таблеток по 125 мг
Фамцикловір Сандоз таблетки, вкриті оболонкою, 250 мг
Пухирі по 15 і 21 таблетки по 250 мг
Фамцикловір Сандоз, таблетки, вкриті оболонкою, 500 мг
Пухирі з 14 і 21 таблетками по 500 мг
Не всі розміри упаковок можна продавати.
06.6 Інструкції з використання та поводження
Невикористані ліки та відходи, отримані з цього препарату, слід утилізувати відповідно до місцевих правил.
07.0 ВЛАСНИК РОЗРОБНИЦТВА
Sandoz S.p.A.
Ларго Умберто Боччоні, 1
21040 Оріджіо В.А
08.0 НОМЕР РОЗВИТКУ З РОБОТИ
Фамцикловір Сандоз, таблетки, вкриті оболонкою, 125 мг
10 таблеток A.I.C. n. 029173046
Фамцикловір Сандоз таблетки, вкриті оболонкою, 250 мг
15 таблеток A.I.C. n. 029173034
21 таблетка A.I.C. n. 029173010
Фамцикловір Сандоз, таблетки, вкриті оболонкою, 500 мг
14 таблеток A.I.C. n. 029173061
21 таблетка A.I.C. n. 029173059
09.0 ДАТА ПЕРШОГО ДОЗВІЛЕННЯ АБО ОНОВЛЕННЯ ДОЗВІЛЛЯ
Фамцикловір Сандоз 250 мг, вкриті плівковою оболонкою - 21 таблетка:
Перша авторизація: 01.06.1995
Поновлення: 22.06.2010
Фамцикловір Сандоз 125 мг, вкриті плівковою оболонкою - 10 таблеток
Фамцикловір Сандоз 250 мг, вкриті плівковою оболонкою - 15 таблеток
Фамцикловір Сандоз 500 мг, вкриті плівковою оболонкою - 14 таблеток
Фамцикловір Сандоз 500 мг, вкриті плівковою оболонкою - 21 таблетка
Перша авторизація: 07.05.2002
Поновлення: 22.06.2010
10.0 ДАТА ПЕРЕГЛЯНУ ТЕКСТУ
Січня 2014 року














.jpg)