Діючі речовини: стронцій (стронцій ранелат)
OSSEOR 2 г гранули для пероральної суспензії
Показання Для чого використовується Osseor? Для чого це?
OSSEOR - це ліки, що застосовується для лікування важкого остеопорозу:
- у жінок у постменопаузі,
- у дорослих чоловіків,
з високим ризиком переломів, для яких неможливо вдатися до альтернативних методів лікування. У жінок у постменопаузі ранелат стронцію знижує ризик переломів хребта та стегна.
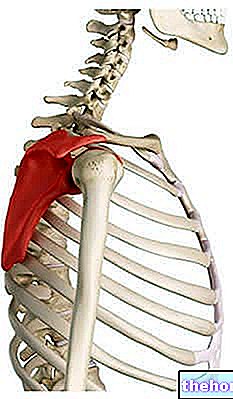
Остеопороз
Тіло безперервно руйнує стару кістку і формує нову кістку. У разі остеопорозу тіло руйнує більше кісток, ніж утворюється, так що поступово відбувається втрата кісткової тканини, а кістки стають більш тонкими і крихкими. Це відбувається особливо у жінок після менопаузи.
У багатьох людей з остеопорозом немає симптомів, і можливо навіть не знати, що у вас остеопороз. Однак остеопороз схильний до переломів (переломів кісток), особливо в хребті, стегнах і зап'ястях.
Як працює OSSEOR
OSSEOR, що містить діючу речовину стронцію ранелат, належить до групи ліків, що використовуються для лікування захворювань кісток.
OSSEOR зменшує руйнування кісток і стимулює реконструкцію кісток, тим самим зменшуючи ризик переломів. Сформована нова кістка нормальної якості.
Протипоказання Коли Осеор не слід застосовувати
Не приймайте OSSEOR
- якщо у вас алергія на стронцій ранелат або будь -який інший інгредієнт OSSEOR (перерахований у розділі 6).
- якщо у вас або колись був тромбоз (наприклад, ураження кровоносних судин ноги або легенів).
- якщо ви іммобілізовані назавжди або протягом певного періоду, наприклад, якщо ви перебуваєте в інвалідному візку, або якщо ви прикуті до ліжка, або вам потрібно пройти операцію, або якщо ви перебуваєте після операції. Ризик венозного тромбозу (тромбозу гомілки або легені) може бути більшим при тривалій іммобілізації.
- якщо вам відома ішемічна хвороба серця або цереброваскулярна хвороба, напр. якщо у вас був діагностований інфаркт, інсульт або транзиторна ішемічна атака (тимчасове зменшення припливу крові до мозку; також відомий як «міні-інсульт»), стенокардія або закупорка судин серця або мозку .
- якщо у вас є або були проблеми з кровообігом (захворювання периферичних артерій) або якщо вам зробили операцію на артеріях ніг.
- якщо у вас високий кров'яний тиск, який не контролюється лікуванням.
Заходи безпеки при застосуванні Що потрібно знати, перш ніж приймати Оссер
Поговоріть зі своїм лікарем або фармацевтом, перш ніж приймати OSSEOR:
- якщо у вас є ризик серцевих захворювань; це включає високий кров'яний тиск, високий рівень холестерину, діабет, куріння - якщо у вас є ризик тромбозу
- якщо у вас важке захворювання нирок.
Ваш лікар буде оцінювати стан вашого серця та судин через регулярні проміжки часу, зазвичай кожні 6-12 місяців, протягом усього періоду лікування OSSEOR.
Під час лікування, якщо виникає алергічна реакція (наприклад, набряк обличчя, язика або горла, утруднене дихання або ковтання, шкірний висип), вам слід негайно припинити прийом OSSEOR та звернутися до лікаря (див. Розділ 4).
При застосуванні OSSEOR повідомлялося про потенційно небезпечні для життя шкірні висипання (синдром Стівенса-Джонсона (SJS), токсичний епідермальний некроліз та тяжкі реакції гіперчутливості (DRESS)).
Найбільший ризик виникнення важких шкірних реакцій спостерігається протягом перших кількох тижнів лікування синдрому Стівенса-Джонсона та токсичного епідермального некролізу та, як правило, приблизно 3-6 тижнів для DRESS.
Якщо у вас виникли висип або серйозні шкірні симптоми (див. Розділ 4), припиніть прийом OSSEOR, негайно зверніться до лікаря та повідомте, що ви приймаєте цей препарат.
Якщо під час використання OSSEOR ви відчували синдром Стівенса-Джонсона, токсичний епідермальний некроліз або DRESS, вам ніколи не слід знову розпочинати лікування OSSEOR.
Якщо ви азіатського походження, перед прийомом OSSEOR поговоріть зі своїм лікарем, оскільки у вас може бути більший ризик шкірних реакцій.
Діти та підлітки
OSSEOR не призначений для застосування у дітей та підлітків (віком до 18 років).
Взаємодії Які ліки або продукти харчування можуть змінити дію Оссеору
Інші ліки та OSSEOR
Повідомте свого лікаря або фармацевта, якщо ви приймаєте, нещодавно приймали або могли б приймати будь -які інші ліки.
Припиніть прийом OSSEOR, якщо вам доведеться приймати пероральні тетрацикліни, такі як доксициклін або хінолони, такі як ципрофлоксацин (два типи антибіотиків). Ви можете перезапустити OSSEOR, коли закінчите приймати ці антибіотики. Якщо ви не впевнені, запитайте свого лікаря або фармацевта. Якщо якщо ви приймаєте ліки, що містять кальцій, перед прийомом OSSEOR витримайте принаймні 2 години. Якщо це неможливо, допустимий одночасний прийом двох ліків.
Якщо необхідно перевірити рівень кальцію в крові або сечі, ви повинні повідомити лабораторію, що ви приймаєте OSSEOR, оскільки це може вплинути на деякі методи дослідження.
OSSEOR з їжею та напоями
Їжа, молоко та його похідні зменшують всмоктування ранелату стронцію.Рекомендується приймати OSSEOR в проміжку між прийомами їжі, бажано перед сном, принаймні через дві години після прийому їжі, молока та похідних молока. Або добавок кальцію.
Попередження Важливо знати, що:
Вагітність та годування груддю
Не приймайте OSSEOR під час вагітності або годування груддю. У разі випадкового прийому під час вагітності або годування груддю негайно припиніть прийом препарату та повідомте про це лікаря.
Водіння автомобіля та роботу з машинами
Навряд чи OSSEOR вплине на здатність керувати автомобілем або працювати з механізмами.
OSSEOR містить аспартам (E951):
Якщо у вас є фенілкетонурія (рідкісне спадкове порушення обміну речовин), перед початком прийому цього препарату проконсультуйтеся з лікарем.
Доза, спосіб та час введення Як застосовувати Оссер: Дозування
Лікування повинен розпочинати тільки лікар, який має досвід лікування остеопорозу.
Завжди приймайте цей препарат точно так, як вам сказав ваш лікар або фармацевт. Якщо є сумніви, зверніться до лікаря або фармацевта.
OSSEOR призначений для перорального застосування. Рекомендована доза - один пакетик по 2 г на день.
Рекомендується приймати OSSEOR перед сном, бажано принаймні через 2 години після вечері. Ви також можете лягати спати відразу після прийому OSSEOR.
Візьміть гранули, що містяться в пакетиках, після того, як ви помістите їх у суспензію у склянку, що містить щонайменше 30 мл води (приблизно одну третину стандартної склянки) (див. Інструкції нижче). OSSEOR може взаємодіяти з молоком та його похідними; тому він Важливо, щоб OSSEOR змішували лише з водою, щоб переконатися, що ліки діє належним чином.
- Перелийте гранули з пакетика в склянку;
- Додати води;
- Перемішуйте до повного розсіювання грануляту у воді.
Випийте негайно. Не дозволяйте пройти більше 24 годин, перш ніж випити суспензію. Якщо з якихось причин ви не можете прийняти ліки відразу, не забудьте перемішати його ще раз перед вживанням.
Ваш лікар може порадити Вам приймати добавки кальцію та вітаміну D на додаток до OSSEOR. Не приймайте добавки кальцію перед сном, одночасно з OSSEOR.
Ваш лікар скаже вам, як довго продовжувати приймати OSSEOR. Лікування остеопорозу зазвичай триває тривалий час. Важливо продовжувати прийом OSSEOR стільки, скільки призначить лікар.
Передозування Що робити, якщо ви прийняли занадто багато Osseor
Якщо ви приймаєте більше OSSEOR, ніж слід
Якщо ви приймаєте більше пакетиків OSSEOR, ніж призначив ваш лікар, повідомте про це свого лікаря або фармацевта. Вони можуть порадити вам пити молоко або приймати антациди, щоб зменшити всмоктування активного інгредієнта.
Якщо ви забули прийняти OSSEOR
Не приймайте подвійну дозу, щоб компенсувати пропущену дозу. Просто прийміть наступну дозу в призначений час.
Якщо ви припините прийом OSSEOR
Важливо продовжувати прийом OSSEOR протягом того часу, який призначив ваш лікар. OSSEOR може лікувати важкий остеопороз, якщо його приймати постійно.
Побічні ефекти Які побічні ефекти Осеора
Як і всі ліки, цей препарат може викликати побічні ефекти, хоча вони виникають не у всіх.
Припиніть прийом OSSEOR і негайно повідомте свого лікаря, якщо виникне будь -який з наступних побічних ефектів:
Поширені (можуть виникнути до 1 з 10 пацієнтів):
- Інфаркт: раптові стискаючі болі в грудях, які можуть поширюватися на ліву руку, щелепу, живіт, спину та / або плечі. Іншими симптомами можуть бути: нудота / блювота, пітливість, задишка, серцебиття, (сильна) втома та / або запаморочення. У пацієнтів з високим ризиком серцевих захворювань інфаркт може виникати із загальною частотою. Якщо ви пацієнт з високим ризиком, ваш лікар не призначить OSSEOR.
- Згустки крові у венах (тромбоз): біль, почервоніння, набряк ніг, раптовий біль у грудях або утруднене дихання.
Рідкісні (можуть виникнути до 1 з 1000 пацієнтів):
- Ознаки тяжких реакцій гіперчутливості (DRESS): спочатку у вигляді грипоподібних симптомів і висипу на обличчі, потім обширна висипка з високою температурою (нечасто), підвищення рівня ферментів печінки, виявлене в аналізах крові (нечасто), збільшення певного типу білого клітини крові (еозинофілія) (рідко) та збільшення лімфатичних вузлів (нечасто).
Дуже рідко (може виникнути до 1 з 10000 пацієнтів):
- Ознаки потенційно небезпечних для життя шкірних висипань (синдром Стівенса-Джонсона, токсичний епідермальний некроліз): спочатку у вигляді червонуватих мішенеподібних або кругових плям, часто з центральними пухирями на тулубі. Додатковими ознаками можуть бути виразка рота, горла, носа, статевих органів та кон’юнктивіт (опухлі та почервонілі очі). Ці потенційно небезпечні для життя висипання на шкірі часто супроводжуються симптомами грипу. Висип може прогресувати до утворення пухирів по всьому тілу або лущення шкіри.
Інші можливі побічні ефекти
Дуже часто (можуть вражати більш ніж 1 з 10 осіб): свербіж, кропив’янка, висип на шкірі, ангіоневротичний набряк (наприклад, набряк обличчя, язика або горла, утруднене дихання або ковтання), біль у кістках, кінцівках, м’язах та / або в суглобах, м’язові судоми.
Часто: блювота, біль у животі, рефлюкс, порушення травлення, запор, метеоризм, утруднення сну, запалення печінки (гепатит), набряк кінцівок, гіперреактивність бронхів (симптоми включають хрипи, задишку та кашель), підвищення рівня м’язів фермент (креатинфосфокіназа). Нудота, діарея, головний біль, екзема, погіршення пам’яті, непритомність, поколювання, запаморочення, запаморочення. Однак ці ефекти є легкими та тимчасовими і зазвичай не вимагають припинення лікування. Скажіть своєму лікарю, якщо будь -який із цих побічних ефектів стане тривожним або тривалим.
Нечасті (можуть виникнути до 1 із 100 осіб): судоми, подразнення слизової оболонки рота (наприклад, виразка рота та запалення ясен), випадання волосся, сплутаність свідомості, нудота, сухість у роті, подразнення шкіри.
Рідко: зменшення вироблення клітин крові в кістковому мозку. Якщо ви припинили терапію через реакції гіперчутливості, не слід перезапускати OSSEOR.
Повідомлення про побічні ефекти
Якщо у Вас виникли будь -які побічні ефекти, зверніться до лікаря або фармацевта, що включає будь -які можливі побічні ефекти, не зазначені у цій інструкції. Ви також можете повідомляти про побічні ефекти безпосередньо за допомогою національної системи звітності, наведеної у Додатку V. Повідомляючи про побічні ефекти, ви можете допомогти надати більше інформації про безпеку застосування цього лікарського засобу.
Термін придатності та утримання
Зберігайте цей препарат подалі від очей та недоступного для дітей місця.
Не використовуйте цей препарат після закінчення терміну придатності, зазначеного на картонній упаковці та пакетику після слова EXP. Термін придатності відноситься до останнього дня цього місяця. Після розчинення у воді суспензія стабільна протягом 24 годин.
Однак рекомендується випити суспензію одразу після приготування (див. Розділ 3). Цей лікарський засіб не вимагає особливих умов зберігання.
Не викидайте будь -які ліки через стічні води або побутові відходи. Запитайте у фармацевта, як викидати ліки, якими ви більше не користуєтесь. Це допоможе захистити навколишнє середовище.
Склад та лікарська форма
Що містить OSSEOR
- Діюча речовина - ранелат стронцію. Кожен пакетик містить 2 г ранелату стронцію.
- Інші інгредієнти: аспартам (Е 951), мальтодекстрин, маніт (Е 421).
Опис того, як виглядає OSSEOR, та вміст пакета
OSSEOR доступний у пакетиках, що містять жовті гранули для пероральної суспензії. OSSEOR поставляється в упаковках по 7, 14, 28, 56, 84 або 100 пакетиків. Не всі розміри упаковок можна продавати.
Джерело з інформацією про упаковку: AIFA (Італійське агентство з лікарських засобів). Вміст, опублікований у січні 2016 р. Наявна інформація може бути не актуальною.
Щоб мати доступ до найновішої версії, бажано зайти на веб-сайт AIFA (Італійське агентство з лікарських засобів). Відмова від відповідальності та корисна інформація.
01.0 НАЗВА ЛЕКАРСТВЕННОГО ПРОДУКТУ
OSSEOR 2G ГРАНУЛЯТ ДЛЯ УСНОЇ ПІДВІСКИ
▼ Лікарський засіб підлягає додатковому моніторингу. Це дозволить швидко ідентифікувати нову інформацію про безпеку. Медичних працівників просять повідомляти про будь -які підозрювані побічні реакції. Див. Розділ 4.8 для отримання інформації про те, як повідомляти про побічні реакції.
02.0 ЯКІСНИЙ І КІЛЬКІСНИЙ СКЛАД
Кожен пакетик містить 2 г ранелату стронцію.
Допоміжна речовина з відомим ефектом:
кожен пакетик також містить 20 мг аспартаму (Е 951)
Повний список допоміжних речовин див. У розділі 6.1.
03.0 ФАРМАЦЕВТИЧНА ФОРМА
Гранули для пероральної суспензії
Жовтий гранулят
04.0 КЛІНІЧНА ІНФОРМАЦІЯ
04.1 Терапевтичні показання
Лікування важкого остеопорозу:
• у жінок у постменопаузі,
• у дорослих чоловіків,
з високим ризиком переломів, лікування яких іншими лікарськими засобами, дозволеними для лікування остеопорозу, неможливе, наприклад, через протипоказання або непереносимість.
У жінок у постменопаузі стронцій ранелат знижує ризик переломів хребців та стегон (див. Розділ 5.1).
Рішення про призначення стронцію ранелату має ґрунтуватися на оцінці загальних ризиків для окремого пацієнта (див. Розділи 4.3 та 4.4).
04.2 Дозування та спосіб введення
Лікування повинен розпочинати тільки лікар, який має досвід лікування остеопорозу.
Дозування
Рекомендована доза становить один пакетик по 2 г один раз на день для перорального застосування.
Через природу стану, що піддається лікуванню, ранелат стронцію призначений для тривалого застосування.
Всмоктування стронцію ранелату зменшується з їжею, молоком та його похідними, тому OSSEOR слід вводити між прийомами їжі. Через повільне всмоктування OSSEOR слід приймати перед сном, бажано щонайменше через дві години після їжі (див. Розділи 4.5 та 5.2).
Пацієнтам, які отримують ранелат стронцію, слід приймати вітамін D та добавки кальцію, якщо їх дієта недостатня.
Пацієнти літнього віку
Ефективність та безпеку стронцію ранелату були продемонстровані у великій вибірці дорослих чоловіків та жінок у постменопаузі будь -якого віку (до 100 років із включенням) з остеопорозом. Не потрібно коригувати дозування щодо віку.
Пацієнти з нирковою недостатністю
Пацієнтам з тяжкою нирковою недостатністю (кліренс креатиніну менше 30 мл / хв) (див. Розділи 4.4 та 5.2) ранелат стронцію не рекомендується. Пацієнтам з нирковою недостатністю легкого та помірного ступеня коригування дози не потрібно (кліренс креатиніну 30 - 70 мл) / хв) (див. розділи 4.4 та 5.2).
Пацієнти з печінковою недостатністю
У пацієнтів з печінковою недостатністю коригування дози не потрібне (див. Розділ 5.2).
Педіатричне населення
Безпека та ефективність застосування OSSEOR у дітей віком до 18 років не встановлені.
Спосіб введення
Для перорального застосування
Гранули пакетиків слід брати після суспензії в склянці, що містить мінімум 30 мл води (приблизно одну третину звичайної склянки).
Хоча дослідження використання показали, що ранелат стронцію залишається стабільним у суспензії протягом 24 годин після приготування, суспензію слід випити одразу після приготування.
04.3 Протипоказання
• Підвищена чутливість до активної речовини або до будь -якої з допоміжних речовин, перерахованих у розділі 6.1.
• Поточна або попередня венозна тромбоемболія (ВТЕ), включаючи тромбоз глибоких вен та легеневу емболію.
• Тимчасова або постійна іммобілізація через, наприклад, операцію або тривале перебування в ліжку.
• Встановлена, поточна або попередня історія ішемічної хвороби серця, захворювань периферичних артерій та / або цереброваскулярних захворювань.
• неконтрольована гіпертензія.
04.4 Спеціальні попередження та відповідні запобіжні заходи щодо використання
Ішемічні серцеві події
В об'єднаному аналізі плацебо-контрольованих рандомізованих клінічних випробувань у пацієнтів з постменопаузальним остеопорозом було відзначено значне збільшення інфаркту міокарда у пацієнтів, які отримували OSSEOR, порівняно з тими, які отримували плацебо (див. Розділ 4.8).
Перед початком лікування пацієнтів слід оцінити на серцево -судинний ризик.
Пацієнтів зі значними факторами ризику серцево -судинних подій (наприклад, гіпертонія, гіперліпідемія, цукровий діабет, тютюнопаління) слід застосовувати лише стронцію ранелат тільки після ретельного обстеження (див. Розділи 4.3 та 4.8).
Під час лікування OSSEOR ці серцево-судинні ризики слід контролювати через регулярні проміжки часу, зазвичай кожні 6-12 місяців.
Лікування слід припинити, якщо у пацієнта розвивається ішемічна хвороба серця, хвороба периферичних артерій, цереброваскулярна хвороба або якщо гіпертонія не контролюється (див. Розділ 4.3).
Венозна тромбоемболія
У плацебо-контрольованих дослідженнях фази III лікування ранелатом стронцію асоціювалося зі збільшенням щорічної захворюваності на венозну тромбоемболію (ВТЕ), включаючи легеневу емболію (див. Розділ 4.8). Причина такого збільшення невідома. OSSEOR протипоказаний пацієнтам з попередньою венозною тромбоемболією (див. Розділ 4.3), тому його слід з обережністю застосовувати пацієнтам з ризиком ВТЕ.
Під час лікування пацієнтів старше 80 років з ризиком ВТЕ слід переоцінити необхідність продовження лікування OSSEOR. Лікування препаратом OSSEOR слід якомога швидше припинити у разі захворювання або стану, що призводить до іммобілізації (див. Розділ 4.3), і вжити відповідних профілактичних заходів. і пацієнт повністю рухливий. Коли виникає ВТЕ, операцію OSSEOR слід припинити.
Застосування у пацієнтів з нирковою недостатністю
За відсутності даних про безпеку кісток у пацієнтів з тяжкою нирковою недостатністю, які отримують стронцій ранелат, OSSEOR не рекомендується пацієнтам з кліренсом креатиніну менше 30 мл / хв. (див. розділ 5.2). Відповідно до належної клінічної практики, пацієнтам з хронічною нирковою недостатністю рекомендується періодичний контроль функції нирок. Продовження терапії OSSEOR у пацієнтів з тяжкою нирковою недостатністю слід оцінювати індивідуально.
Шкірні реакції
Під час застосування OSSEOR повідомлялося про небезпечні для життя шкірні реакції (синдром Стівенса-Джонсона (SJS), токсичний епідермальний некроліз (NET) та медикаментозну висип з еозинофілією та системними симптомами (DRESS)).
Пацієнтів слід поінформувати про ознаки та симптоми та ретельно стежити за шкірними реакціями. Найбільший ризик захворюваності на SJS або NET є протягом перших кількох тижнів лікування та протягом 3-6 тижнів для DRESS.
Якщо ознаки та симптоми SJS або NET (наприклад, прогресуюча шкірна висипка, часто з утворенням пухирів та слизових оболонок) або DRESS (наприклад, висип, лихоманка, еозинофілія та системне ураження (наприклад, аденопатія, гепатит, нефропатія та захворювання легенів) виникають інтерстиціально), лікування OSSEOR слід негайно припинити.
Найкращі результати в лікуванні SJS, NET або DRESS досягаються після ранньої діагностики та негайного припинення застосування будь -якого підозрілого препарату. Раннє припинення лікування пов'язане з кращим прогнозом. Клінічна картина DRESS зникала в більшості випадків після припинення лікування OSSEOR та початку терапії кортикостероїдами, якщо це було необхідно. Одужання може бути повільним, і в деяких випадках повідомлялося про рецидиви синдрому після припинення терапії кортикостероїдами.
У пацієнтів, у яких за допомогою OSSEOR розвинувся SJS, NET або DRESS, терапію OSSEOR більше не слід розпочинати.
У пацієнтів азіатського походження повідомлялося про більш високу, хоча й досі рідкість, реакцію гіперчутливості, включаючи шкірну висип, SJS або NET.
Взаємодія з лабораторними дослідженнями
Стронцій перешкоджає колориметричним методам визначення концентрації кальцію в крові та сечі. Тому в клінічній практиці для забезпечення точної оцінки концентрації кальцію в крові та сечі необхідно використовувати атомно -емісійну спектрометрію з індуктивно зв’язаною плазмою або атомно -абсорбційну спектрометрію.
Допоміжна речовина
OSSEOR містить аспартам, джерело фенілаланіну, який може бути небезпечним для пацієнтів з фенілкетонурією.
04.5 Взаємодія з іншими лікарськими засобами та інші форми взаємодії
Їжа, молоко та його похідні та лікарські засоби, що містять кальцій, можуть зменшити біодоступність ранелату стронцію приблизно на 60 - 70%. Тому введення OSSEOR та цих продуктів має бути розділене принаймні на дві години (див. Розділи 4.2 та 5.2).
Оскільки двовалентні катіони можуть утворювати погано абсорбується комплекс з пероральними тетрациклінами (наприклад, доксицикліном) та хінолоновими антибіотиками (наприклад, ципрофлоксацином) на рівні шлунково-кишкового тракту, одночасне застосування стронцію ранелату з цими лікарськими засобами не рекомендується. Як запобіжний захід, застосування OSSEOR слід припинити під час лікування пероральними тетрациклінами або хінолоновими антибіотиками.
Клінічне дослідження в природних умовах про взаємодію з лікарськими засобами показало, що вживання гідроксидів алюмінію та магнію за дві години до або одночасно з ранелатом стронцію спричинило незначне зменшення абсорбції ранелату стронцію (зменшення AUC на 20-25%). абсорбція залишалася практично незмінною при введенні антациду через дві години після стронцію ранелату. Тому краще приймати антациди принаймні через дві години після прийому OSSEOR. Однак, оскільки рекомендується приймати OSSEOR перед сном, коли цей режим дозування не застосовується , одночасне застосування залишається прийнятним.
Ніякої взаємодії з прийомом пероральних добавок вітаміну D не спостерігалося.
У клінічних випробуваннях не було продемонстровано жодної клінічної взаємодії та значного збільшення рівня стронцію в крові з лікарськими засобами, які в сучасній практиці зазвичай призначаються одночасно з OSSEOR, включаючи: нестероїдні протизапальні препарати (включаючи ацетилсаліцилову кислоту) , аніліди (такі як парацетамол), блокатори Н2 та інгібітори протонної помпи, діуретики, дигоксин та серцеві глікозиди, органічні нітрати та інші судинорозширювальні засоби при серцевих захворюваннях, блокатори кальцієвих каналів, бета-блокатори, інгібітори АПФ, антагоністи ангіотензину II, селективні бета-2- агоністи адренергічних рецепторів, пероральні антикоагулянти, інгібітори агрегації тромбоцитів, статини, фібрати та похідні бензодіазепінів.
04.6 Вагітність та лактація
Вагітність
Дані про застосування стронцію ранелату вагітним жінкам відсутні. Дослідження на тваринах показали, що у високих дозах оборотні кісткові ефекти у потомства щурів та кроликів, які лікувалися під час вагітності (див. Розділ 5.3). лікування слід припинити.
Час годування
Фізико-хімічні дані свідчать про екскрецію ранелату стронцію в грудне молоко. OSSEOR не слід застосовувати під час лактації.
Родючість
У дослідженнях на тваринах не було виявлено жодного впливу на фертильність чоловіків і жінок.
04.7 Вплив на здатність керувати автомобілем та працювати з механізмами
Ранлат стронцію не впливає або має незначний вплив на здатність керувати автомобілем або працювати з механізмами.
04.8 Побічні ефекти
Короткий опис профілю безпеки
OSSEOR вивчали у клінічних випробуваннях, в яких брали участь приблизно 8000 осіб. Довгострокова безпека оцінювалася у дослідженнях фази III у жінок у постменопаузі з остеопорозом, які отримували лікування протягом 60 місяців із застосуванням стронцію ранелату 2 г / день (n = 3352) або плацебо (n = 3317). Середній вік на момент включення становив 75 років, а 23% зарахованих пацієнтів були у віці від 80 до 100 років.
В об’єднаному аналізі рандомізованих плацебо-контрольованих досліджень у пацієнтів з остеопорозом у постменопаузі найпоширенішими побічними реакціями були нудота та діарея, про які зазвичай повідомлялося на початку лікування, без істотних відмінностей між групами на пізніх стадіях. Припинення терапії відбувається переважно через нудоту.
Не було ніякої різниці в характері побічних реакцій між групами лікування, незалежно від того, чи були пацієнти молодше чи старше 80 років на момент включення.
Таблиця побічних реакцій
Під час клінічних випробувань та / або під час постмаркетингового застосування стронцію ранелату повідомлялося про такі побічні реакції. Нижче наведені побічні реакції за такою умовою: дуже часто (≥ 1/10); часто (≥ 1/100,
§ Частота клінічних випробувань була подібною у групі препаратів та групі плацебо.
* Повідомляється як рідкість в азіатських країнах.
# Для побічних реакцій, які не спостерігалися у клінічних випробуваннях, верхня межа 95% -ного довірчого інтервалу не перевищує 3 / X, причому X представляє загальний розмір вибірки з усіх клінічних випробувань та відповідних досліджень.
кістково -м'язової фракції, що перевищує верхню межу норми в 3 рази. У більшості випадків ці значення спонтанно нормалізувалися без будь -яких змін у терапії.
Опис окремих побічних реакцій
Венозна тромбоемболія
У дослідженнях фази III щорічна частота випадків венозної тромбоемболії (ВТЕ), що спостерігалася протягом 5 років, становила приблизно 0,7% з відносним ризиком 1,4 (95% ДІ = [1,0; 2, 0]) у пацієнтів, які отримували ранелат стронцію порівняно з плацебо (див. розділ 4.4).
Інфаркт міокарда
У зведеному аналізі плацебо-контрольованих рандомізованих клінічних досліджень у пацієнтів з постменопаузальним остеопорозом було відзначено значне збільшення інфаркту міокарда у пацієнтів, які отримували ранелат стронцію порівняно з пацієнтами, які отримували плацебо (1,7% порівняно з 1,1%), з відносним ризиком 1,6 (95% ДІ = [1,07; 2,38]).
Повідомлення про підозрювані побічні реакції
Повідомлення про підозрювані побічні реакції, що виникають після реєстрації лікарського засобу, є важливими, оскільки вони дозволяють постійно контролювати співвідношення користі / ризику лікарського засобу. Медичних працівників просять повідомляти про будь -які підозрювані побічні реакції через національну систему звітності.
04.9 Передозування
Симптоми
У клінічному дослідженні, що оцінювало повторне введення 4 г стронцію ранелату щодня протягом більше 25 днів у здорових жінок у постменопаузі, було виявлено хорошу переносимість. Одноразове введення доз до 11 г у молодих здорових добровольців чоловічої статі не викликало особливих симптомів.
Управління
Зі спостережень за епізодами передозування в клінічних дослідженнях (до 4 г / добу протягом максимального періоду часу 147 днів) клінічно значущих ефектів не виявлено.
Введення молока або антацидів може бути корисним для зменшення абсорбції активного інгредієнта. У разі значного передозування може бути розглянута можливість викликати блювоту для усунення неактивного інгредієнта.
05.0 ФАРМАКОЛОГІЧНІ ВЛАСТИВОСТІ
05.1 Фармакодинамічні властивості
Фармакотерапевтична група: Препарати для лікування захворювань кісток - Інші препарати, що впливають на структуру та мінералізацію кісток, код АТС: M05BX03
Механізм дії
В пробірці, ранелат стронцію:
- збільшує утворення кісток у культурах кісткової тканини, а також реплікацію попередників остеобластів та синтез колагену у культурах кісткових клітин;
- зменшує резорбцію кісток за рахунок зменшення диференціації остеокластів та їх резорбційної активності.
Це визначає відновлення балансу кісткового обміну на користь його формування.
Активність ранелату стронцію була продемонстрована в кількох експериментальних дослідженнях. Зокрема, у інтактних щурів ранелат стронцію збільшує трабекулярну кісткову масу, кількість і товщину трабекул, що призводить до поліпшення міцності кісток.
Стронцій в основному абсорбується на кристалічній поверхні, і лише в обмеженій мірі він замінює кальцій у кристалі апатиту у новоутвореній кістці як у тварин, так і у людей, що піддаються лікуванню. Ранелат стронцію не змінює характеристик кісткового кристала. У біопсіях кісток гребеня клубової кістки, взятих після обробки стронцію ранелатом 2 г / добу протягом 60 місяців у дослідженнях фази III, не було виявлено ніякого шкідливого впливу на якість кісток або мінералізацію.
Сукупні ефекти розподілу стронцію в кістках (див. Розділ 5.2) та більш високе поглинання рентгенівського випромінювання стронцію порівняно з кальцієм призводять до збільшення значення кісткової денситометрії (МЩКТ), виміряної за допомогою двопроменевої фотонної абсорбціометрії ( DXA). Наявні дані вказують на те, що ці фактори становлять приблизно 50% спостережуваних змін у МЩКТ за 3 роки лікування OSSEOR 2 г / добу. Це слід враховувати при оцінці змін у МЩКТ під час лікування OSSEOR. У дослідженнях фази III, які продемонстрували ефективність лікування OSSEOR щодо зменшення переломів, OSSEOR збільшував середню МЩКТ від включення приблизно на 4% щорічно на поперекових хребцях і на 2% щорічно на рівні поперекових хребців. Шийки стегнової кістки, що досягає , залежно від дослідження, відповідно від 13 до 15% та від 5 до 6% через 3 роки.
У дослідженнях фази III, порівняно з плацебо, біохімічні маркери утворення кістки (специфічна лужна фосфатаза та С-кінцевий пропептид проколагену типу I) були збільшені, а також показники резорбції кістки (C-телопептид сироватки та зшивання N-телопептиду в сечі) зменшився з третього місяця до третього року лікування.
На додаток до первинних фармакологічних ефектів ранелату стронцію, спостерігалося незначне зниження рівня кальцію в сироватці крові та гормону паращитовидних залоз (ПТГ), підвищення концентрації фосфору в крові та загальної активності лужної фосфатази без клінічних наслідків.
Клінічна ефективність
Остеопороз визначається як МЩКТ хребта або тазостегнового суглоба, що на 2,5 або більше стандартних відхилень нижче середнього значення серед молодої нормальної популяції. Деякі фактори ризику пов'язані з постменопаузальним остеопорозом, включаючи низьку кісткову масу, низьку мінеральну щільність кісток, ранню менопаузу, куріння та сімейний анамнез остеопорозу. Клінічним наслідком остеопорозу є переломи. Ризик переломів зростає зі збільшенням кількості факторів ризику.
Лікування постменопаузального остеопорозу
Програма дослідження для оцінки зменшення переломів за допомогою OSSEOR складалася з двох плацебо-контрольованих досліджень фази III: дослідження SOTI та дослідження TROPOS. У дослідженні SOTI взяли участь 1649 жінок у постменопаузі з документально підтвердженим остеопорозом (низька поперекова МЩКТ та поширені переломи хребців) та середнім віком 70 років. У дослідженні TROPOS взяла участь 5 091 жінка в постменопаузі з остеопорозом (низький МЩКТ шийки стегнової кістки та принаймні один перелом у більш ніж половини пацієнтів) та середнім віком 77 років. Разом дослідження SOTI та TROPOS охопили 1556 пацієнтів старше 80 років на момент включення (23,1% досліджуваної популяції). В обох дослідженнях, крім терапії (2 г / день стронцію або плацебо), пацієнти були прийом адекватних добавок кальцію та вітаміну D.
OSSEOR знизив відносний ризик нових переломів хребців на 41% за 3 роки лікування у дослідженні SOTI (таблиця 1). Ефект був значним, починаючи з першого курсу. Аналогічні переваги були продемонстровані у жінок з множинними переломами при зарахуванні. Щодо клінічних переломів хребців (визначених як переломи, пов’язані з болем у спині та / або зменшенням висоти тіла щонайменше на 1 см), відносний ризик зменшився на 38%. OSSEOR також зменшила кількість пацієнтів зі зменшеною „висотою тіла щонайменше 1 см порівняно з плацебо. Оцінка якості життя за спеціальною шкалою QUALIOST, а також загальні показники сприйняття здоров'я за загальною шкалою SF-36 свідчать про переваги OSSEOR порівняно з плацебо.
Ефективність OSSEOR у зниженні ризику нових переломів хребців була підтверджена дослідженням TROPOS навіть для пацієнтів з остеопорозом без переломів ламкості на момент включення.
Спільний аналіз досліджень SOTI та TROPOS показав, що у пацієнтів старше 80 років на момент включення OSSEOR знизив відносний ризик нових переломів хребців на 32% за 3 роки лікування (частота 19,1% з ранелат стронцію проти 26,5% з плацебо).
В одному аналізі в результаті пацієнтів у дослідженнях SOTI та TROPOS з МПК поперекових хребців та / або шиї стегнової кістки в остеопенічному діапазоні на момент включення та без поширених переломів, але принаймні з одним додатковим фактором ризику перелому (N = 176), OSSEOR знизив ризик першого перелому хребця на 72% протягом 3 років (частота переломів хребців 3,6% з ранелатом стронцію проти 12,0% з плацебо).
Аналіз в результаті була проведена в підгрупі пацієнтів з TROPOS, що представляють особливий медичний інтерес та з високим ризиком переломів [визначено як пацієнти з Т-показником МЩКТ шийки стегнової кістки ≤-3 SD (діапазон виробників, що відповідає -2,4 SD відповідно до NHANES III) та " вік> 74 роки (n = 1977, тобто 40% досліджуваної популяції TROPOS)].
У цій групі протягом 3 років лікування OSSEOR знизив ризик переломів стегна на 36% порівняно з плацебо (таблиця 2).
Лікування остеопорозу у людини
Ефективність OSSEOR була продемонстрована у чоловіків з остеопорозом у подвійному сліпому, плацебо-контрольованому 2-річному дослідженні, основний аналіз якого був проведений через рік у 243 пацієнтів (популяція Намір лікувати, 161 пацієнт, що отримував ранелат стронцію) з високим ризиком переломів (середній вік 72,7 року; середня поперекова МЩКТ з Т -показником -2,6; 28% поширений перелом хребця).
Усі пацієнти щодня отримували добавки кальцію (1000 мг) та вітаміну D (800 МО).
Статистично значуще збільшення показників МЩКТ спостерігалося вже через 6 місяців від початку лікування OSSEOR порівняно з плацебо.
Статистично значуще збільшення середніх показників МЩКТ поперекового відділу хребта спостерігалося протягом 12-місячного періоду, основний критерій ефективності (E (SE) = 5,32%; 95% ДІ = [3,86; 6,79]: p менопауза.
Спостерігалося статистично значуще збільшення МЩКТ шийки стегнової кістки та загальної МЩКТ стегнової кістки (стор
Педіатричне населення
Європейське агентство з лікарських засобів відмовилося від зобов’язання подавати результати досліджень з OSSEOR у всіх підгрупах педіатричної популяції з остеопорозом (див. Розділ 4.2 для інформації про застосування у педіатрії).
05.2 "Фармакокінетичні властивості
Ранелат стронцію складається з 2 стабільних атомів стронцію та молекули ранелової кислоти, органічного компонента, який представляє найкращий компроміс з точки зору молекулярної маси, фармакокінетики та прийнятності лікарського засобу. Фармакокінетику стронцію та ранелової кислоти оцінювали у здорових молодих добровольців чоловічої статі, у здорових жінок у постменопаузі та під час тривалого лікування у чоловіків з остеопорозом та у жінок з постменопаузальним остеопорозом, включаючи літніх людей.
Поглинання, розподіл та зв'язування ранелової кислоти з білками плазми низькі через її високу полярність. Немає накопичення ранелової кислоти та доказів метаболізму у тварин та людини.Ранелова кислота, що поглинається, швидко виводиться у незміненому вигляді із сечею.
Поглинання
Абсолютна біодоступність стронцію становить 25% (діапазон 19-27%) після пероральної дози 2 г стронцію ранелату. Максимальна концентрація у плазмі крові досягається через 3-5 годин після одноразової дози 2 г.
Рівноважний стан досягається через 2 тижні лікування. Вживання стронцію ранелату разом з кальцієм або їжею знижує біодоступність стронцію приблизно на 60-70%порівняно з введенням через 3 години після їжі. Через відносно повільне всмоктування стронцію, слід уникати споживання їжі та кальцію до та після прийому OSSEOR. . Оральні добавки вітаміну D не заважають впливу стронцію.
Розповсюдження
Об'єм розподілу стронцію становить приблизно 1 л / кг. Зв’язування стронцію з білками плазми людини є низьким (25%), і стронцій має «високу спорідненість до кісткової тканини. Вимірювання концентрації стронцію в біоптатах кісток гребеня клубової кістки пацієнтів, які отримували до 60 г ранелату стронцію до 60 місяців. , показує, що концентрація стронцію в кістках може досягати плато приблизно через 3 роки лікування. Немає даних про пацієнтів, які б демонстрували кінетику елімінації стронцію з кістки після припинення прийому.
Біотрансформація
Як двовалентний катіон, стронцій не метаболізується. Ранлат стронцію не інгібує ферментний комплекс цитохрому Р450.
Ліквідація
Елімінація стронцію не залежить від часу та дози.Ефективний період напіввиведення стронцію становить приблизно 60 годин. Екскреція стронцію відбувається через нирки та шлунково -кишковий тракт. Його плазмовий кліренс становить приблизно 12 мл / хв (CV 22%), а нирковий кліренс - приблизно 7 мл / хв (CV 28%).
Фармакокінетика, зокрема, популяцій
Пацієнти літнього віку
Фармакокінетичні дані про популяцію не показали кореляції між віком та очевидним кліренсом стронцію у цільовій популяції.
Ниркова недостатність
У пацієнтів з помірною або помірною нирковою недостатністю (кліренс креатиніну 30-70 мл / хв) кліренс стронцію зменшується зі зменшенням кліренсу креатиніну (приблизно на 30% зменшується діапазон кліренсу креатиніну на 30-70 мл / хв); це призводить до збільшення у дослідженнях фази III 85% пацієнтів мали кліренс креатиніну між 30 і 70 мл / хв, 6% - менше 30 мл / хв до включення, а середній кліренс креатиніну становив 50 мл / хв. для пацієнтів з помірною та помірною нирковою недостатністю коригування дози не потрібне.Фармакокінетичних даних для пацієнтів з тяжкою нирковою недостатністю немає (кліренс креатиніну
Печінкова недостатність
Фармакокінетичних даних щодо пацієнтів з печінковою недостатністю немає.Через фармакокінетичні властивості стронцію ефекту не очікується.
05.3 Дані доклінічної безпеки
Неклінічні дані не виявляють особливої небезпеки для людини на основі звичайних досліджень фармакологія безпеки, генотоксичність, канцерогенний потенціал.
У гризунів хронічне пероральне введення високих доз ранелату стронцію призвело до аномалій кісток та зубів, що полягали переважно у спонтанних переломах та уповільненій мінералізації, які були оборотними після припинення лікування. Ці ефекти були виявлені з рівнем стронцію в кістках у 2-3 рази вище, ніж у людей після лікування, яке тривало до 3 років.
Дослідження токсичності для розвитку призвели до аномалій кісток та зубів у потомства щурів та кроликів (наприклад, схилення довгих кісток та хвилястих ребер). Ці ефекти є оборотними через 8 тижнів після припинення лікування.
Оцінка екологічного ризику (ERA)
Оцінка екологічного ризику ранелату стронцію була проведена відповідно до європейських настанов щодо ЕРА.
Ранелат стронцію не становить загрози для навколишнього середовища.
06.0 ФАРМАЦЕВТИЧНА ІНФОРМАЦІЯ
06.1 Допоміжні речовини
Аспартам (E951)
Мальтодекстрин
Маніт (E421)
06.2 Несумісність
Не актуально.
06.3 Строк дії
- 3 роки.
- Після розчинення у воді суспензія стабільна протягом 24 годин. Однак рекомендується випити суспензію одразу після приготування (див. Розділ 4.2).
06.4 Особливі умови зберігання
Цей лікарський засіб не вимагає особливих умов зберігання.
Щодо умов зберігання після розчинення лікарського засобу, див. Розділ 6.3.
06.5 Характер негайної упаковки та вміст упаковки
Паперові / поліетиленові / алюмінієві / поліетиленові пакети.
Пачки
Упаковки по 7, 14, 28, 56, 84 або 100 пакетиків.
Не всі розміри упаковок можна продавати.
06.6 Інструкції з використання та поводження
Ніяких спеціальних вказівок.
07.0 ВЛАСНИК РОЗРОБНИЦТВА
LES LABORATOIRES SERVIER
50, вулиця Карно
92284 Suresnes cedex
Франція
08.0 НОМЕР РОЗВИТКУ З РОБОТИ
ЄС/1/04/287/001
ЄС/1/04/287/002
ЄС/1/04/287/003
ЄС/1/04/287/004
ЄС/1/04/287/005
ЄС/1/04/287/006
036588061
036588022
036588034
036588046
036588010
036588059
09.0 ДАТА ПЕРШОГО ДОЗВІЛЕННЯ АБО ОНОВЛЕННЯ ДОЗВІЛЛЯ
Дата першого дозволу: 21 вересня 2004 року
Дата останнього оновлення: 21 вересня 2014 року